
- •Государственное образовательное учреждение высшего профессионального образования Санкт-Петербургский государственный горный институт им. Г.В. Плеханова (технический университет)
- •Конспект практических занятий физическая химия
- •Применение первого начала термодинамики к процессам в идеальных газах
- •Расчет теплоемкости Вычисление средней теплоемкости
- •Расчет теплоемкости по Нейману и Коппу
- •Расчет теплоемкости твердого вещества по Эйнштейну-Дебаю
- •Расчет теплоемкости газа по квантово-статистической теории
- •Расчет количества теплоты для нагревания/охлаждения вещества
- •Вычисление теплового эффекта химической реакции Вычисление теплового эффекта химической реакции через систему термохимических уравнений
- •Вычисление теплового эффекта химической реакции при обычных условиях
- •Вычисление теплового эффекта реакций в водных растворах по стандартным энтальпиям образования гидратированных ионов
- •Вычисление теплового эффекта при заданной температуре
- •Вычисление теплового баланса процесса
- •Вычисление изменения энтропии химической реакции Вычисление изменения энтропии химической реакции при обычных условиях
- •Вычисление изменения энтропии химической реакции при заданной температуре
- •Вычисление энергии Гиббса химической реакции и определение направления протекания процесса Вычисление энергии Гиббса для реакций, протекающих при обычных условиях
- •Вычисление изобарно-изотермического потенциала реакций в водных растворах по стандартным энергиям Гиббса образования гидратированых ионов
- •Вычисление энергии Гиббса химической реакции при заданной температуре
- •Использование закона действующих масс для расчета состава равновесной газовой смеси
- •Уравнение изотермы химической реакции (влияние состава на равновесие)
- •Расчет энергии Гиббса и константы равновесия при заданной температуре
- •6. Вычислить изменение энтропии реакции при 850 k:
- •8. Вычислить константу равновесия данной реакции по уравнению:
- •Метод Темкина-Шварцмана
- •Метод приведенных энергий Гиббса
- •Уравнение изобары химической реакции
- •1) Константу равновесия при данной температуре,;
- •2) Тепловой эффект реакции.
Расчет теплоемкости Вычисление средней теплоемкости
Средней теплоемкостью системы называют количество тепла, отнесенное к вызванному им повышению температуры системы:
![]()
связь между средней и истинной теплоемкостью:
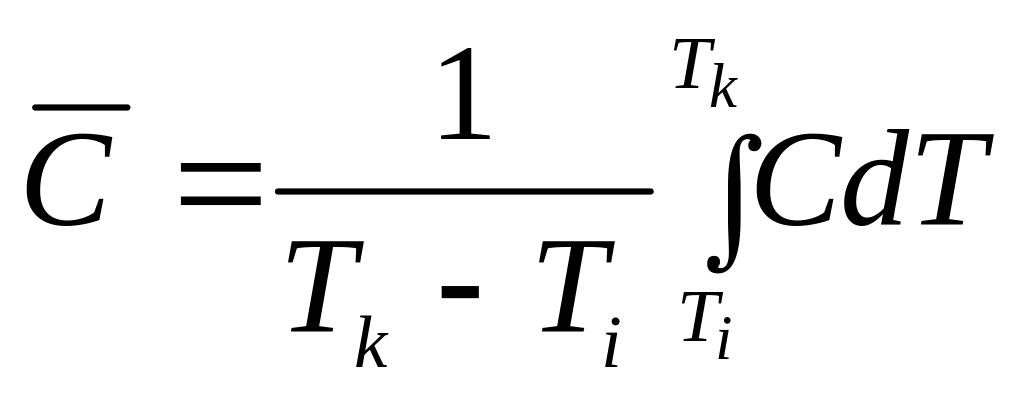
![]()
Пример 1. Вычислить значение средней теплоемкости кальцита (карбоната кальция) для интервала температур 298 – 800 K.
Решение.
1. По таблице 44 «Термодинамические
свойства простых веществ…» определить
коэффициенты уравнения Келли:
![]() .
.
2. Проинтегрировать уравнение для средней теплоемкости, использовав для истинной теплоемкости ряд Келли для неорганических веществ:

3. Подставить численные значения температур и коэффициентов уравнения Келли и произвести вычисления:

Пример 2. Вычислить значение средней теплоемкости ацетилена для интервала температур 298 – 800 K.
Решение.
1. По таблице 44 «Термодинамические
свойства простых веществ…» определить
коэффициенты уравнения Келли:
![]() .
.
2. Проинтегрировать уравнение для средней теплоемкости, использовав для истинной теплоемкости ряд Келли для органических веществ:

3. Подставить численные значения температур и коэффициентов уравнения Келли и произвести вычисления:

Расчет теплоемкости по Нейману и Коппу
Правило Ф.Э.Неймана и Г.Коппа: мольная теплоемкость сложного твердого тела при комнатных температурах аддитивно складывается из атомных теплоемкостей отдельных атомов. Для всех атомов, находящихся в Периодической системе за калием, считают Ср = 26,0 Дж/(моль К), а для более легких элементов принимают следующие значения:
Элемент С Н В Si О F Р S
Ср, Дж/(моль·К) 7,6 9,6 11,3 15,9 16,8 21,0 22,6 22,6
Пример 1. для Са3(РО4)2 Ср = 326.0+222,6+816,8 = 257,6 Дж/(моль К), а табличное значение Ср = 227,8 Дж/(моль К), т.е. в данном случае ошибка (около 13 %) приемлема для грубых оценок.
Расчет теплоемкости твердого вещества по Эйнштейну-Дебаю
![]()
![]() – функция
теплоемкости Эйнштейна.
– функция
теплоемкости Эйнштейна.
Характеристическая
температура
![]() определяется из эксперимента или
вычислена по полуэмпирическим уравнениям,
например, по уравнению Линдемана:
определяется из эксперимента или
вычислена по полуэмпирическим уравнениям,
например, по уравнению Линдемана:
 ,
,
где
Тm
– температура плавления, K;
М
– молярная масса; VM
– молярный объем (объем одного моля
вещества),
![]() ,
d
– плотность вещества.
,
d
– плотность вещества.
Пример 1. Вычислить теплоемкость меди для температуры 300 K по Эйнштейну и сопоставить полученное значение со справочными данными.
Решение. 1. По таблице 47 (Характеристическая температура кристаллических веществ) краткого справочника физико-химических величин определить характеристическую температуру; для меди она равна 313 K
2.
Вычислить соотношение
![]()
3. По
таблице 46 «Термодинамические функции
линейного гармонического осциллятора
(по Эйнштейну)» по вычисленному значению
![]() определить функцию теплоемкости по
Эйнштейну:
определить функцию теплоемкости по
Эйнштейну:
![]()
4.
Вычислить теплоемкость меди
![]() .
.
5. Сравнить полученное значение со справочным (24,43 Дж/моль∙K)
Пример 2. Вычислить теплоемкость флюорита (фторида кальция) для температуры 300 K по Дебаю, по Нейману-Коппу и сопоставить полученные значения со справочными данными.
Решение. 1. По таблице 47 (Характеристическая температура кристаллических веществ) краткого справочника физико-химических величин определить характеристическую температуру; для фторида кальция она равна 474 K.
2.
Вычислить соотношение
![]()
3. По
таблице 48 «Термодинамические колебательные
функции кристаллических веществ (по
Дебаю)» по вычисленному значению
определить функцию теплоемкости по
Дебаю:
![]()
4.
Вычислить теплоемкость хлорида натрия
![]() .
.
5. Вычислить теплоемкость хлорида натрия по правилу Неймана-Коппа:
![]()
5. Сравнить полученное значение со справочным (67,03 Дж/моль∙K)
