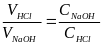- •Введение
- •Общие правила работы в лаборатории
- •Структура отчёта о лабораторных работах
- •Лабораторная работа №1 определение молярной массы эквивалента (эквивалентной массы) металла по объему вытесненного водорода
- •Методика выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №2 зависимость свойств элементов от их положения в периодической системе д.И. Менделеева
- •Методика выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №3 определение тепловых эффектов химических процессов
- •М етодика выполнения работы
- •Результаты измерений
- •Результаты измерений
- •Контрольные вопросы
- •Лабораторная работа №4 приготовление растворов
- •Методика выполнения работы
- •Соотношения массовых долей и плотностей раствора hCl (20єС)
- •Результаты расчетов
- •Плотность водного раствора сульфата никеля при температуре 18 °с
- •Результаты расчетов
- •Контрольные вопросы
- •Лабораторная работа №5 определение молекулярной массы вещества криоскопическим методом
- •Методика выполнения работы
- •Результаты опыта
- •Контрольные вопросы
- •Лабораторная работа №6 скорость химических реакций и химическое равновесие
- •Методика выполнения работы
- •Результаты опыта
- •1/3 2/3 1,0 С, моль/л
- •Результаты опыта
- •Результаты опыта
- •Результаты опыта
- •Контрольные вопросы
- •Лабораторная работа №7 водородный показатель среды. Гидролиз солей
- •Методика выполнения
- •Результаты опыта
- •Контрольные вопросы
- •Лабораторная работа №8 электролитическая диссоциация произведение растворимости
- •Методика выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 9 получение и изучение свойств комплексных соединений
- •Методика выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 10 окислительно-восстановительные реакции
- •Методика выполнения Окислители и восстановители, окислительно-восстановительная двойственность
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций
- •Контрольные вопросы
- •Лабораторная работа № 11 гальванический элемент
- •Методика выполнения
- •Результаты опытов
- •Контрольные вопросы
- •Лабораторная работа № 12 коррозия металлов и защита от неё
- •Методика выполнения
- •Контрольные вопросы
- •Лабораторная работа № 13 электролиз растворов электролитов
- •Методика выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №14 способы водоподготовки
- •Методика выполнения Умягчение воды
- •Контрольные вопросы
- •Лабораторная работа №15 органические вещества и полимеры
- •Методика выполнения Получение и свойства алифатических углеводородов
- •Характерные реакции кислородсодержащих органических соединений
- •Получение полимеров
- •Контрольные вопросы
- •Содержание
Результаты расчетов
Номер колбы |
V HCl, см3 |
V НаОН, см3 |
Расчет |
Погрешность измерений |
1 |
|
V1 |
|
|
2 |
|
V2 |
||
3 |
|
V3 |
||
|
|
Vср |
Опыт №3. Приготовление раствора заданной концентрации из навески твердого вещества и воды
Получить у преподавателя задание на приготовление раствора соли определённой массовой доли. На аналитических весах взвесить заданную массу кристаллогидрата.
Рассчитать массу воды, необходимой для приготовления заданного раствора с учётом кристаллизационной воды в навеске. С помощью мерного цилиндра отмерить расчётное количество воды, имея в виду, что плотность её равна 1 г/см3. Навеску кристаллогидрата поместить в химический стакан при постепенном добавлении отмеренной воды, добиться полного растворения её, осторожно перемешивая раствор стеклянной палочкой. Часть раствора перелить в цилиндр, измерить его плотность ареометром и проверить правильность приготовления раствора, сравнив опытное значение плотности с нижеприведёнными (табл. 4.3):
Таблица 4.3
Плотность водного раствора сульфата никеля при температуре 18 °с
Массовая доля, W |
0,01 |
0,02 |
0,04 |
0,06 |
0,08 |
0,10 |
Плотность с, г/см3 |
1,009 |
1,020 |
1,042 |
1,063 |
1,085 |
1,100 |
Раствор слить в специальную ёмкость (в раковину не выливать!). Произвести пересчёт массовой доли в следующие виды концентрации: молярную, молярную концентрацию эквивалента, молярную и титр.
Результаты расчётов свести в табл. 4.4.
Таблица 4.4
Результаты расчетов
№ задания |
Навеска NiSO4*7H2O г |
Массовая доля |
Количество безводной соли в навеске, г |
Количество воды в навеске, г |
Расчетное количество воды, г |
Приливаемое количество воды, г |
Плотность раствора р, г/см3 |
C(NiSO4), моль/дм3
|
C(NiSO4), моль/дм3
|
µ моль/кг
|
Т, г/см3 |
|
|
|
|
|
|
|
|
|
|
|
|
Сделать выводы.
Контрольные вопросы
1. Что называется концентрацией?
2. Что такое титр, в каких единицах он выражается?
3. Напишите формулу, связывающую титр с молярной концентрацией эквивалента?
4. Дайте определение молярной концентрации; в каких единицах она выражается?
5. Какие виды концентрации изменяют свои численные величины с изменением температуры, а какие – не изменяют?
6. Дайте определение молярной концентрации эквивалента. В каких единицах она выражается?
7. Что называется моляльностью? В каких единицах выражается моляльность раствора?
8. Приведите определение мольно-долевой концентрации. Какие значения она может принимать?
9. Какой объём соляной кислоты, содержащей 0,35 массовых долей НС1, необходимо взять для приготовления 2 дм3 раствора с молярной концентрацией, равной 0,2 моль/дм ?