- •Isbn 5-7629-0807-0 © cПбГэту "лэти", 2007 Введение
- •Основы физико-химического анализа многокомпонентных систем
- •2. ТриангуляциЯ и тетраэдрация. Диаграммы состояния многокомпонентных систем
- •3. Диаграммы "состав – свойство" многокомпонентных систем
- •Контрольные задания
- •4. Прогнозирование полупроводниковых свойств в многокомпонентных системах
- •5. Материалы современной оптоэлектроники и наноэлектроники
- •5.1. Расчет параметров кристаллической решетки и ширины запрещенной зоны в гетероструктурах
- •Контрольные вопросы
- •5.2. Приближение ковалентного радиуса и виртуального кристалла
- •5.3. Построение зонных диаграмм гетероструктуры
- •5.4. Расчет коэффициентов преломления и диэлектрической проницаемости твердых растворов
- •Контрольный вопрос
- •5.5. Расчет упругих напряжений и деформаций
- •Контрольный вопрос
- •5.6. Влияние пластической деформации на электрофизические и оптические свойства материалов и характеристики приборов на гетероструктурах
- •Контрольный вопрос
- •5.7. Твердые растворы на основе соединений а2в6 и а4в6
- •Заключение
- •Приложение
- •197376, С.-Петербург, ул. Проф. Попова, 5
3. Диаграммы "состав – свойство" многокомпонентных систем
В ФХА строят диаграммы "состав – свойство". При этом измеряют различные физические характеристики системы (температуру фазовых переходов, параметр кристаллической решетки, значение ширины запрещенной зоны, теплопроводности, плотности, коэффициента преломления и др.). Аналитические выражения, описывающие фазовые равновесия в многокомпонентных системах, очень громоздкие и лишь приблизительно определяют области сосуществования фаз, поэтому геометрический анализ диаграмм играет исключительно важную роль в материаловедении [13], [14].
Если геометрический образ совокупности составов представлен в виде плоской геометрической фигуры (например, для тройной системы А – В – С или четырехкомпонентных твердых растворов AхB1–хC1–х–yD – треугольник, для четырехкомпонентных твердых растворов AхB1–хCуD1–y – квадрат), то на поверхности этой фигуры могут быть построены кривые, объединяющие все составы с постоянным значением измеряемого свойства. Эта операция аналогична нанесению на географическую карту (геометрический образ) кривых, объединяющих точки местности с одинаковой высотой (свойство).
Для нахождения технологических решений, обеспечивающих получение полупроводниковых твердых растворов, например AхB1–хC, с заданным составом х, необходимо предварительное построение изотерм ликвидуса и изоконцентрат солидуса заданного состава х.
Изотермы ликвидуса могут быть найдены разными методами, например дифференциальным термическим анализом. На практике также распространен визуальный метод регистрации температуры ликвидуса: по значению температуры появления первого кристаллика при охлаждении расплава или по исчезновению последнего кристаллика в расплаве при нагревании.
Изоконцентрата солидуса х – кривая, соединяющая все составы расплавов в системе А – В – С, при охлаждении которых кристаллизуется твердый раствор AхB1–хC с изомолярным составом х0.
Изоконцентраты, как правило, определяют по результатам нахождения состава х первого образовавшегося кристалла или непосредственно в ходе жидкофазной эпитаксии, для чего используют рентгеноспектральный микроанализ или рентгеновский фазовый анализ.
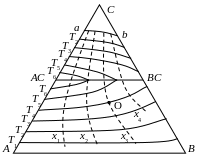
Изотерма ликвидуса – это геометрический образ совокупности точек на поверхности ликвидуса, соответствующих одному и тому же значению температуры фазового перехода. Система изотерм ликвидуса получается пересечением поверхности ликвидуса плоскостями, параллельными основанию концентрационного треугольника. Высота плоскостей над плоскостью основания равна значению температуры ликвидуса. Это значение отмечается на каждой изотерме (рисунок). Для тройной системы А – В – С можно задать любой состав расплава.
|
Изотермы ликвидуса и изоконцентраты солидуса в тройной системе А – В – С |
Задача 3.1. Найти состав загрузки (состав жидкой фазы) тройной системы А – В – С, из которой можно вырастить слой твердого раствора х3 при температуре эпитаксии Т4 (рисунок).
Указание. Находится точка пересечения О (выделена на рисунке) изотермы ликвидуса Т4 и изоконцентраты солидуса х3. Значения атомных долей NA, NB, NC определяются по значению нормированных высот, опущенных из точки О, отвечающей найденному составу, на противоположную сторону концентрационного треугольника (см. задачу 1.1).
Задача 3.2. Найти состав загрузки по условиям задачи 3.1, выраженный в массовых концентрациях.
Решение. Перевод атомных долей в массовые концентрации для тройной системы А – В – С с составом AхBуC1–х–у осуществляется по выражениям:
![]() ;
;
![]() ;
;
![]() ,
где М = хАА + уАВ
+ (1 – х – у)АС;
,
где М = хАА + уАВ
+ (1 – х – у)АС;
Аi – атомная масса i-го компонента (i = А, В, С); Сi – массовая концентрация i-го компонента (i = А, В, С).
Задача 3.3. Показать, как по данным пересечения изотермами ликвидуса и изоконцентратами солидуса квазибинарного разреза АС – ВС восстановить диаграмму состояния для квазибинарной системы (АС)х(ВС)1–х.
Указание. Воспользоваться
решением задачи 1.5. Лучи, исходящие из
вершины С ΔАВС, несут информацию
об отношении
![]() .
Такие лучи, проведенные через точки
пересечения изоконцентрат солидуса и
квазибинарного разреза, дают информацию
о составе жидкой фазы на квазибинарном
разрезе, который находится в равновесии
с составом х твердого раствора
AхB1–хC
или
.
Такие лучи, проведенные через точки
пересечения изоконцентрат солидуса и
квазибинарного разреза, дают информацию
о составе жидкой фазы на квазибинарном
разрезе, который находится в равновесии
с составом х твердого раствора
AхB1–хC
или
A0,5хB0,5(1–х)C.
Задача 3.4. Прямые, связывающие равновесные составы жидкой и твердой фаз, называют конодами. По данным рисунка построить семейство конод для изоконцентраты солидуса с составом х = 0,3.
Указание. По определению, изоконцентрата солидуса х = 0,3 – это совокупность составов жидкой фазы (точек на поверхности ликвидуса), из которых кристаллизуется один и тот же состав твердых растворов AхB1–хС. В связи с этим каждая из конод должна связывать одну (любую) точку изоконцентраты солидуса с единственной точкой на квазибинарном разрезе А0,3В0,7С.
Задача 3.5. Как правило, используются мольные концентрационные треугольники Гиббса. Когда целесообразно в качестве геометрического образа использовать массовый концентрационный треугольник Гиббса?
Ответ. При анализе свойств,
пропорциональных массовым концентрациям
составляющих компонентов. Например,
при построении кривых изогипс (кривых
постоянной интенсивности характеристического
рентгеновского излучения при
рентгеноспектральном микроанализе
тройных металлических сплавов [15]). Метод
изогипс (метод Заславского–Дедегкаева)
заключается в следующем: на сторонах
массового концентрационного треугольника
Гиббса для тройной системы А – В
– С строят калибровочные зависимости
относительной интенсивности
характеристического рентгеновского
излучения аналитической линии i-го
элемента (i = А, В, С):
![]() ,
где
,
где
![]() –
интенсивность характеристического
рентгеновского излучения аналитической
линии i-го элемента в образце с
массовой концентрацией сi;
–
интенсивность характеристического
рентгеновского излучения аналитической
линии i-го элемента в образце с
массовой концентрацией сi;
![]() – аналогичная величина i-го элемента
в эталоне. Каждый из трех элементов
содержится в двух двойных системах,
например, элемент А – в А – В
и А – С. В каждой из этих двух
систем массовая концентрация и значение
относительной интенсивности
характеристического рентгеновского
излучения аналитической линии изменяются
от нуля до максимального значения в
вершине А. Каждому значению
относительной интенсивности i-го
элемента сопоставляется геометрический
образ: точка на стороне треугольника
Гиббса, соответствующая составу двойной
системы с этим значением
– аналогичная величина i-го элемента
в эталоне. Каждый из трех элементов
содержится в двух двойных системах,
например, элемент А – в А – В
и А – С. В каждой из этих двух
систем массовая концентрация и значение
относительной интенсивности
характеристического рентгеновского
излучения аналитической линии изменяются
от нуля до максимального значения в
вершине А. Каждому значению
относительной интенсивности i-го
элемента сопоставляется геометрический
образ: точка на стороне треугольника
Гиббса, соответствующая составу двойной
системы с этим значением
![]() .
.
Система пересекающихся изогипс для двух элементов позволяет определить состав тройной системы. На практике значения измеряются с некоторой погрешностью, поэтому точка пересечения изогипс для двух элементов с некоторой погрешностью соответствует искомому составу тройного соединения.
Погрешность уменьшается, если анализировать результат пересечения изогипс всех трех элементов. В общем случае в результате пересечения получается треугольник несоответствия, центр расположения которого наиболее точно определяет искомый состав.
Задача 3.6. Можно ли использовать метод изогипс для РСМА полупроводниковых твердых растворов AхB1–хC1–х–yD и AхB1–хCyD1–у? Какие особенности методики анализа надо учесть в этом случае?
Ответ. Рассматриваемый метод изогипс, использующий графоаналитические решения на геометрическом образе многокомпонентных систем AхB1–хC1–х–yD и AхB1–хCyD1–у, обладает существенным достоинством – искомые составы х и у определяются только в области существования твердых растворов. Для нахождения х и у предпочтительнее использовать мольные концентрационные геометрические образы (треугольник или квадрат).
Принципиальная применимость концентрационных геометрических образов обеспечивается выбором в качестве эталонов бинарных соединений (например, AD, BD, CD для твердых растворов AхB1–хC1–х–yD). Близость составов эталона и анализируемых образцов в значительной степени нивелирует погрешности определения искомых составов.