
- •Особливості відбору проб на аналіз
- •Консервування та підготовка проб води до аналізу
- •Методи аналізу води
- •1.1. Визначення кольоровості води
- •1.2. Визначення запаху
- •Лабораторна робота № 2 визначення зависей та розчинених речовин
- •2.1. Визначення прозорості води
- •2.2. Визначення каламутності води
- •2.3. Визначення вмісту розчинених речовин (сухого залишку)
- •Лабораторна робота № 3 визначення перманганатної й дихроматної окиснюваності
- •3.1. Визначення перманганатної окиснюваності води
- •3.2. Визначення хімічного споживання кисню
- •3.3. Визначення дихроматної окиснюваності води прискореним методом
- •Лабораторна робота № 4 визначення біохімічного споживання кисню
- •Лабораторна робота № 5 визначення твердості води
- •5.1. Визначення твердості води спиртово-мильним методом
- •5.2. Визначення загальної твердості комплексометричним методом
- •5.3. Визначення загальної карбонатної твердості
- •5.4. Визначення залишкової карбонатної твердості
- •Лабораторна робота № 6 визначення розчиненого кисню методом вінклера
- •Лабораторна робота № 7 визначення кислотності й лужності води
- •7.1. Визначення рН води
- •7.2. Визначення кислотності води
- •7.3. Визначення лужності
- •Лабораторна робота № 8 визначення сполук нітрогену — аміаку, нітритів і нітратів
- •8.1. Визначення аміаку
- •Напівкількісний метод
- •Кількісний фотоколориметричний метод
- •8.2. Визначення нітритів
- •Якісний метод з наближеною кількісною оцінкою
- •Кількісний фотометричний метод
- •8.3. Визначення нітратів
- •Лабораторна робота № 9 визначення активного хлору
- •Лабораторна робота № 10 дослідження антропогенної евтрофікації водойм
- •11.3. Функціональна схема аналізатора
- •11.4. Підготовка аналізатора до роботи
- •11.4.1. Техніка безпеки
- •11.4.2. Градуювання аналізатора
- •11.5. Вимірювання масової концентрації ртуті
- •12.3. Функціональна схема й принцип роботи аналізатора
- •12.4. Принцип дії аналізатора
- •12.4.1. Принцип дії каналу вимірювань масової концентрації розчиненого у воді кисню о2
- •12.4.2. Принцип дії каналу вимірювання рН
- •12.4.3. Принцип дії каналу вимірювання температури
- •12.5. Приготування аналізатора до вимірювань
- •12.5.1. Приготування чутливого елемента о2
- •12.5.2. Приготування електродної системи рН
- •12.6. Порядок проведення вимірювань
- •12.6.1. Техніка безпеки
- •12.6.2. Порядок проведення вимірювань
- •12.6.3. Відлік показників вимірювань
- •12.6.4. Графічний аналіз результатів вимірювань
- •Додаток
- •Бібліографічний список
8.2. Визначення нітритів
Нітрити визначають фотометричним методом із реактивом Грісса (суміш сульфанілової кислоти і α-нафтиламіну). Нітрити є нестійкими сполуками, тому їх або визначають одразу після відбору проб води, або консервують додаванням 1 мл концентрованої Н2SО4 або 2…4 мл хлороформу на 1 л проби, можна також охолоджувати пробу води до 3…4°С.
У кислому розчині нітрити взаємодіють з первинними амінами з утворенням солей діазонію. При подальшому їх сполученні з ароматичними сполуками, що містять амінні та гідроксогрупи, утворюється азобарвник, концентрацію якого визначають фотометричним методом.
Для визначення нітрит-іонів у водах запропоновано метод, який ґрунтується на діазотуванні сульфанілової кислоти наявними в пробах води нітритами і взаємодії утвореної солі діазонію з α-нафтиламіном, що приводить до утворення червоно-фіолетового барвника:
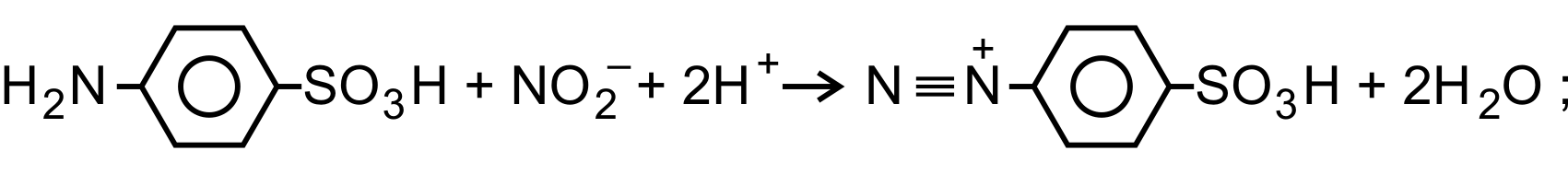
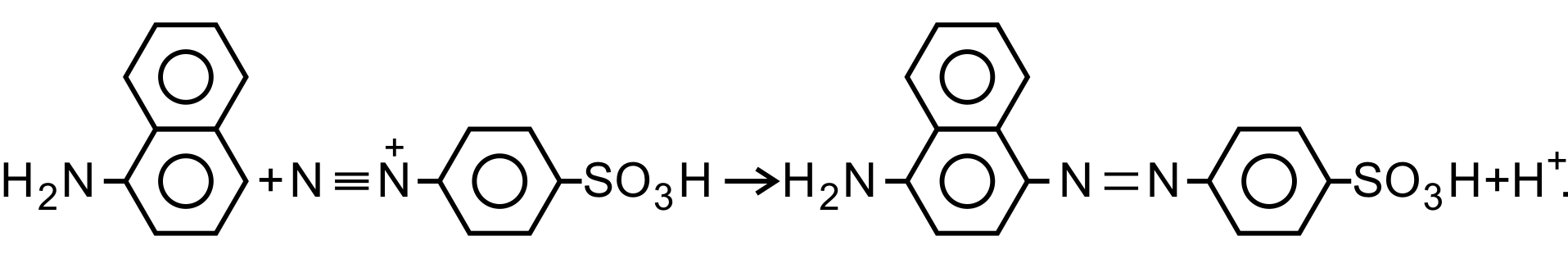
Чутливість описаного методу становить 0,002 мг/л NO2.
Визначенню нітритів перешкоджають завислі речовини та каламутність води, тому пробу перед аналізом фільтрують. За потреби проби прояснюють, додаючи гідроксид алюмінію. Для цього до 100 мл проби води додають 0,5 г активованого вугілля, 1 мл 2,5%-го розчину алюмокалієвих галунів КАl(SО4)2∙12Н2О і аміак до рН=5,8. Після збовтування тверда фаза випадає в осад і після повного прояснення розчину його фільтрують крізь фільтр «синя стрічка».
Для визначення відбирають частину фільтрату. Визначенню можуть перешкоджати сильні окисники та відновники. Ферум (III), меркурій (II), срібло, вісмут, плюмбум, золото та метаванадати в умовах визначення випадають в осад: йони купруму (II) знижують результати аналізу внаслідок каталітичної дії на розкладання діазотованої сульфанілової кислоти. Для забарвлених вод слід провести контрольний дослід, у якому до окремої проби води доливають тільки розчин сульфанілової кислоти. Отримане значення оптичної густини віднімають від оптичної густини досліджуваної проби.
Якісний метод з наближеною кількісною оцінкою
Обладнання і матеріали: пробірки; волюметричні піпетки; колби на 200 мл; водяна баня; реактив Грісса (0,5 г сульфанілової кислоти розчиняють при нагріванні в 150 мл 12%-го розчину ацетатної кислоти; окремо розчиняють при нагріванні 0,25 г α-нафтиламіну в 150 мл 12%-го розчину ацетатної кислоти; доводять до однакових об'ємів і змішують).
Хід роботи
Наливають у пробірку 10 мл води, яку аналізують. Додають 0,5 мл реактиву Грісса. Нагрівають суміш на водяній бані за температури 70°С упродовж п’яти хвилин. За даними табл. 8.2 визначають вміст у воді нітритів.
Таблиця 8.2. Визначення вмісту нітритів за кольором розчину
Забарвлення при розгляданні |
Масова концентрація нітритів, мг/л |
|
збоку |
зверху |
|
Немає Ледь помітне рожеве Дуже світле рожеве Блідо-рожеве Світло-рожеве Рожеве Яскраво-рожеве Червоне |
Немає Помітне рожеве Блідо-рожеве Світло-рожеве Рожеве Світло-червоне Червоне Яскраво-червоне |
0,001 0,002 0,004 0,020 0,030 0,040 0,070 0,400 |
