
- •Назначение и свойства промывочной жидкости для бурения осложненных зон.
- •Часть 1. Теоретические основы структурирования промывочных жидкостей
- •Структура промывочных жидкостей
- •Гидрофобные (коагуляционные) структуры
- •Толщина диффузионного слоя с увеличением концентрации ионов и их заряда снижается в соответствии с уравнением
- •Гидрофильные структуры
- •1.2.1 Структура воды
- •1.2.2 Поверхностная энергия твердых тел.
- •Поверхностные натяжения твердых тел
- •1.2.3. Взаимодействие воды с поверхностью твердых тел.
- •2. Структура глинистого раствора.
- •2.1 Структурообразователи
- •2.2 Механизм гидрофильного структурообразования глинистых растворов
- •2.3. Объёмная электрическая энергия промывочной жидкости
- •Среднее значение
- •2.4. Приборы для определения прочности структуры промывочных жидкостей
- •3. Структурирование глинистых растворов
- •3.1. Способы структурирования
- •3.2. Структурирование промывочной жидкости за счет повышения концентрации дисперсной фазы
- •3.3. Структурирование буровых растворов путем диспергирования твердой фазы
- •Влияние числа импульсов генератора на свойства растворов
- •3.4. Влияние температуры на прочность структуры глинистых растворов
- •4. Роль электролитов в структурировании промывочных жидкостей.
- •4.1. Общие сведения об электролитах, применяемых при бурении скважин.
- •Зависимость рН растворов солей от их концентрации
- •Теплота растворения электролитов
- •4.2. Электролиты в роли структурообразователя
- •4.3. Активация твердой фазы электролитами.
- •4.4. Дезактивация дисперсной фазы электролитами
- •5. Роль полимеров в структурировании промывочных жидкостей.
- •5.1. Полимеры – структурообразователи.
- •5.1.2. Синтетические структурообразователи
- •5.2. Активность полимеров
- •Расчетные значения энергии поляризации
- •5.3. Другие функции полимеров.
- •5.4. Активация полимеров.
- •5.5. Активация дисперсионной среды полимерных растворов.
- •5.6. Активация твердой фазы полимерами
- •5.7. Дезактивация дисперсной фазы гидрофобными веществами (пав, полимерами, маслами)
- •5.8 Стабильность (седиментационная и агрегативная устойчивость) раствора.
- •5.9 Стабилизация буровых растворов полимерами.
- •Устойчивость реагентов к агрессии солей
- •6. Деструктурирование промывочных жидкостей
- •6.1. Искусственное деструктурирование (разжижение) промывочных жидкостей путем снижения концентрации твердой фазы
- •6.2. Деструктурирование промывочных жидкостей путём активации твёрдой фазы. Понизители вязкости.
- •6.3. Деструктурирование минерализованных промывочных жидкостей
- •7. Структурная вязкость и коэффициент трения промывочных жидкостей
- •7.1.Вязкость ньютоновских жидкостей
- •Силу трения можно выразить формулой
- •Тогда касательное напряжение составит
- •Коэффициент кинематической вязкости будет
- •7.2. Вязкость структурированных жидкостей
- •7.2.1. Анализ существующих теорий
- •7.2.2. Влияние скорости течения, диаметра труб и концентрации твердой фазы на вязкость и коэффициент трения структурированных жидкостей
- •Влияние вязкости полимерного раствора и скорости
- •Зависимость показания раствора от концентрации кельцана
- •7.2.3. Влияние активации и дезактивации твёрдой фазы на коэффициент трения (вязкость) структурированных жидкостей.
- •7.3. Деструктурирование промывочных жидкостей при циркуляции.
- •7.3.1. Влияние длительности циркуляции структурированной жидкости на её вязкость
- •7.3.2. Влияние температуры на вязкость промывочных жидкостей.
- •7.4. Определение вязкости (касательных напряжений) промывочных жидкостей.
- •Значения вязкости различных буровых растворов
- •7.5. Влияние прочности структуры и вязкости промывочных жидкостей на процесс бурения
- •7.6. Тиксотропия промывочных жидкостей
- •Выводы:
- •7.7.Плотность промывочной жидкости.
- •Плотность аэрированной жидкости определяется по формуле
- •Часть II. Стабилизация неустойчивых стенок скважин. Задачами второй части исследований являются:
- •8.Общие сведения о структуре горных пород.
- •8.1 Химические связи в минералах
- •8.2. Межмолекулярные связи в горных породах.
- •8.3 Поверхностная энергия горных пород.
- •8.4 Устойчивость горных пород стенок скважин.
- •9. Промывочные жидкости для бурения уплотненных глин.
- •9.1. Уплотненные глины
- •Значения коэффициента для различной плотности глины
- •9.2. Осложнения при бурении уплотненных глин.
- •9.2.1. Механизм увлажнения и набухания глин.
- •9.2.2. Фильтрация воды в горные породы.
- •9.2.3. Разупрочнение уплотненных глин.
- •9.2.4. Диспергирование и размывание глин.
- •9.2.5. Влияние гидравлического давления на увлажнение глины.
- •9.2.6. Влияние горного давления на увлажнение глины.
- •9.3. Промывочные жидкости, применяемые для профилактики осложнений в уплотненных глинах
- •9.4. Основные направления выбора промывочной жидкости для бурения глинистых пород
- •9.5. Анализ эффективности применяющихся глинистых растворов для бурения уплотненных глин.
- •9.6. Анализ эффективности полимерных и полимерглинистых растворов.
- •9.7. Анализ эффективности ингибирующих растворов
- •10. Промывочные жидкости для бурения неуплотненных глин
- •10.1. Глинистые неуплотненные породы. Осложнения при их бурении.
- •10.2. Анализ влияния электролитов на увлажнение и прочность неуплотненной глины.
- •Зависимость пластической прочности образца глины от влажности к2
- •10.3. Влияние полимеров и полимерсолевых растворов на увлажнение и прочность неуплотненных глин.
- •10.4. Полимерполисолевые промывочные жидкости, для бурения неуплотненных глин (общие понятия).
- •10.5. Исследование крепящих свойств полимерполисолевых растворов.
- •10.5.1. Теоретические рассуждения.
- •10.5.2. Экспериментальные исследования.
- •11. Промывочные жидкости для бурения микротрещиноватых глинистых пород.
- •11.1. Микротрещиноватые глинистые породы. Осложнения при бурении
- •11.2. Влияние технологических параметров бурения на раскрытие трещин
- •11.3. Влияние гидродинамического давления на раскрытие трещин
- •11.4. Промывочные жидкости. Механизм их действия. Анализ эффективности.
- •12. Промывочные жидкости для бурения трещиноватых горных пород.
- •12.1. Трещиноватые горные породы
- •12.2. Поглощение промывочной жидкости в трещиноватых породах
- •12.3. Мероприятия по предупреждению поглощения промывочных жидкостей
- •12.4. Анализ эффективности различных наполнителей для кольматации трещин
- •Закупоривающая способность глинистых паст
- •Определение закупоривающей способности вол
- •Закупоривающая способность вус
- •Зависимость объема тампонажной смеси от состава ее компонентов
- •12.5. Применение пен при бурении трещиноватых пород
- •13. Промывочные жидкости для бурения соленосных отложений
- •13.1. Осложнения при бурении соленосных отложений
- •13.2. Растворение хемогенных горных пород Растворение горных пород в промывочной жидкости характерно для галлоидов и сульфатов, в меньшей степени карбонатов.
- •Измерение массы и длины образцов соли при растворении в воде
- •13.3. Размывание хемогенных пород
- •Зависимость скорости и константы растворения соли от скорости потока
- •13.4. Анализ влияния различных компонентов промывочной жидкости на растворяющую способность раствора
- •Скорость растворения галита в перемешиваемом растворе, м/с10-7 (емкость 10л)
- •Из анализа результатов следует:
- •13.5. Промывочные жидкости, применяемые для бурения соленосных отложений
- •Промывочные жидкости, применяемые в России при бурении соленосных отложений
- •Продолжение таблицы 13.7
- •13.6. Анализ качества применяющихся промывочных жидкостей для бурения соленосных отложений
- •Скорость растворения галита в циркулирующих растворах
- •13.7. Силикатные растворы
- •Состав и свойства сульфатосиликатных и карбонатосиликатных растворов
- •13.8. Лигниноглинистые растворы
- •Заключение
- •Библиографический список
- •3. Структурирование глинистых растворов 42
- •4. Роль электролитов в структурировании промывочных жидкостей. 55
- •5. Роль полимеров в структурировании промывочных жидкостей. 78
- •6. Деструктурирование промывочных жидкостей 116
- •7. Структурная вязкость и коэффициент трения промывочных жидкостей 131
- •9. Промывочные жидкости для бурения 188
- •10. Промывочные жидкости для бурения неуплотненных глин 222
- •11. Промывочные жидкости для бурения микротрещиноватых глинистых пород. 264
- •12. Промывочные жидкости для бурения трещиноватых горных пород. 279
- •13. Промывочные жидкости для бурения соленосных отложений 304
Гидрофильные структуры
Классическая теория ДЛФО является “первым приближением” [2], она рассчитана для типично гидрофобных дисперсных систем с водной дисперсионной средой, устойчивость которой обеспечивается только электрическим фактором отталкивания и межмолекулярными силами притяжения частиц.
В теории авторы не учитывают существования гидратных слоев, характерных для гидрофильной твердой фазы, в том числе частиц дисперсной фазы всех промывочных жидкостей.
Гидрофильными структурами (гидрогелями) назовем структуры, состоящие преимущественно из соорентированных под воздействием гидрофильных частиц твердой фазы дисперсной системы молекул воды.
Теория гидрофильного структурообразования отсутствует, поэтому процесс гидрофильного структурообразования рассмотрим поподробнее, начнем со структуры воды.
1.2.1 Структура воды
Вода, как известно [7]. Это природное неорганическое соединение, имеющее молекулярное строение, близкое соединениям водорода с галогенами: HI, НСl, HBr, соединениям водорода c серой H2S, селеном H2Se, теллуром Н2Те, азотом NH3. углеродом СН4 и т.д. Однако в отличие от воды все перечисленные соединения в атмосферных условиях являются газами, хотя молекулярный вес большинства из них превышает молекулярный вес воды. Вода же является жидкостью. Такая аномалия объясняется наличием связей между молекулами, обусловленных специфическим строением молекул воды.
Молекула воды, состоит из атома кислорода и двух атомов водорода. Атом кислорода на втором энергетическом уровне имеет два подуровня: 2S (орбиталь с двумя электронами 2 S2) и 2Р (с четырьмя электронами: орбиталъ с двумя электронами 2Р2 и два неспаренных электрона).
2S
2P
2S2
2P2
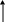
Н Н
Рис.1.1. Схема строения молекулы воды
Совместно с электронами двух атомов водорода Н неспаренные электроны кислорода образуют спаренные орбитали (рис. 1.1). Таким образом, образуется ковалентная связь между атомом кислорода и двумя атомами водорода. Длина этой связи 0,96 А.
Энергия связи Н-ОН составляет 493 кДж/молъ.
O М
М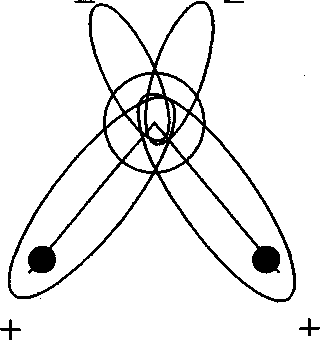
H
H
O
H
H
Поскольку электроотрицательность атомов водорода и кислорода значительно отличаются, то, как было отмечено выше, ионное облако (спаренная орбиталь) смещается в сторону более электроотрицательного атома (атома кислорода), молекула воды поляризуется: на атоме кислорода (в вершинах орбиталей с неподеленными электронными парами) возникает отрицательный заряд, а на атомах водорода - положительный заряд. За счет разноименности зарядов вершин, образованных таким образом молекул (диполей) воды возникает их взаимное притяжение по вершинам тетраэдров в направлении О-Н, что и обусловливает прочность связи молекул воды.
Энергия межмолекулярного взаимодействия молекул воды складывается из всех трех видов ван-дер-ваальсового взаимодействия (ориентационного, индукционного и дисперсного) и энергии водородной связи.
Ориентационное взаимодействие (эффект Кезома). Молекулы воды в объеме стремятся ориентироваться так, чтобы энергия системы была минимальной. В одном слое молекулы-диполи устанавливаются в хвост друг другу (т.е. положительно заряженная часть молекулы направлена в сторону отрицательно заряженной части) в другом слое, в обратную сторону [33] таким образом, чтобы под положительно заряженной частью молекулы первого слоя располагалась отрицательно заряженная часть второго слоя (рис. 1.3)

Рис. 1.3. Схема ориентирования молекул воды
Энергию ориентационного взаимодействия можно представить как сумму кулоновского притяжения и отталкивания зарядов полюсов диполей. Расчет взаимодействия двух одинаковых полярных молекул (с дипольным моментом ) приводит к формуле:
Uop = -22 / S3,
где S - расстояние между центрами диполей
Такая энергия ориентационного взаимодействия возможна в том случае, когда положение молекул фиксировано (в кристаллах льда в контакте с твердым телом), когда тепловое движение не расстраивает ориентацию молекул, т.е. при Uop>>RT. В жидкой воде тепловое движение приводит к всевозможным ориентациям молекул, что способствует резкому снижению энергии ориентационного взаимодействия. Для двух взаимодействующих молекул при комнатной температуре она составляет всего 190 10 -67 Дж/моль.
При температуре 0°С (лед) при фиксированном положении молекул прочность воды на растяжение равна 1 МПа (для сравнения: прочность гранита на растяжение 2,9 МПа), при температуре 100 °С (пар) связь между молекулами почти отсутствует. Молекулы воды ведут себя как молекулы газа.
Такая зависимость снижения молекулярных сил взаимодействия от температуры объясняется тем, что с повышением температуры повышается кинетическая энергия молекул воды (тепловая энергия в соответствии с законом сохранения энергии переходит в кинетическую энергию молекул).
Каждая молекула воды за счет повышения температуры (по данным Я.И. Франкеля и Д.К. Максвелла [5]) получает энергию равную
q 0 = RT (1.11)
где R - постоянная Больцмана, равная 1,38 10 -23 Дж/К; Т - температура воды по Кельвину.
Кинетическая энергия молекул, по мнению ряда исследователей [5] затрачивается на колебательные движения (осцилляции) и трансляции (броуновское движение).
Если
обозначить удельные затраты энергии
на перемещение молекул на единицу
расстояния dx
через
![]() ,
а расстояние между двумя точками
трансляции (амплитуду трансляции) через
,
а расстояние между двумя точками
трансляции (амплитуду трансляции) через
![]() ,
(1.12)
,
(1.12)
(здесь
![]() - скорость осцилляции), то общие затраты
энергии на перемещение
молекул воды составят:
- скорость осцилляции), то общие затраты
энергии на перемещение
молекул воды составят:
![]() ,
(1.13)
,
(1.13)
откуда после интегрирования получим
![]() ,
(1.14)
,
(1.14)
где С - постоянная интегрирования, Ек - кинетическая энергия активации.
Это значит, что кинетическая энергия молекулы будет накапливаться постепенно в течение времени. После того как величина этой энергии окажется больше некоторого критического значения, молекула переходит (транслирует) в новое положение. Энергию, которую необходимо затратить на ее трансляцию, называют энергией активации Ек.
Найдя по формуле постоянную интегрирования С при условии, что Е=0, t=t0, где t0 - период осцилляции, и решив уравнение относительно t, получим
![]() ,
(1.15)
,
(1.15)
т.е. период трансляции t зависит от периода осцилляции, энергии активации и температуры воды.
С увеличением температуры воды период осцилляции и энергия активации снижаются. В соответствии с данными Д. Эйзенберга и В. Кауцина [5] период осцилляции воды составляет:
°С |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
t010-12, с |
12,5 |
8,9 |
6,7 |
5,2 |
4 |
3,4 |
2,8 |
2,3 |
а энергия активации:
°С |
0 |
10 |
20 |
30 |
50 |
100 |
150 |
EkкДж/моль |
22 |
19 |
17 |
12 |
14,2 |
11,7 |
8,5 |
Расчеты показывают, что период трансляции молекул воды в жидком состоянии в миллионы раз меньше периода трансляций молекул льда. Высокая скорость и хаотическое направление трансляций молекул воды обуславливают слабые межмолекулярные связи воды. С учетом теплового движения энергия ориентационного взаимодействия будет
Uop = - (24 / 3r6)(1 / RT).
Следовательно, прочность межмолекулярных связей воды увеличивается с увеличением периода трансляций молекул и ориентировки молекул под воздействием электрического поля поверхности твердого тела или ионов. Доля ориентационного взаимодействия для воды составляет 75-80 % ван-дер-ваальсового взаимодействия.
Энергия индукционного взаимодействия для молекул воды может быть определена по формуле
Еинд = -22 / r6, (1.16)
где — поляризуемость.
Поляризуемость молекул воды в объеме под воздействием слабых диполей невелика, поэтому и энергия индукционного взаимодействия воды также невелика и составляет, по данным исследований [33] около 4 %.
Энергия дисперсионного взаимодействия для молекул воды определяется формулой
Едисп
=
![]() (1.17)
(1.17)
и составляет по расчетам Ф. Лондона 4710 -67 Дж/моль (здесь I — потенциал ионизации молекул).
Доля дисперсионного взаимодействия для воды несколько выше индукционной (около 20 %).
Водородная связь. Между молекулами воды помимо ван-дер-ваальсового взаимодействия существует еще специфическое взаимодействие, обусловленное способностью атома водорода какой-либо молекулы образовывать дополнительную связь с высокоэлектроотрицательными химическими элементами О, N, Cl, F, близкую к химической связи. Энергия водородной связи равна 29 кДж/моль, что в 5-6 раз выше энергии ван-дер-ваальсового взаимодействия, но в 15-20 раз меньше энергии химической связи.
Энергия водородной связи включает три слагаемых [33]: энергию кулоновского взаимодействия, энергию поляризации и переноса заряда, энергию отталкивания. На больших расстояниях преобладает кулоновская энергия притяжения, при уменьшении расстояния появляются поляризация и вслед за ней перенос заряда (донорно-акцепторный перенос), способствующий притяжению и, наконец, при малом расстоянии (доли нанометра) происходит отталкивание.
