- •Назначение и свойства промывочной жидкости для бурения осложненных зон.
- •Часть 1. Теоретические основы структурирования промывочных жидкостей
- •Структура промывочных жидкостей
- •Гидрофобные (коагуляционные) структуры
- •Толщина диффузионного слоя с увеличением концентрации ионов и их заряда снижается в соответствии с уравнением
- •Гидрофильные структуры
- •1.2.1 Структура воды
- •1.2.2 Поверхностная энергия твердых тел.
- •Поверхностные натяжения твердых тел
- •1.2.3. Взаимодействие воды с поверхностью твердых тел.
- •2. Структура глинистого раствора.
- •2.1 Структурообразователи
- •2.2 Механизм гидрофильного структурообразования глинистых растворов
- •2.3. Объёмная электрическая энергия промывочной жидкости
- •Среднее значение
- •2.4. Приборы для определения прочности структуры промывочных жидкостей
- •3. Структурирование глинистых растворов
- •3.1. Способы структурирования
- •3.2. Структурирование промывочной жидкости за счет повышения концентрации дисперсной фазы
- •3.3. Структурирование буровых растворов путем диспергирования твердой фазы
- •Влияние числа импульсов генератора на свойства растворов
- •3.4. Влияние температуры на прочность структуры глинистых растворов
- •4. Роль электролитов в структурировании промывочных жидкостей.
- •4.1. Общие сведения об электролитах, применяемых при бурении скважин.
- •Зависимость рН растворов солей от их концентрации
- •Теплота растворения электролитов
- •4.2. Электролиты в роли структурообразователя
- •4.3. Активация твердой фазы электролитами.
- •4.4. Дезактивация дисперсной фазы электролитами
- •5. Роль полимеров в структурировании промывочных жидкостей.
- •5.1. Полимеры – структурообразователи.
- •5.1.2. Синтетические структурообразователи
- •5.2. Активность полимеров
- •Расчетные значения энергии поляризации
- •5.3. Другие функции полимеров.
- •5.4. Активация полимеров.
- •5.5. Активация дисперсионной среды полимерных растворов.
- •5.6. Активация твердой фазы полимерами
- •5.7. Дезактивация дисперсной фазы гидрофобными веществами (пав, полимерами, маслами)
- •5.8 Стабильность (седиментационная и агрегативная устойчивость) раствора.
- •5.9 Стабилизация буровых растворов полимерами.
- •Устойчивость реагентов к агрессии солей
- •6. Деструктурирование промывочных жидкостей
- •6.1. Искусственное деструктурирование (разжижение) промывочных жидкостей путем снижения концентрации твердой фазы
- •6.2. Деструктурирование промывочных жидкостей путём активации твёрдой фазы. Понизители вязкости.
- •6.3. Деструктурирование минерализованных промывочных жидкостей
- •7. Структурная вязкость и коэффициент трения промывочных жидкостей
- •7.1.Вязкость ньютоновских жидкостей
- •Силу трения можно выразить формулой
- •Тогда касательное напряжение составит
- •Коэффициент кинематической вязкости будет
- •7.2. Вязкость структурированных жидкостей
- •7.2.1. Анализ существующих теорий
- •7.2.2. Влияние скорости течения, диаметра труб и концентрации твердой фазы на вязкость и коэффициент трения структурированных жидкостей
- •Влияние вязкости полимерного раствора и скорости
- •Зависимость показания раствора от концентрации кельцана
- •7.2.3. Влияние активации и дезактивации твёрдой фазы на коэффициент трения (вязкость) структурированных жидкостей.
- •7.3. Деструктурирование промывочных жидкостей при циркуляции.
- •7.3.1. Влияние длительности циркуляции структурированной жидкости на её вязкость
- •7.3.2. Влияние температуры на вязкость промывочных жидкостей.
- •7.4. Определение вязкости (касательных напряжений) промывочных жидкостей.
- •Значения вязкости различных буровых растворов
- •7.5. Влияние прочности структуры и вязкости промывочных жидкостей на процесс бурения
- •7.6. Тиксотропия промывочных жидкостей
- •Выводы:
- •7.7.Плотность промывочной жидкости.
- •Плотность аэрированной жидкости определяется по формуле
- •Часть II. Стабилизация неустойчивых стенок скважин. Задачами второй части исследований являются:
- •8.Общие сведения о структуре горных пород.
- •8.1 Химические связи в минералах
- •8.2. Межмолекулярные связи в горных породах.
- •8.3 Поверхностная энергия горных пород.
- •8.4 Устойчивость горных пород стенок скважин.
- •9. Промывочные жидкости для бурения уплотненных глин.
- •9.1. Уплотненные глины
- •Значения коэффициента для различной плотности глины
- •9.2. Осложнения при бурении уплотненных глин.
- •9.2.1. Механизм увлажнения и набухания глин.
- •9.2.2. Фильтрация воды в горные породы.
- •9.2.3. Разупрочнение уплотненных глин.
- •9.2.4. Диспергирование и размывание глин.
- •9.2.5. Влияние гидравлического давления на увлажнение глины.
- •9.2.6. Влияние горного давления на увлажнение глины.
- •9.3. Промывочные жидкости, применяемые для профилактики осложнений в уплотненных глинах
- •9.4. Основные направления выбора промывочной жидкости для бурения глинистых пород
- •9.5. Анализ эффективности применяющихся глинистых растворов для бурения уплотненных глин.
- •9.6. Анализ эффективности полимерных и полимерглинистых растворов.
- •9.7. Анализ эффективности ингибирующих растворов
- •10. Промывочные жидкости для бурения неуплотненных глин
- •10.1. Глинистые неуплотненные породы. Осложнения при их бурении.
- •10.2. Анализ влияния электролитов на увлажнение и прочность неуплотненной глины.
- •Зависимость пластической прочности образца глины от влажности к2
- •10.3. Влияние полимеров и полимерсолевых растворов на увлажнение и прочность неуплотненных глин.
- •10.4. Полимерполисолевые промывочные жидкости, для бурения неуплотненных глин (общие понятия).
- •10.5. Исследование крепящих свойств полимерполисолевых растворов.
- •10.5.1. Теоретические рассуждения.
- •10.5.2. Экспериментальные исследования.
- •11. Промывочные жидкости для бурения микротрещиноватых глинистых пород.
- •11.1. Микротрещиноватые глинистые породы. Осложнения при бурении
- •11.2. Влияние технологических параметров бурения на раскрытие трещин
- •11.3. Влияние гидродинамического давления на раскрытие трещин
- •11.4. Промывочные жидкости. Механизм их действия. Анализ эффективности.
- •12. Промывочные жидкости для бурения трещиноватых горных пород.
- •12.1. Трещиноватые горные породы
- •12.2. Поглощение промывочной жидкости в трещиноватых породах
- •12.3. Мероприятия по предупреждению поглощения промывочных жидкостей
- •12.4. Анализ эффективности различных наполнителей для кольматации трещин
- •Закупоривающая способность глинистых паст
- •Определение закупоривающей способности вол
- •Закупоривающая способность вус
- •Зависимость объема тампонажной смеси от состава ее компонентов
- •12.5. Применение пен при бурении трещиноватых пород
- •13. Промывочные жидкости для бурения соленосных отложений
- •13.1. Осложнения при бурении соленосных отложений
- •13.2. Растворение хемогенных горных пород Растворение горных пород в промывочной жидкости характерно для галлоидов и сульфатов, в меньшей степени карбонатов.
- •Измерение массы и длины образцов соли при растворении в воде
- •13.3. Размывание хемогенных пород
- •Зависимость скорости и константы растворения соли от скорости потока
- •13.4. Анализ влияния различных компонентов промывочной жидкости на растворяющую способность раствора
- •Скорость растворения галита в перемешиваемом растворе, м/с10-7 (емкость 10л)
- •Из анализа результатов следует:
- •13.5. Промывочные жидкости, применяемые для бурения соленосных отложений
- •Промывочные жидкости, применяемые в России при бурении соленосных отложений
- •Продолжение таблицы 13.7
- •13.6. Анализ качества применяющихся промывочных жидкостей для бурения соленосных отложений
- •Скорость растворения галита в циркулирующих растворах
- •13.7. Силикатные растворы
- •Состав и свойства сульфатосиликатных и карбонатосиликатных растворов
- •13.8. Лигниноглинистые растворы
- •Заключение
- •Библиографический список
- •3. Структурирование глинистых растворов 42
- •4. Роль электролитов в структурировании промывочных жидкостей. 55
- •5. Роль полимеров в структурировании промывочных жидкостей. 78
- •6. Деструктурирование промывочных жидкостей 116
- •7. Структурная вязкость и коэффициент трения промывочных жидкостей 131
- •9. Промывочные жидкости для бурения 188
- •10. Промывочные жидкости для бурения неуплотненных глин 222
- •11. Промывочные жидкости для бурения микротрещиноватых глинистых пород. 264
- •12. Промывочные жидкости для бурения трещиноватых горных пород. 279
- •13. Промывочные жидкости для бурения соленосных отложений 304
4.2. Электролиты в роли структурообразователя
При промывке скважины в соленосных горных породах глинистыми и полимерными растворами происходит их интенсивная коагуляция поэтому ведутся поиски по замене этих растворов растворами, устойчивыми к солевой агрессии. К таким растворам можно отнести растворы с конденсированной твердой фазой. Конденсированная твердая фаза должна быть:
гидрофильной,
обладать активными функциональными
группами: – ОН-;
– СО3-;![]() ;
SiO2-;
;
SiO2-;
агрегативно- и седиментационно устойчивой.
Для получения конденсированной твердой фазы используют легкорастворимые в воде соли, вступающие друг с другом или с водой в реакцию с получением нерастворимых или малорастворимых (но с гидрофильной поверхностью) соединений.
Так, в результате взаимодействия ионов магния растворенного в воде бишофита с гидроксильной группой ОН- каустической соды образуются кристаллики гидроксида магния с гидрофильной поверхностью:
MgCl2+NaOH=Mg(OH)2+Na++Cl-
Благодаря наличию полярных групп -ОН вокруг микрокриcталлов Mg(OH)2 в воде образуются сольватные слои, значительной величины, в результате чего раствор в спокойном состоянии превращается в гидрогель. Поэтому буровые растворы с конденсированной твердой фазой, содержащей гидроксильную группу, получили название гидрогелей (в данном случае гидрогель магния).
С целью получения твердой фазы о большой удельной поверхностью и большей агрегативной и седиментационной устойчивостью рост частиц твердой фазы ограничивают введением в раствор полимеров (чаще всего КМЦ). Адсорбируясь на микрокристаллах Mg(OH)2, КМЦ не только ограничивает рост кристалла, но и активирует поверхность твердой фазы.
Подобные гидрогели могут образовывать гидроксиды трех и четырехвалентных элементов: Al(OH)3; Si(ОН)4 и т.д. В отличие от двухвалентных металлов, которые образуют гидроксиды только в щелочной среде трех- и четырехвалентные элементы образуют гидроксиды даже в кислой среде. Так, например, гидроксид алюминия появляется уже при рН=5. При действии на кислые растворы солей алюминия щелочью из раствора выпадает студенистый осадок гидрогеля алюминия.
Кремниевые кислоты Н2О·SiO2, Si(OH)4, в растворе также образуют гидрогели.
При высушивании гидрогелей получают аэрогели: алюмогели, силикагели.
Предотвращая сращивание микрокристаллов с помощью полимеров, получают стойкие структурированные растворы.
Наряду с гидрогелями широкое распространение получают промывочные жидкости с конденсированной твердой фазой, образованной из двух взаимодействующих в растворе друг с другом солей:
Na2CO3+CaCl2=CaCO3+2Na++2Cl-
Na2SiO3+CaCl2=CaSiO3+2Na++2Cl- и т.д.
или двух солей и воды:
Al(SO4)3+3CaCl2+3H2O=3CaSO4+2Al(OH)3+3H++3Cl-
Полученные таким образом соли также имеют гидрофильные функциональные группы и способны образовывать гели, поэтому их называют солегелями и гидросолегелями.
С целью ограничения роста кристаллов и гидрофилизации твердой фазы так же, как и при получении гидрогелей, в раствор добавляют полимеры: КМЦ, гипан, крахмал. Тип солегелей определяется по наименованию аниона и катиона конденсированной соли (сульфатно-кальциевый солегель, силикатно-кальциевый солегель, алюмо-силикатный солегель) или по названию соли (например, гипсовый солегель).
При введении в раствор щелочных солей наряду с солями образуются гидроокислы поливалентных металлов. Такие растворы получили название гидросолегелей.
Наиболее широкое распространение в России получил разработанный O.K. Ангелопуло гидрогель магния. Им было установлено, что концентрированные и насыщенные растворы МgСl2, а также насыщенные растворы NaCI и КС1, содержащие 15-20 % MgCl2 после обработки 1,5-2,0% NaOH, через несколько часов интенсивного перемешивания превращаются в структурированную систему- гидрогель магния, которая даже без добавки полимеров сохраняет стабильность в течение нескольких месяцев. Тем не менее с целью получения раствора с малым СНС в процессе приготовления раствора, когда СНС достигнет 3-5 Па, гидрогель обрабатывают полимерами.
Известно, что конденсация (кристаллизация) соли быстрее начинается при наличии центров кристаллизации - мельчайших твердых частиц в растворе, поэтому для ускорения конденсации соединений в раствор добавляют так называемые активированные (NaOH) затравки кристаллизации: сконденсированный гидроксид магния, асбест, тонко-, диспергированный мел, глину, гидролизный лигнин, отходы бумажного, химического и металлургического производства (частично растворимые шламы, шлаки, золу, диспергированную известь и т.д.).
При получении солегелей для предотвращения конденсирования крупных кристаллов полимер (по гельтехнологии O.K. Ангелопуло) вводят в один из электролитов до смешивания с другим электролитом.
Вместо электролитов для получения гелей могут использоваться природные (асбест, торф) и искусственные полимеры. Так, при введении в раствор полимеров (КМЦ, ПАА) кислой асбестовой затравки (КАЗ) и небольшого количества щелочи получают буровой раствор под названием асбогель.
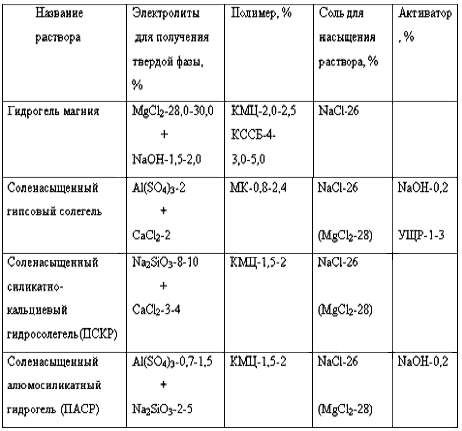
Гидрогели и солегели при бурении соленосных отложений для максимально возможного снижения растворяющей способности промывочной жидкости насыщают солями одновалентных или двухвалентных металлов в зависимости от требуемой соли. В табл.4.5 приводится состав некоторых гидро- и солегелей, применяемых для бурения соленосных отложений.
К недостаткам гидрогелей и солегелей следует отнести высокую материалоемкость дефицитных материалов, что значительно повышает себестоимость промывочных жидкостей.
Таблица 4.5
Состав гидрогелей и солегелей, применяемых в России для бурения соленосных отложений