
- •Практикум
- •1 Мета і задачі практичних занять
- •2 Вміст практичних занять
- •1.1 Розрахунок витратних коефіцієнтів
- •1.2 Приклади розв’язку задач
- •1.3 Задачі для самостійного розв’язку
- •2.1 Основи технологічних розрахунків – закони збереження і стехіометричних співвідношень
- •2.2 Приклади розв’язку задач
- •2.3 Задачі для самостійного розв’язку
- •Тема 3 Матеріальні розрахунки хіміко-технологічних процесів. Складання матеріальних балансів
- •3.2 Приклади розв’язку задач
- •3.3 Задачі для самостійного розв'язання
- •4.1 Теплові розрахунки хіміко-технологічних процесів. Складання теплових балансів
- •4.2 Приклади розв’язку задач
- •4.3 Задачі для самостійного розв'язання
- •Тема 5 Хімічна рівновага. Розрахунки рівноважних виходів
- •5.1. Розрахунок рівноважного складу суміші для хімічних процесів, які супроводжуються одною оборотною реакцією
- •5.1.1 Приклади розв’язку задач
- •5.1.2 Задача для самостійного розв'язання
- •5.2 Розрахунок рівноважного складу суміші для хімічних процесів, що супроводжуються декількома паралельними або послідовними оборотними процесами
- •5.3 Задачі для самостійного розв’язання
- •Тема 6 Кінетика хіміко-технологічних процесів. Розрахунок кінетичних параметрів
- •6.1 Розрахункові формули швидкості процесів.
- •6.2.Розрахунок кінетичних параметрів.
- •6.2.1.Методи визначення порядку реакцій.
- •6.2.1.1. Визначення порядку реакції по періоду напіврозпаду (тобто часу, протягом якого концентрація реагуючої речовини зменшиться удвічі).
- •6.2.1.2. Метод Оствальда-Нойеса.
- •6.2.1.3. Універсальний метод визначення порядків реакцій.
- •6.2.2. Константи швидкості, передекспоненціальний множник, енергія активації.
- •6.3 Задачі для самостійного вирішення
- •7.1 Розрахунок гетерогенно-каталітичних процесів
- •7.1 Основні формули для розрахунку гетерогенно-каталітичних реакцій
- •7.2 Розрахунки каталітичних процесів і реакторів.
- •7.3 Задачі для самостійного рішення
- •Тема 8 Електрохімічні процеси
- •8.2 Приклади розв’язку задач
7.2 Розрахунки каталітичних процесів і реакторів.
Задача №1
Визначити константи швидкостей реакцій:
СН3ОН + 0,5О2 → СН2О + Н2О
СН2О + 0,5О2 → СО + Н2О
по наступним вихідним даним: витрати газу Vг=10-2 м3/год; об’єм каталізатору Vкат=5·10-6 м3; початкова концентрація СН3ОН в метанольно-повітряній суміші С(СН3ОН), об’ємна частка – 6,5%; загальна ступінь перетворення СН3ОН: Х1=0,98; ступінь перетворення СН3ОН в СН2О: Х2=0,90. Реактор вважати без градієнтним, тобто прийняти, що ступінь перетворення і швидкість реакції постійні по всьому об’єму. Кисень повітря взятий в надлишку.
Розв’язання.
Необоротні реакції окислення метанолу і формальдегіду можна приймати псевдо мономолекулярними, тому що кисень повітря взятий в надлишку, тому
![]() ;
;
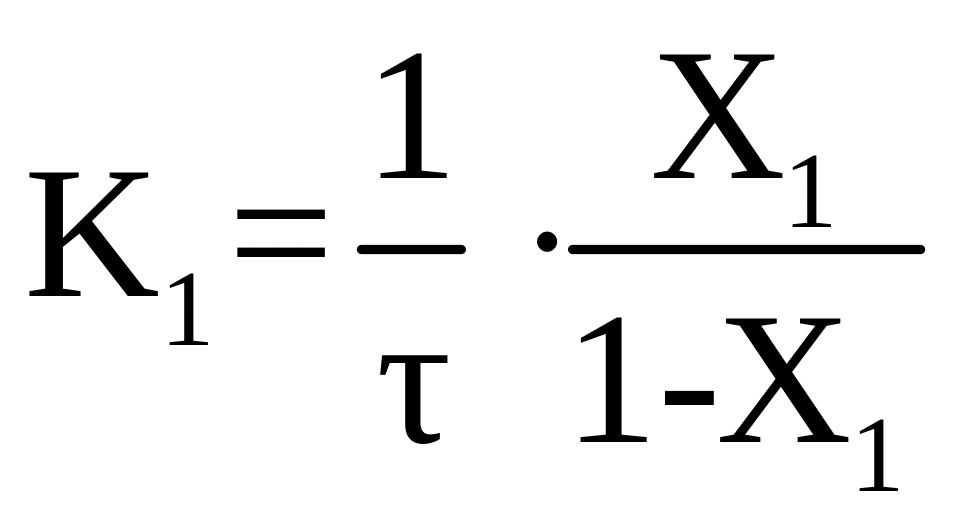 ;
;
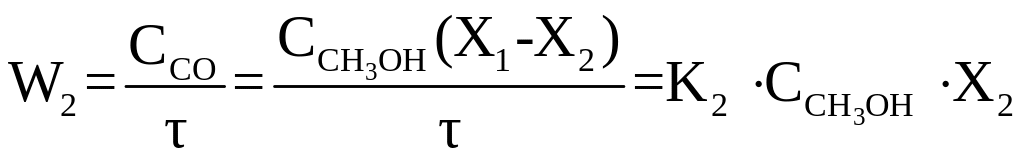 ;
;
 .
.
Фіктивний час контакту газу з каталізатором:

Визначаємо константи швидкостей К1 і К2:

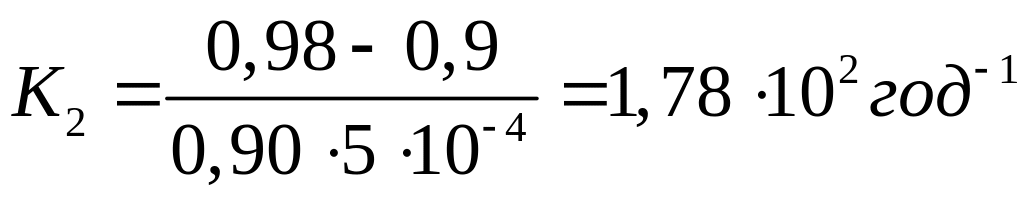
Задача № 2
Визначити діаметр реактора, об’єм каталізатору, висоту шару каталізатору (в потоці) при синтезі формаліну із метанолу в реакторі киплячого шару по вихідним даним: продуктивність по формаліну П=1900 кг/год, ступінь перетворення метанолу в формальдегід Х=0,90, початкова концентрація метанолу С(СН3ОН) в об’ємних частках – 6,5%; концентрація формальдегіду в об’ємних частках 37%, фіктивний час контакту газу з каталізатором τф=5·10-4 год; лінійна швидкість газу W=0,6 м/с.
Розв’язання.
Витрати метанолу при утворенні формальдегіду: кг/год:
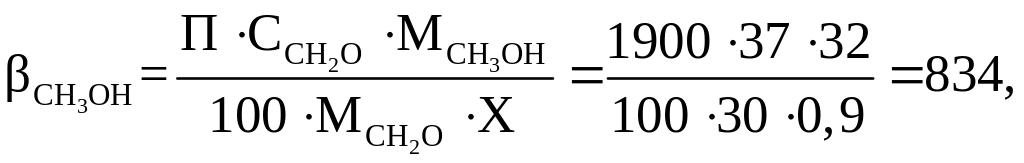
об’єм метанолу, нм3/год
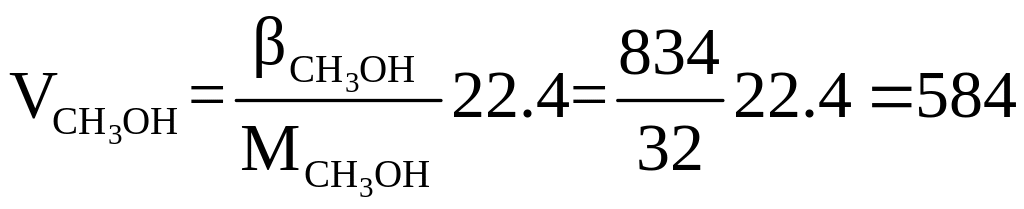
Витрати вихідної газової суміші, нм3/год
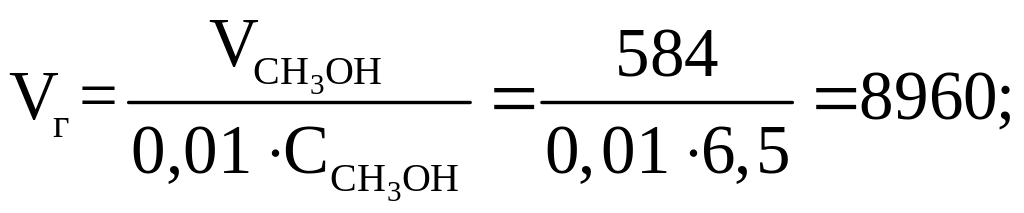
визначаємо діаметр реактора, м:
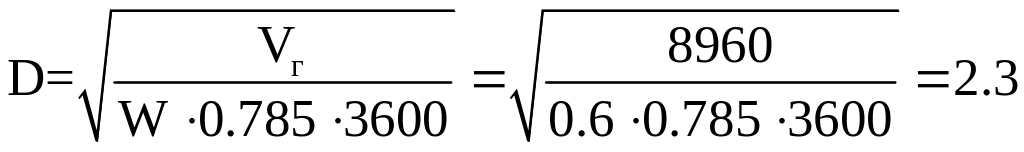
Площа перетину реактора, м2:
![]()
об’єм каталізатору, м3:
![]()
Висота шару каталізатору, м:
![]()
Задача № 3
Визначити об’єм каталізатора Vкат в колоні синтезу аміаку і фіктивний час контакту газу з каталізатором τф по наступним даним: продуктивність колони по аміаку П=96 т/добу; тиск Р=8·107 Па, температура Т=773 К; коефіцієнт стиснення азото-водневої суміші f=3,5; об’ємна швидкість газу Vоб=60000 год-1; ступінь перетворення Х=20%; витрати азото-водневої суміші VN2+H2=3000 нм3 на 1 кг NH3.
Розв’язання.
Годинна продуктивність колони. т/год:
![]() .
.
Об’єм циркулюючого газу, ни3/год:

Робочий об’єм азото-водневої суміші, м3/год

об’єм каталізатора м3/год:
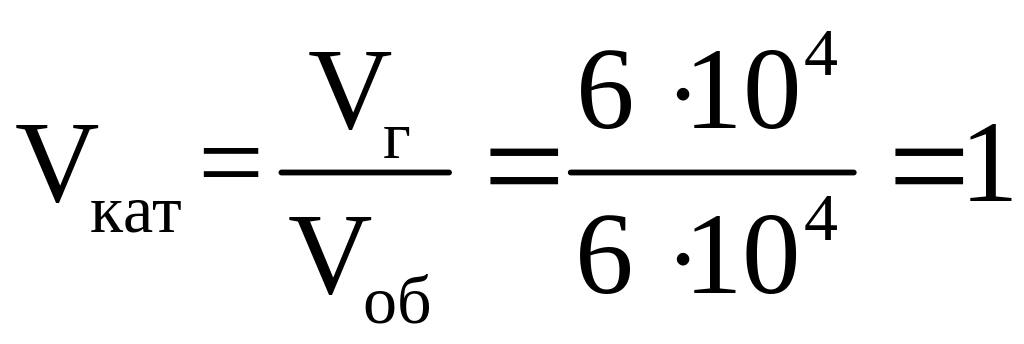
Фіктивний час контакту газу з каталізатором, с:
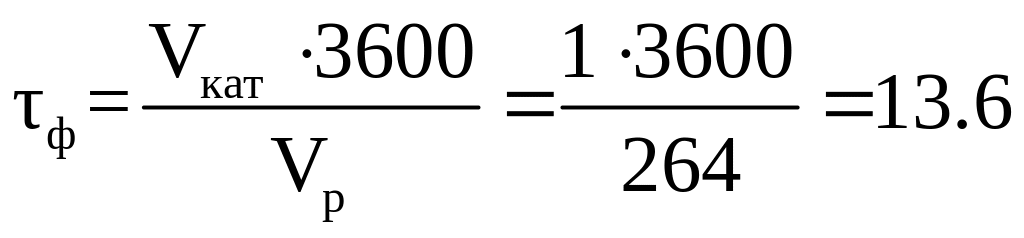 .
.
Задача № 4
Визначити гідравлічний опір фільтруючого шару каталізатору висотою Н=1,7 м в реакторі діаметром D=2,5 м. Витрати газу Vг=8500 м3/год, густина газу ρг=0,45 кг/м3, в’язкість газу μг=0,294·10-4 м-1. питома зовнішня поверхня зерен каталізатору S=415 м-1, порізність ε=0,43.
Розв’язання.
Площа перетину реактора, м2:
![]()
Фіктивна швидкість газу, м/с:
![]()
Визначаємо критерій Рейнольда:

Коефіцієнт опору при Re>50:
![]()
Гідравлічний опір шару каталізатору, Па:
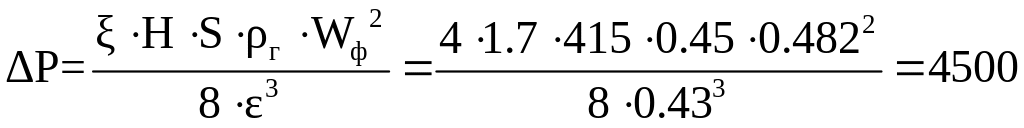
Задача № 5
Визначити найбільший розмір сферичних часток каталізатору в реакторі КШ. Вихідні дані: діаметр реактора D=0,61 м; фіктивна швидкість газуWф =0,117·103 м/с; густина частин каталізатору ρт=50000 кг/м3, в’язкість газу μг=0,256·10-3Па·с; густина газу на вході в реактор ρг.вх=14,45 кг/м3, густина газу на виході із реактора ρг.вих=16,52 кг/м3.
Розв’язання.
Розрахунок ведемо шляхом рішення наступних рівнянь:
![]()
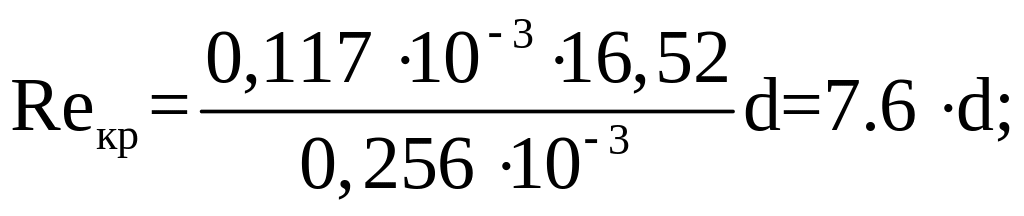
![]()
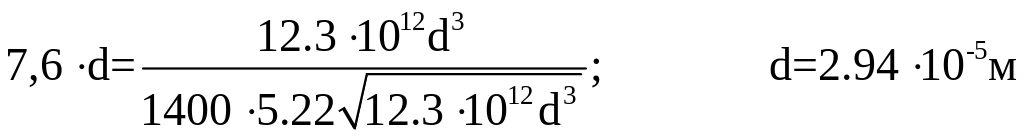 .
.
