
- •Практикум
- •1 Мета і задачі практичних занять
- •2 Вміст практичних занять
- •1.1 Розрахунок витратних коефіцієнтів
- •1.2 Приклади розв’язку задач
- •1.3 Задачі для самостійного розв’язку
- •2.1 Основи технологічних розрахунків – закони збереження і стехіометричних співвідношень
- •2.2 Приклади розв’язку задач
- •2.3 Задачі для самостійного розв’язку
- •Тема 3 Матеріальні розрахунки хіміко-технологічних процесів. Складання матеріальних балансів
- •3.2 Приклади розв’язку задач
- •3.3 Задачі для самостійного розв'язання
- •4.1 Теплові розрахунки хіміко-технологічних процесів. Складання теплових балансів
- •4.2 Приклади розв’язку задач
- •4.3 Задачі для самостійного розв'язання
- •Тема 5 Хімічна рівновага. Розрахунки рівноважних виходів
- •5.1. Розрахунок рівноважного складу суміші для хімічних процесів, які супроводжуються одною оборотною реакцією
- •5.1.1 Приклади розв’язку задач
- •5.1.2 Задача для самостійного розв'язання
- •5.2 Розрахунок рівноважного складу суміші для хімічних процесів, що супроводжуються декількома паралельними або послідовними оборотними процесами
- •5.3 Задачі для самостійного розв’язання
- •Тема 6 Кінетика хіміко-технологічних процесів. Розрахунок кінетичних параметрів
- •6.1 Розрахункові формули швидкості процесів.
- •6.2.Розрахунок кінетичних параметрів.
- •6.2.1.Методи визначення порядку реакцій.
- •6.2.1.1. Визначення порядку реакції по періоду напіврозпаду (тобто часу, протягом якого концентрація реагуючої речовини зменшиться удвічі).
- •6.2.1.2. Метод Оствальда-Нойеса.
- •6.2.1.3. Універсальний метод визначення порядків реакцій.
- •6.2.2. Константи швидкості, передекспоненціальний множник, енергія активації.
- •6.3 Задачі для самостійного вирішення
- •7.1 Розрахунок гетерогенно-каталітичних процесів
- •7.1 Основні формули для розрахунку гетерогенно-каталітичних реакцій
- •7.2 Розрахунки каталітичних процесів і реакторів.
- •7.3 Задачі для самостійного рішення
- •Тема 8 Електрохімічні процеси
- •8.2 Приклади розв’язку задач
7.1 Розрахунок гетерогенно-каталітичних процесів
Пришвидшуючи дія каталізаторів специфічна. Вона принципово відрізняється від дії інших факторів, які впливають на швидкість процесу – температури, тиску, вихідної концентрації реагентів, інтенсивності перемішування. Застосування каталізаторів – засіб підвищення швидкості хімічних реакцій, який не має обмежень і найбільш ефективний; в присутності каталізаторів можливе підвищення швидкості хімічних реакцій в мільйони разів.
В промисловості найбільш розповсюджений гетерогенний каталіз на твердих каталізаторів. Загальна швидкість гетерогенно-каталітичного процесу лімітується найбільш повільною стадією. В загальному випадку константа швидкості каталітичного процесу
К=f (К1, К2, Кпоб., Dвих, Dпрод.),
де К1, К2, Кпоб – константи швидкостей прямої, зворотної та побічної реакцій;
Dвих, Dпрод – коефіцієнти дифузії реагентів і продуктів реакції.
В кінетичній області К не залежить від D.
При розрахунках гетерогенно-каталітичних процесів використовуються такі їх технологічні параметри: ступінь перетворення – Х, активність каталізатора – А, константа швидкості процесу – К, час контакту реагенту з каталізатором – τ, об’ємна швидкість газу в шарі каталізатору – Vоб. Крім цих характеристик при розрахунках каталітичних реакторів визначають їх габаритні розміри, висоту шару каталізатору, гідравлічний опір фільтруючого або зваженого шару каталізатору, максимальні і мінімальні розміри часток каталізатору.
7.1 Основні формули для розрахунку гетерогенно-каталітичних реакцій
7.1.1 Активність каталізатору
 , (7.1)
, (7.1)
де ΔЕ=Е – Ек – пониження енергії активації каталітичної реакції в порівнянні з некаталітичною.
7.1.2 Фіктивний час контакту газу з каталізатором, с:
 ,
(7.2)
,
(7.2)
де Vкат – об’єм каталізатору, м3;
Vг – об’єм газової суміші, м3/год;
H – висота шару каталізатору, м;
W – лінійна швидкість газу, м/год.
7.1.3 Дійсний час контакту реагенту з каталізатором, с:
![]() , (7.3)
, (7.3)
де ε – порозність шару каталізатору,
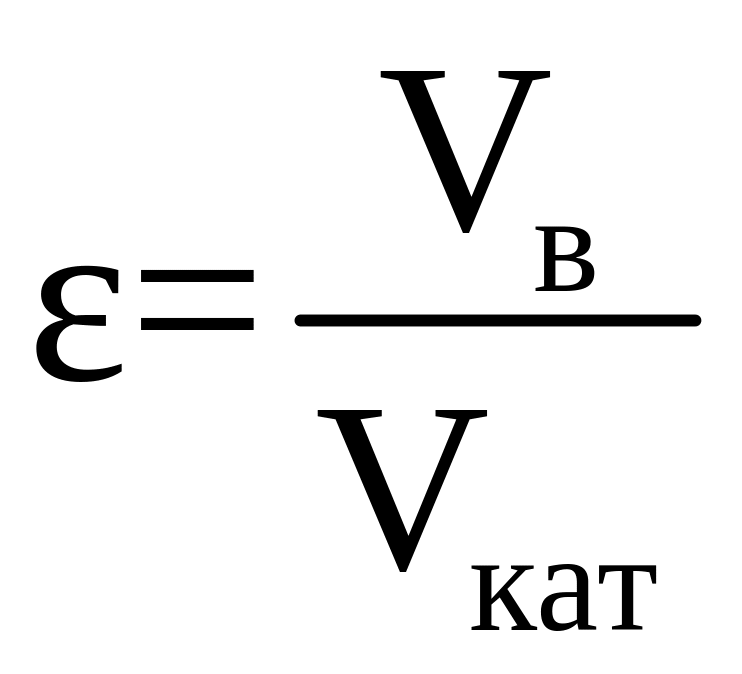 ,
(7.4)
,
(7.4)
де Vв – вільний об’єм шару, не зайнятий каталізатором, м3.
7.1.4 Об’ємна швидкість газу, год-1:
 ,
(7.5)
,
(7.5)
7.1.5 Необхідний для реалізації процесу об’єм каталізатору, м3:
![]() , (7.6)
, (7.6)
де С – коефіцієнт запасу, який вводиться із-за отруєння і механічних втрат каталізатору.
7.1.6 Діаметр зерна каталізатору d можна розрахувати із наступних залежностей:
![]() (7.7)
(7.7)
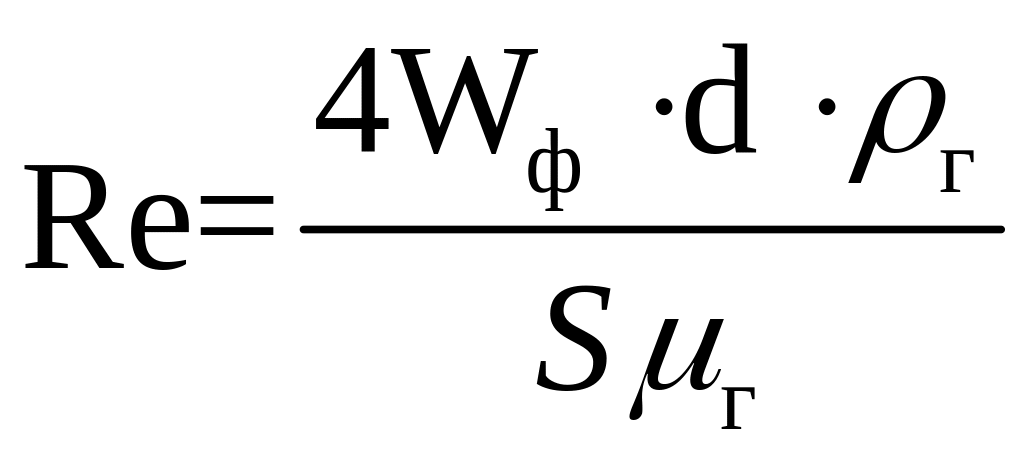 , (7.8)
, (7.8)
де
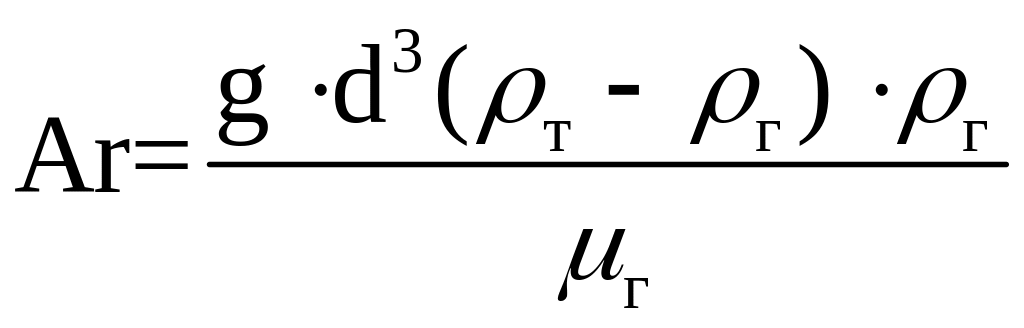 (7.9)
(7.9)
 , (7.10)
, (7.10)
де d – діаметр зерна каталізатору, м;
μг – кінетичний коефіцієнт в’язкості газу, Па·с;
ρт, ρг – густина каталізатору і газової суміші, кг/м3;
Wкр – критична швидкість зважування частинок каталізатору, м/с;
Ar, Re – критерій Архімеда і Рейнольда.
7.1.7 Кінцева температура реакційної суміші Ткін в реакторі з фільтруючим шаром каталізатору при адіабатичному режимі визначається за рівнянням:
 , (7.11)
, (7.11)
де Тн – початкова температура реакційної суміші, К;
qp – тепловий ефект реакції, кДж/моль;
Спр – концентрація продуктів в реакційній суміші, об’ємна частка, %;
![]() – середня
теплоємність реакційної суміші,
кДж/моль·град;
– середня
теплоємність реакційної суміші,
кДж/моль·град;
Х – ступінь перетворення, %.
7.1.8 Гідравлічний опір фільтруючого шару каталізатору:
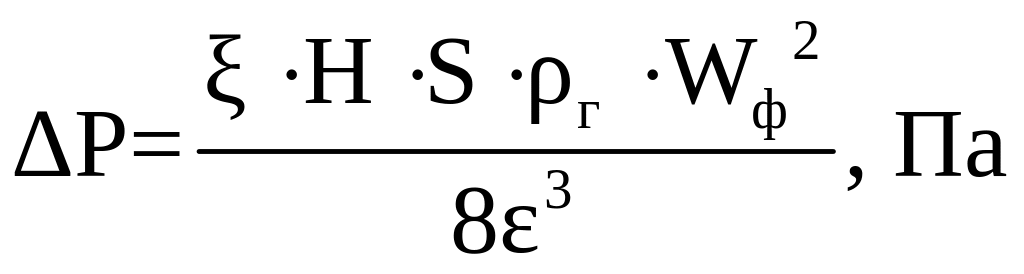 (7.12)
(7.12)
де
ξ – коефіцієнт опору каталізатору (при
Re<50
![]() ;
при
Re>50
;
при
Re>50
![]() );
);
Н – висота шару, м;
S – питома зовнішня поверхня зерна каталізатору, м-1;
Wф – фіктивна швидкість газу, м/с.
7.1.9 Розрахунок кінетики гетерогенного каталізу різноманітний в залежності від того, в якій області протікає процес. Розрізняють зовнішньо дифузійну область протікання процесу, кінетичну і внутрішньо дифузійну області. Якщо швидкість процесу лімітується швидкістю дифузії реагентів до поверхні каталізатору, то процес протікає у зовнішньо дифузійній області і швидкість процесу розраховується за рівнянням:
![]() (7.13)
(7.13)
де Кн – коефіцієнт масопередачі, м/год;
![]() -
концентрація основного реагенту А в
газі, моль/м3;
-
концентрація основного реагенту А в
газі, моль/м3;
![]() -
рівноважна концентрація реагенту А у
поверхні каталізатору, моль/м3.
-
рівноважна концентрація реагенту А у
поверхні каталізатору, моль/м3.
Швидкість процесу в кінетичній області:
![]() (7.14)
(7.14)
де К – константа швидкості процесу, м/год;
Vкат – об’єм каталізатору, м3;
S – питома поверхня каталізатору, м-1;
ΔС – рушійна сила процесу, моль/м3.
В кінетичній області протікання процесу лімітуючою стадією являється швидкість хімічної взаємодії.
Швидкість процесу у внутрішньо дифузійній області:
![]() (7.14)
(7.14)
де KS – константа швидкості реакції, віднесена до одиниці поверхні каталізатору. м/год;
![]() -
максимально можлива концентрація
реагенту А у поверхні каталізатора,
моль/м3;
-
максимально можлива концентрація
реагенту А у поверхні каталізатора,
моль/м3;
υ – поправочний множник, який характеризує ступінь використання внутрішньої поверхні пори:
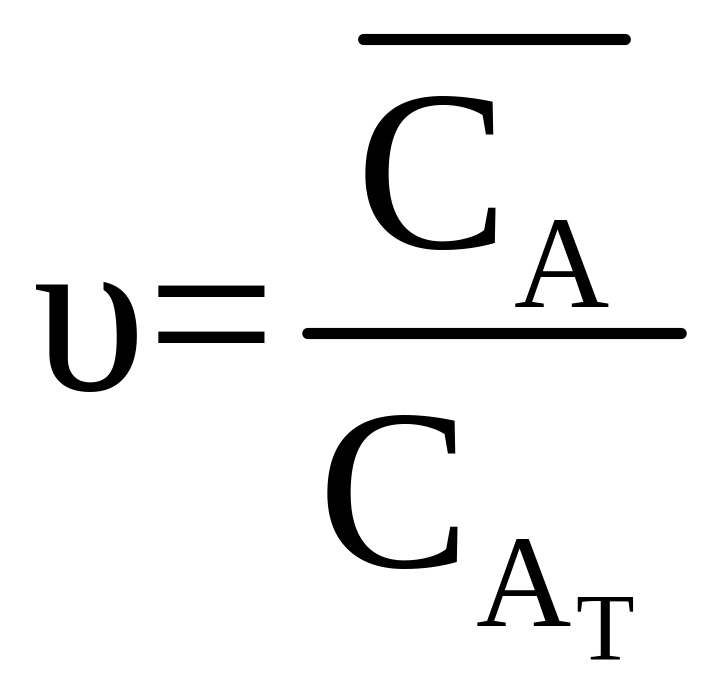 , (7.16)
, (7.16)
де
![]() - середня концентрація А в середині
пори.
- середня концентрація А в середині
пори.
Області протікання процесу визначають по перегину прямої:
 .
.
