
- •Практикум
- •1 Мета і задачі практичних занять
- •2 Вміст практичних занять
- •1.1 Розрахунок витратних коефіцієнтів
- •1.2 Приклади розв’язку задач
- •1.3 Задачі для самостійного розв’язку
- •2.1 Основи технологічних розрахунків – закони збереження і стехіометричних співвідношень
- •2.2 Приклади розв’язку задач
- •2.3 Задачі для самостійного розв’язку
- •Тема 3 Матеріальні розрахунки хіміко-технологічних процесів. Складання матеріальних балансів
- •3.2 Приклади розв’язку задач
- •3.3 Задачі для самостійного розв'язання
- •4.1 Теплові розрахунки хіміко-технологічних процесів. Складання теплових балансів
- •4.2 Приклади розв’язку задач
- •4.3 Задачі для самостійного розв'язання
- •Тема 5 Хімічна рівновага. Розрахунки рівноважних виходів
- •5.1. Розрахунок рівноважного складу суміші для хімічних процесів, які супроводжуються одною оборотною реакцією
- •5.1.1 Приклади розв’язку задач
- •5.1.2 Задача для самостійного розв'язання
- •5.2 Розрахунок рівноважного складу суміші для хімічних процесів, що супроводжуються декількома паралельними або послідовними оборотними процесами
- •5.3 Задачі для самостійного розв’язання
- •Тема 6 Кінетика хіміко-технологічних процесів. Розрахунок кінетичних параметрів
- •6.1 Розрахункові формули швидкості процесів.
- •6.2.Розрахунок кінетичних параметрів.
- •6.2.1.Методи визначення порядку реакцій.
- •6.2.1.1. Визначення порядку реакції по періоду напіврозпаду (тобто часу, протягом якого концентрація реагуючої речовини зменшиться удвічі).
- •6.2.1.2. Метод Оствальда-Нойеса.
- •6.2.1.3. Універсальний метод визначення порядків реакцій.
- •6.2.2. Константи швидкості, передекспоненціальний множник, енергія активації.
- •6.3 Задачі для самостійного вирішення
- •7.1 Розрахунок гетерогенно-каталітичних процесів
- •7.1 Основні формули для розрахунку гетерогенно-каталітичних реакцій
- •7.2 Розрахунки каталітичних процесів і реакторів.
- •7.3 Задачі для самостійного рішення
- •Тема 8 Електрохімічні процеси
- •8.2 Приклади розв’язку задач
5.1.2 Задача для самостійного розв'язання
Для
реакції, представленої стехіометричним
рівнянням
![]() скласти розрахункові рівняння і визначити
склад рівно-важної суміші. Тип реакції,
склад вихідної суміші, константа
рівноваги при заданій температурі і
тиску в системі рівноваги представлені
в таблиці 5.2.
скласти розрахункові рівняння і визначити
склад рівно-важної суміші. Тип реакції,
склад вихідної суміші, константа
рівноваги при заданій температурі і
тиску в системі рівноваги представлені
в таблиці 5.2.
Таблиця 5.2 - Дані для розрахунку складу рівноважної суміші
№ варі- анту |
Тип реакції |
Кр |
Р, МПа |
Склад вихідної суміші, моль |
||||||
|
|
|
|
інерти |
||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
||
1 |
|
4 |
3 |
5 |
- |
1 |
- |
3 |
||
2 |
|
1 |
15 |
2 |
3 |
- |
- |
1 |
||
3 |
|
0,5 |
5 |
- |
3 |
2 |
- |
2 |
||
4 |
|
12 |
10 |
1 |
3 |
- |
2 |
- |
||
5 |
|
0,7 |
5 |
- |
1 |
1 |
3 |
1 |
||
6 |
|
3 |
5 |
3 |
- |
1 |
- |
- |
||
7 |
|
8 |
1 |
1 |
3 |
- |
- |
4 |
||
8 |
|
0,04 |
5 |
1 |
3 |
- |
- |
- |
||
9 |
|
0,04 |
1 |
4 |
12 |
1 |
- |
3 |
||
10 |
|
0,05 |
30 |
4 |
12 |
1 |
- |
3 |
||
11 |
|
15 |
2 |
3 |
3 |
1 |
3 |
2 |
||
12 |
|
0,5 |
10 |
3 |
2 |
1 |
- |
- |
||
13 |
|
5 |
10 |
1 |
4 |
- |
1 |
- |
||
14 |
|
7 |
1 |
1 |
- |
1 |
- |
1 |
||
15 |
|
7 |
20 |
1 |
- |
1 |
- |
1 |
||
16 |
|
65 |
1 |
1 |
12 |
- |
- |
- |
||
17 |
|
95 |
2 |
1 |
- |
- |
4 |
- |
||
18 |
|
1 |
10 |
1 |
3 |
- |
3 |
- |
||
19 |
|
15 |
3 |
1 |
- |
1 |
- |
4 |
||
20 |
|
15 |
10 |
1 |
- |
1 |
- |
4 |
||
21 |
|
12 |
0,1 |
8 |
- |
3 |
1 |
1 |
||
22 |
|
5 |
1 |
5 |
- |
4 |
- |
- |
||
23 |
|
4 |
8 |
1 |
1 |
5 |
- |
3 |
||
24 |
|
18 |
15 |
4 |
2 |
1 |
2 |
2 |
||
25 |
|
25 |
6 |
3 |
1 |
- |
1 |
1 |
||
Задача №2.
Константа
рівноваги процесу конверсії монооксиду
вуглецю
![]() описується
рівнянням
описується
рівнянням
![]() .
Склад газу, що надходить на першу сходинку
конверсії, об’ємні частки, %:
.
Склад газу, що надходить на першу сходинку
конверсії, об’ємні частки, %:
![]() -55,0;
-55,0;
![]() -
3,6;
-
3,6;
![]() - 5,4;
- 5,4;
![]() -
25,6;
-
25,6;
![]() -
10,4. Температура газу після конверсії –
750 К; тиск – 2 МПа. Визначити склад
рівноважної суміші після конвектора
першої сходинки.
-
10,4. Температура газу після конверсії –
750 К; тиск – 2 МПа. Визначити склад
рівноважної суміші після конвектора
першої сходинки.
Розв’язок
Визначимо константу рівноваги реакції при заданій температурі 750 К:
![]()
![]()
З достатнім ступенем точності на основі закону Мендєлєєва – Клапейрона можна прирівняти числові значення об’ємних часток компонентів у відсотках до кількості їх молей в суміші.
Складемо баланс молей в стані рівноваги
Таблиця 5.3 - Дані для розрахунку рівноважного складу
Статті розрахунку |
Компоненти, моль |
||||
|
|
|
|
|
|
Склад вихідної суміші |
5,4 |
55,0 |
3,6 |
25,6 |
10,4 |
Утворилось продуктів |
- |
- |
z |
z |
- |
Витратилось речовин |
-z |
-z |
- |
- |
- |
Склад рівноважної суміші |
5,4 - z |
55,0 - z |
3,6 + z |
25,6 + z |
10,4 |
Сума молей в стані рівноваги |
5,4 – z + 55,0 – z + 3,6 + z + 25,6 + z + 10,4 = 100 |
||||
Складемо рівняння закону діючих мас в стані рівноваги:
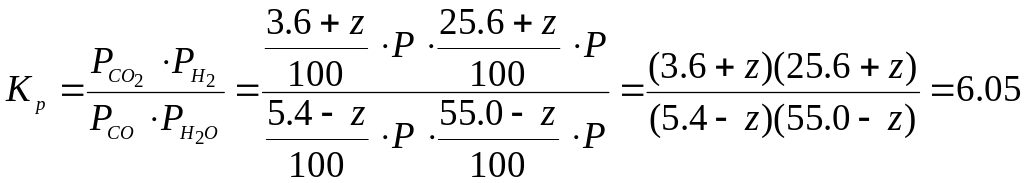
Із рівняння закону діючих мас видно, що тиск в даному випадку не впливає на стан рівноваги. Це узгоджується з принципом Ле-Шательє, згідно якому тиск не впливає на стан рівноваги процесів, що супроводжуються реакціями без зміни об’єму.
Розв’язавши рівняння закону діючих мас, отримаємо два позитивні значення z1=4,65; z2=74,1. На основі закону збереження маси вибираємо z1=4,64, так як в другому випадку витрати вихідних речовин перевищував би реальний вміст монооксиду вуглецю і парів води у вихідній суміші.
Визначимо
склад рівноважної суміші в молях, що
еквівалентно об’ємним часткам, %:
![]() =5,4
– 4,65 = 0,75 %;
=5,4
– 4,65 = 0,75 %;![]() =
55,0 –4,65 =50,35 %;
=
55,0 –4,65 =50,35 %;
![]() =
3,6 + 4,65 = 8,25 %;
=
3,6 + 4,65 = 8,25 %;![]() =25,6
+ 4,65 = 30,25 %. Всього: 0,75 + 50,35+ + 8,25 + 30,25 + 10,4 =
100 %.
=25,6
+ 4,65 = 30,25 %. Всього: 0,75 + 50,35+ + 8,25 + 30,25 + 10,4 =
100 %.
![]() =10,4.
=10,4.
