
- •Практикум
- •1 Мета і задачі практичних занять
- •2 Вміст практичних занять
- •1.1 Розрахунок витратних коефіцієнтів
- •1.2 Приклади розв’язку задач
- •1.3 Задачі для самостійного розв’язку
- •2.1 Основи технологічних розрахунків – закони збереження і стехіометричних співвідношень
- •2.2 Приклади розв’язку задач
- •2.3 Задачі для самостійного розв’язку
- •Тема 3 Матеріальні розрахунки хіміко-технологічних процесів. Складання матеріальних балансів
- •3.2 Приклади розв’язку задач
- •3.3 Задачі для самостійного розв'язання
- •4.1 Теплові розрахунки хіміко-технологічних процесів. Складання теплових балансів
- •4.2 Приклади розв’язку задач
- •4.3 Задачі для самостійного розв'язання
- •Тема 5 Хімічна рівновага. Розрахунки рівноважних виходів
- •5.1. Розрахунок рівноважного складу суміші для хімічних процесів, які супроводжуються одною оборотною реакцією
- •5.1.1 Приклади розв’язку задач
- •5.1.2 Задача для самостійного розв'язання
- •5.2 Розрахунок рівноважного складу суміші для хімічних процесів, що супроводжуються декількома паралельними або послідовними оборотними процесами
- •5.3 Задачі для самостійного розв’язання
- •Тема 6 Кінетика хіміко-технологічних процесів. Розрахунок кінетичних параметрів
- •6.1 Розрахункові формули швидкості процесів.
- •6.2.Розрахунок кінетичних параметрів.
- •6.2.1.Методи визначення порядку реакцій.
- •6.2.1.1. Визначення порядку реакції по періоду напіврозпаду (тобто часу, протягом якого концентрація реагуючої речовини зменшиться удвічі).
- •6.2.1.2. Метод Оствальда-Нойеса.
- •6.2.1.3. Універсальний метод визначення порядків реакцій.
- •6.2.2. Константи швидкості, передекспоненціальний множник, енергія активації.
- •6.3 Задачі для самостійного вирішення
- •7.1 Розрахунок гетерогенно-каталітичних процесів
- •7.1 Основні формули для розрахунку гетерогенно-каталітичних реакцій
- •7.2 Розрахунки каталітичних процесів і реакторів.
- •7.3 Задачі для самостійного рішення
- •Тема 8 Електрохімічні процеси
- •8.2 Приклади розв’язку задач
Тема 5 Хімічна рівновага. Розрахунки рівноважних виходів
Виробництво найважливіших багатотоннажних продуктів хімічної технології: аміаку і водню для його синтезу; оксиду сірки (VI) – сировини для отримання сірчаної кислоти; етанолу, метанолу, ацетилену – найважливіших напівпродуктів органічного синтезу, а також багатьох продуктів тонкого органічного синтезу ведеться з використанням оборотних хімічних реакцій.
Для практичного розрахунку складу рівноважної суміші необхідні наступні вихідні дані: відомості про реакції, що проходять в системі; числові значення констант рівноваги реакцій Кр при заданій температурі; склад вихідної реакційної суміші, загальний тиск, під яким знаходиться система.
Визначення складу рівноважної суміші зводиться до розв'язання рівняння закону діючих мас в стані рівноваги, представленого через мольні частки учасників реакції і загальний тиск системи, і визначенню рівноважних мольних часток. Мольні частки речовин можна легко перерахувати в будь-які традиційно прийняті концентрації.
5.1. Розрахунок рівноважного складу суміші для хімічних процесів, які супроводжуються одною оборотною реакцією
5.1.1 Приклади розв’язку задач
Задача № 1
Скласти розрахункове рівняння для визначення складу рівноважної суміші для процесу, який супроводжується єдиною оборотною реакцією
![]()
Числові значення константи рівноваги Кр при заданій температурі і тиску Р – відомі. Склад вихідної суміші заданий, моль: А = 3; В = 2; R = 1; інертні домішки – 1 моль.
Розв'язок
Константа рівноваги реакції Кр, виражена через парціальні рівноважні тиски (рівняння закону діючих мас), представлена рівнянням
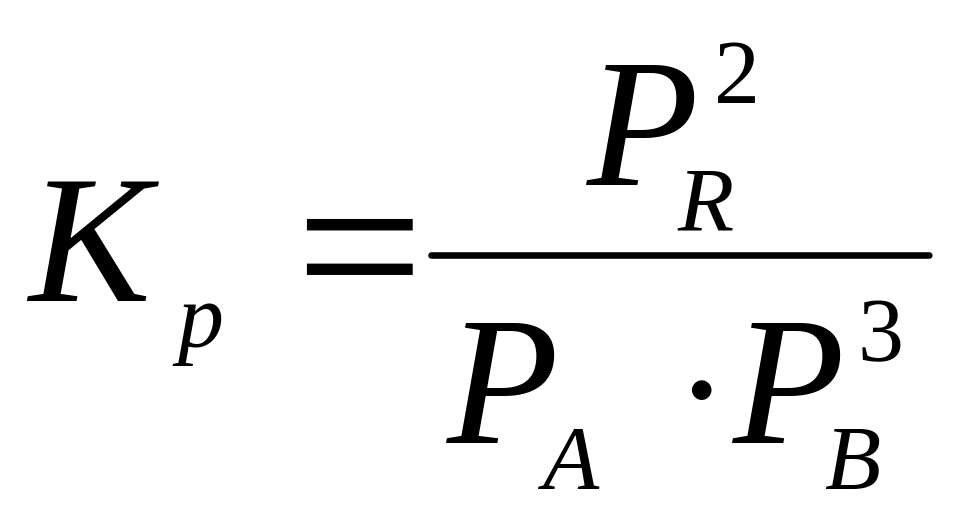 .
(5.1)
.
(5.1)
Парціальний тиск будь-якого компоненту можна визначити за законом Дальтона через загальний тиск системи і мольну частку
![]() .
(5.2)
.
(5.2)
Після підстановки виражених парціальних тисків в рівняння закону діючих мас отримаємо
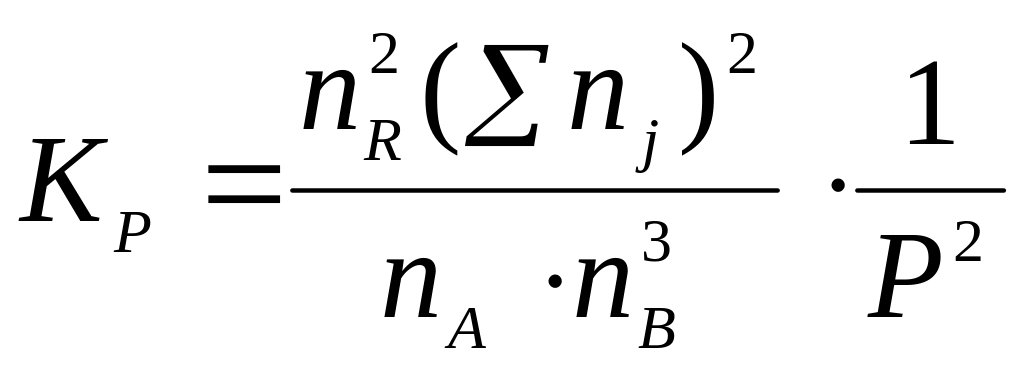 (5.3)
(5.3)
де
![]() - кількість молей сполук в стані рівноваги;
- кількість молей сполук в стані рівноваги;
![]() -
сума молей сполук, в тому числі інертних
домішок, в стані рівноваги;
-
сума молей сполук, в тому числі інертних
домішок, в стані рівноваги;
![]() -
загальний тиск системи.
-
загальний тиск системи.
Для визначення складу рівноважної суміші складемо таблицю балансу молей в стані рівноваги, де Z стехіометрично зв'язані кількості молей сполук, які прореагували і утворилися.
Таблиця 5.1 - Вихідні дані для розрахунку складу рівноважної суміші
Стаття розрахунку |
Компоненти, моль |
|||
|
|
|
інерти |
|
Склад вихідної суміші |
3 |
2 |
1 |
1 |
Утворилось продуктів |
- |
- |
Z |
- |
Витратилось вихідних речовин |
-0,5Z |
-3/2Z |
- |
- |
Склад рівноважної суміші |
3-0,5Z |
2-1,5Z |
1+Z |
1 |
Сума молей в стані рівноваги |
3-0,5Z +2-1,5Z +1+Z +1=7-Z |
|||
Підставивши рівноважні значення кількості молей в рівняння константи рівноваги
![]()
отримаємо алгебраїчне рівняння з одним невідомим Z, яке розв'язується за допомогою графічного або ітераційного методів обчислювальної математики.
Як видно із прикладу, метод придатний для розрахунку складу рівноважної суміші при будь-якому співвідношенні як вихідних речовин, так і продуктів, а також в стані розбавлення інертними домішками.
