
- •Тема: група речовин, що ізолюються з біологічного матеріалу полярними розчинниками План лекції
- •1. Загальна характеристика групи. Фізичні і хімічні властивості речовин.
- •2. Сучасні загальні і окремі методи ізолювання речовин групи з біологічного матеріалу. Поділ групи на підгрупи.
- •3. Фактори, що впливають на ефективність ізолювання речовин.
- •Фактори, що впливають на ступінь екстракції речовин з водних витяжок органічними розчинниками:
- •4. Методи очищення витяжок від домішок і концентрування виділених речовин.
- •1. Принципова схема аналізу «лікарських» отрут
- •«Лікарської» отрути в біологічному об'єкті
- •3. Хімічні методи дослідження «лікарських» отрут.
- •4. Фізико-хімічні методи ідентифікації препаратів.
- •Максимуми поглинання деяких хромофорів:
- •Вплив замісників на положення смуг поглинання монозаміщених похідних бензолу (в етанолі):
- •Хроматографічні методи:
- •5. Фармакологічні дослідження «лікарських» отрут.
- •6. Кількісне визначення «лікарських» отрут
- •План лекції
- •1. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних саліцилової кислоти
- •4. Виявлення саліцилової кислоти по уф-спектрам.
- •2. Застосування, токсикологічна характеристика, методи, виділення з біологічного матеріалу і методи аналізу похідних барбітурової кислоти
- •Загальна формула названих барбітуратів
- •Фізико-хімічні властивості.
- •1. Реакції забарвлення.
- •2. Мікрокристалоскопічні реакції.
- •3. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних піразолону
- •Спрямований хіміко-токсикологічний аналіз похідних піразолону.
- •1. Застосування і фізико-хімічні властивості алкалоїдів
- •Головними алкалоїдами даної групи є:
- •Головними алкалоїдами даної групи є:
- •2. Токсична дія алкалоїдів.
- •3. Поведінка в організмі і метаболізм.
- •4. Спрямований хіміко-токсикологічний аналіз алкалоїдів.
- •Апоморфін к·10 –7 Атропін к·10 –4,35
- •Кодеїн к·10 –6,05
- •2. Мікрокристалокопічні реакції.
- •2. Реакції забарвлення на алкалоїди.
- •Максимуми поглинання алкалоїдів
- •План лекції
- •1. Застосування, токсикологічна характернстика, методи виділення з біологічного матеріалу і методи аналізу похідних фенотіазіну.
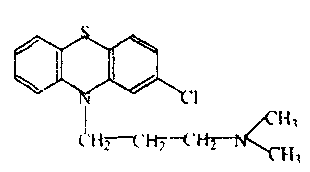
- •Аминазин
- •Дипразин
- •Тизерцин (левомепромазин)
- •Направлений хіміко-токсикологічний аналіз на похідні фенотіазину проводять відповідно до схеми:
- •План лекції
- •2. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних 1,4-бенздиазепіну.
- •3. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних п-амінобензойної кислоти
- •2. Мікрокристалоскопічні реакції - високочутливі, специфічні:
- •3. Реакції забарвлення:
Направлений хіміко-токсикологічний аналіз на похідні фенотіазину проводять відповідно до схеми:
Об'єкти дослідженя - мозок, печінка, нирки, шлунок з вмістом,
промивні води, легені, сеча.
Ізолювання препаратів проводиться за методами К.М.Саломатіна –
модифікованим методам Cтаса-Oтто (1) і Сшедзинського (2) з
врахуванням фізико-хімічних властивостей похідних фенотіазіну і стану біологічного матеріалу.
Методи характеризуються використанням амфіфильних розчинників – етанолу (1) і ацетонітрилу (2), що допускає наявність великої кількості співекстрактивних домішок. Для руйнування зв'язку отрута - білок (рН 2-3) застосовуються кислоти - оксалатна (1) і хлористоводнева (2). При виділенні у водну фазу основи фенотіазинів утворюють солі, добре розчинні у воді, хлороформі, але погано розчинні в ефірі, що використовується для очищення витяжки від домішок. Крім екстракції ефіром домішок очищення витяжок проводять осадження білків 96 % спиртом, фільтруванням (1), а також висолюванням домішок за допомогою розчину Nа2SO4(2).
Враховуючи, що фенотіазіни - сильні основи, їхнє виділення з водної в ефірну фазу проводиться при рН 13, для чого водні витяжки подлужнюють розчином NaOH.

Водна фаза
Ефірна фаза
Для додаткового очищення проводиться реекстракція препаратів 0,5 % розчином Н2SO4, в який переходять солі фенотіазинів і сульфатної кислоти, домішки залишаються в ефірній фазі.
ТСХ-скринінг проводиться в загальній системі розчинників - хлороформ диоксан - ацетон - 25 % розчин аміаку (45:47,5:5:2,5); сорбент - силікагель КСК; проявники - концентровані кислоти (Н2SO4, KNO3, HC1), а також розчини окислювачів НСlO4 і NaNO2; реактиви Марки, Манделіна.
Наявність плям рожевого і бузковго кольору в 3-їй зоні (Rf = 0,63-0,83) вказує на можливість присутності у витяжці похідних фенотіазіну.
Отруту із сорбенту силікагелю виділяють елюентом – метанол-диетиламін (9:1) з наступним проведенням підтверджуючого етапу в окремій системі розчинників - хлороформ - етанол (20:1) і циклогексан - ацетон (5:1); сорбент - основний окис алюмінію.
В якості «свідків» використовуються хлороформні розчини препаратів даної групи. Для проведення наступного етапу аналізу фенотіазіни елюють розчинниками метанол - диетиламін (9:1).
Очищення. Етап скринінга методом тонкошарової хроматографії дозволяє паралельно проводити якісне очищення від біогенних домішок, що локалізуються на хроматографічних пластинках в областях Rf <0,2 і Rf> 0,8.
Однак, в елюаті можлива присутність залишків домішок, що видаляються з використанням методів: екстракційного, гель-хроматофафії; електрофорезу; сполучення екстракційного і ТСХ-методів.
Підтверджуючі дослідження елюату включають найбільш чутливі хімічні і фізико-хімічні методи аналізу похідних фенотіазіну.
Хімічні реакції:
1. Реакції осадження з загальноалкалоїдними осадовими реактивами (пікринова кислота; сіль Рейнеке; реактиви Драгендорфа, Марме; Майєра, Зонненшейна й ін.).
Аморфні або кристалічні осади з нехарактерною формою частинок вказують на наявність гетероциклічного атома азоту в препаратах. Реакції високочутливі, не специфічні.
2. Реакції забарвлення засновані переважно на хімічних процесах окислювання, дегідрування, конденсації з альдегідами з використанням концентрованих кислот - Н2SO4, HNO3, НС1, НСlO4; реактиви Фреде; Манделіна; Марки; розчинів солей FeCl3, NaNO2.
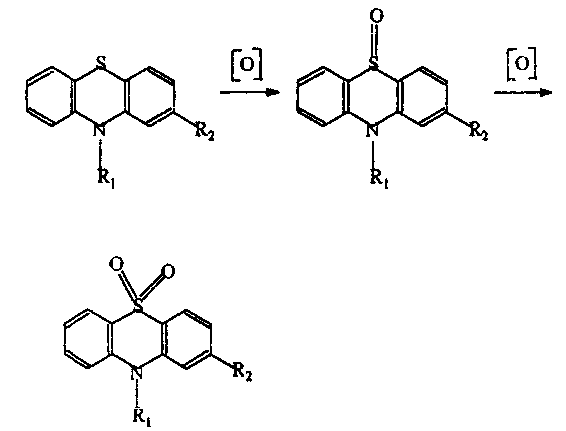
Продукти реакцій забарвлені в червоно-фіолетовий, синювато-червоний кольори. Реакції забарвлення чутливі, не специфічні.
Мікрокристалічні реакції - більшість фенотіазінів утворюють характерні кристалічні осади із сіллю Рейнеке, однак диференціація окремих представників цієї групи за формою кристалів важка
Фізико-хімічні методи аналізу
1 УФ-спектри похідних фенотіазину і їхніх продуктів окислення.
Абсорбція похідних фенотіазіну в УФ-області спектру характеризується наявністю 2 максимумів.
λmax 1.250-260 нм
2.300-315 нм
Порівняння Уф-спектрів солей похідних фенотіазіну зі спектрами їхніх основ показує, що вони практично ідентичні. Отже, їхній Уф-спектри відбивають тільки електронну структуру фенотіазинової частини молекули (аміππназин, дипразин). Виключення представляють ті похідні, що в 2-положенні містять радикали з вільними π-електронами(тизерцін).(
Сульфоксиди фенотіазінів мають на відміну від нативних сполук 4 максимуми в УФ-області: 230,265, 285 і 400 нм.
ІЧ-спектри основ похідних фенотіазіну (диск із бромідом калію) використовуються для підтвердження результатів дослідження в комплексі з хроматографічними і спектральними методами.
3. Поділ і ідентифікацію похідних фенотіазіну проводять ГРХ і ВЕРХ-методами по параметрах утримання (час й об’єми втримання).
Для кількісного аналізу похідних фенотіазіну при проведенні хіміко-токсикологічних досліджень застосовуються спектральні і хроматографічні методи.
Спектральні методи
• Фотометрія у видимій області спектру заснована на вимірі поглинання забарвлених продуктів реакції похідних фенотіазіну. Найбільше широко застосовується методика з концентрованою сульфатною кислотою. Heдостатками методики є:
• можливість обвуглювання соекстрактивних речовин, особливо при використанні, гнилостно-розкладеного біологічного матеріалу
• нестабільне забарвлення з невідтвореними значеннями оптичної густини
• Фотометрія в УФ-області спектру - високочутливий метод, що вимагає ретельного очищення витягів і використовується в сполученні з ТСХ-методом
Вимір оптичної густини проводяться при λmax 250 - 255 нм у 0,5 % розчині сульфатної кислоти.
• Екстракційна фотометрія, заснована на екстракції іонного асоціату фенотіазінів з кислотним індикатором (метиловим оранжевим) хлороформом, з наступним фотометричним забарвленням органічного шару
Метод чутливий, який не вимагає високого ступеня очищення від домішок. Приклад сполуки іонного асоціату аміназину і метилового оранжевого.
.
:
Хроматографічні методи:
• ГРХ і ВЕРХ методи (кількісна оцінка вмісту фенотіазінів проводитися по висоті, площі або вазі піку відповідної отрути).
• ТСХ-метод (кількісна оцінка вмісту фенотіазінів проводитися по інтенсивності забарвлення плями або його площі).
Хіміко-токсикологічний аналіз похідних фенотіазіну оцінюється по спільних результатах хімічних і фізико-хімічних методів.
Тема: ХІМІКО-ТОКСИКОЛОГІЧНИЙ АНАЛІЗ СИНТЕТИЧНИХ
«ЛІКАРСЬКИХ» ОТРУТ ОСНОВНОГО ХАРАКТЕРУ.
