- •Тема: група речовин, що ізолюються з біологічного матеріалу полярними розчинниками План лекції
- •1. Загальна характеристика групи. Фізичні і хімічні властивості речовин.
- •2. Сучасні загальні і окремі методи ізолювання речовин групи з біологічного матеріалу. Поділ групи на підгрупи.
- •3. Фактори, що впливають на ефективність ізолювання речовин.
- •Фактори, що впливають на ступінь екстракції речовин з водних витяжок органічними розчинниками:
- •4. Методи очищення витяжок від домішок і концентрування виділених речовин.
- •1. Принципова схема аналізу «лікарських» отрут
- •«Лікарської» отрути в біологічному об'єкті
- •3. Хімічні методи дослідження «лікарських» отрут.
- •4. Фізико-хімічні методи ідентифікації препаратів.
- •Максимуми поглинання деяких хромофорів:
- •Вплив замісників на положення смуг поглинання монозаміщених похідних бензолу (в етанолі):
- •Хроматографічні методи:
- •5. Фармакологічні дослідження «лікарських» отрут.
- •6. Кількісне визначення «лікарських» отрут
- •План лекції
- •1. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних саліцилової кислоти
- •4. Виявлення саліцилової кислоти по уф-спектрам.
- •2. Застосування, токсикологічна характеристика, методи, виділення з біологічного матеріалу і методи аналізу похідних барбітурової кислоти
- •Загальна формула названих барбітуратів
- •Фізико-хімічні властивості.
- •1. Реакції забарвлення.
- •2. Мікрокристалоскопічні реакції.
- •3. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних піразолону
- •Спрямований хіміко-токсикологічний аналіз похідних піразолону.
- •1. Застосування і фізико-хімічні властивості алкалоїдів
- •Головними алкалоїдами даної групи є:
- •Головними алкалоїдами даної групи є:
- •2. Токсична дія алкалоїдів.
- •3. Поведінка в організмі і метаболізм.
- •4. Спрямований хіміко-токсикологічний аналіз алкалоїдів.
- •Апоморфін к·10 –7 Атропін к·10 –4,35
- •Кодеїн к·10 –6,05
- •2. Мікрокристалокопічні реакції.
- •2. Реакції забарвлення на алкалоїди.
- •Максимуми поглинання алкалоїдів
- •План лекції
- •1. Застосування, токсикологічна характернстика, методи виділення з біологічного матеріалу і методи аналізу похідних фенотіазіну.
- •Аминазин
- •Дипразин
- •Тизерцин (левомепромазин)
- •Направлений хіміко-токсикологічний аналіз на похідні фенотіазину проводять відповідно до схеми:
- •План лекції
- •2. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних 1,4-бенздиазепіну.
- •3. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних п-амінобензойної кислоти
- •2. Мікрокристалоскопічні реакції - високочутливі, специфічні:
- •3. Реакції забарвлення:
1. Реакції забарвлення.
а) із солями кобальту в присутності аміаку. Спостерігається фіолетове забарвлення, зумовлене утворенням внутрішньокомплексною сполукою:
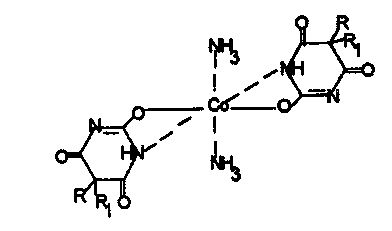
Реакція неспецифічна, так як її дають пурини, пірімідини, сульфаніламідні препарати. Виконанню цієї реакції заважає вода, що розкладає забарвлені сполуки. Реакція є високочутливою і носить попередній характер.
б) мурексидна реакція - при наявності барбітуратів спостерігається рожеве забарвлення. Реакція неспецифічна, тому що неї дають пурини, пірімідини; низкочутлива.
2. Мікрокристалоскопічні реакції.
Виділення кислотної форми барбітуратів - для барбітала характерні безбарвні прозорі прямокутні призми; для фенобарбіталу - сфероїди; для барбамілу - чи пластини призми, згруповані у виді сфероїдів; для етамінала натрію - призматичні кристали. Реакції специфічні, чутливі. Однак необхідно враховувати можливість появи поліморфних модифікацій, тому для підтвердження наявності індивідуальних барбітуратів проводяться окремі реакції з реактивами:
З хлорцинкйодом (барбаміл, барбітал, етамінал натрію – темно-червоні прямокутні пластинки);
Із сумішшю розчинів хлориду заліза і йодиду калію (барбаміл, фенобарбітал, етамінал натрію – оранжево-коричневі чи коричневі призми і їх зростки);
Реакція з дийодокупратом калію в розчині йоду (барбаміл, етамінал натрію - призми і їх зростки);
Підкислений спиртовий розчин йодиду калію (барбітал, етамінал натрію - призми і їх зростки);
Реакція із солями міді і піридином (барбітал – фіолетові кристали у формі зірочок, друз і прямокутників). Наявність осаду зумовлена утворенням внутрішньокомплексної сполуки.
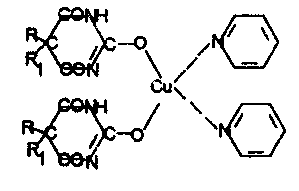
3. Фізико-хімічні методи ідентифікації: виявлення по УФ- і ІЧ-спектрам; методи ТСХ, ГРХ, ВЕРХ.
При хіміко-токсикологічному аналізі кількісне визначення барбітуратів проводиться фізико-хімічними методами:
Спектральними (УФ-спектрофотометрія, фотоколориметрія диференціальна спектрофотометрія, екстракційна фотометрія);
Хроматографічними (тонкошарова хроматографія, газрідинна і рідинна хроматографія).
Найбільш перспективним серед перерахованих методів є диференціальна спектрофотометрія заснована на іміно-імідольній таутомерії барбітуратів. Після виміру оптичної щільності при різних значеннях рН можливо нівелювати вплив домішок на отримані результати:
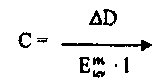
де С – концентрація речовини в %,
ΔD – різниця оптичних густин, вимірюваних:
• при рН 2 (домішки) і рН 10 (барбітурати в імідольній формі і
домішки);
• при рН 10 і рН 13 (барбітурати в диімідольній формі),
Е1сν1% - питомий показник поглинання,
l – товщина поглинаючого шару, у см.
У сполученні з попереднім хроматографічним очищенням (ТСХ метод) диференціальна спектрофотометрія забезпечує надійні і відтворені результати кількісного аналізу барбітуратів.
3. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних піразолону
У медичній практиці широко використовуються похідні піразолону як жарознижуючі, протизапальні і болезаспокійливі препарати.
|
Хімічна формула |
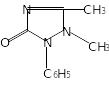
Амідопирин - 1-феніл-2,3-диметил-4- диметиламінопіразолон-5 |
|
Антипірин - 1-фенил-2,3-диметилпиразолон-5 |
|
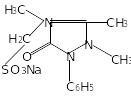
Анальгін - 1-феніл-2,3-диметил-4-метиламінопіразолон-5-метансульфонат натрію. |
|
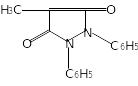
Бутадіон - 1,2-джифеніл-4-N-бутилпиразолидиндион-3,5. |
|
Фізико-хімічні властивості.
Амідопірин – 1-феніл-2,3-диметил-4-диметиламинопіразолон-5.
Білий кристалічний порошок слабогіркого смаку. Кристали препарату мають вид великих прямокутних пластин і уламків їх. Препарат повільно розчиняється у воді (1:20), легко в спирті (1:2), ефірі, дуже легко - у хлороформі. Температура плавлення – 107-109° С.
Антипірин – 1-феніл-2,3-диметилпіразолон-5.
Безбарвні кристали або білий кристалічний порошок без запаху, слабогіркого смаку. Кристали препарату мають вид великих плоских шестикутників з лінійчастими тріщинами. Дуже легко розчинний у воді (1:1), легко - у спирті. Температура плавлення – 110-113° С.
Анальгін - 1-феніл-2,3-диметил-4-метиламінопіразолон-5-N-метансульфонат натрію. Білий або білий з ледь помітним жовтуватим відтінком кристалічний порошок. В присутності вологи швидко розкладається. Кристали препарату мають вид подовжених призм, у полі зору зустрічаються прямокутні пластини. Анальгін легко розчинний у воді (1:1,5), важко - у спирті, не розчинний в ефірі.
Бутадіон – 1,2-дифеніл-4-N-бутилпіразолідиндіон-3,5. Білий або білий зі злегка жовтуватим відтінком порошок. Кристали препарату мають вид тонких подовжених призм, у поле зору видні окремі подовжені прямокутні пластини. Бутадіон мало розчинний у воді, важко - у спирті (1:28), розчинний в ефірі (1:15), хлороформі (1:1), у розчині їдкого натру. Температура плавлення 104-106° С.
Застосування.
Похідні піразолону застосовуються при невралгіях, ревматизмі, хореї, простудних захворюваннях і міозиті. Препарати зменшують проникність капілярів і перешкоджають розвитку запальних процесів.
Токсична дія.
Інтоксикація препаратами зумовлена передозуванням, підвищеною чутливістю до зазначених препаратів, їх неправильним збереженням. При тривалому прийомі препаратів виникає небезпека хронічного отруєння. Анальгін при повторному впливі на організм викликає ознаки анемії, робить нефротоксичну дію й у меншому ступені гeпатотропну дію. При тривалому застосуванні похідні піразолона сприяють гнобленню кровотворення (лейкопенія, агранулоцитоз), викликають збудження функцій ЦНС, зниження температури тіла, хвороби нирок, алергійні реакції (шкірна висипка, набряк слизових, описані окремі випадки анафілактичних реакцій).
Летальні дози похідних піразолону - 5-15 г.
Поводження в організмі.
Похідні піразолону при будь-якому шляху введення швидко всмоктуються в організмі і сліди їх виявляються в сечі вже через 10-20 хвилин після введення. Виділяються похідні піразолону в нативном виді й у виді метаболітів. Основні напрямки метаболізму:

4-аміноaнтипірин монометиламіноантипірин
Деметилювання до 4-аміноантипірину і монометиламіно-антипірину (амідопірин);
Гідроліз до монометиламіноантипірину (анальгін);
Ацетилювання до N-ацетил-4-аміноантипірин (амідопірин, анальгін).
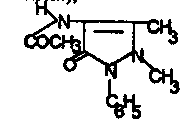
N-ацeтил-4-аміноaнтипірин
Окислювання до 4-гидроксиантипірину (анальгін, амідопирин, антипірин);
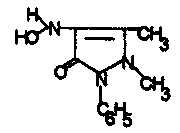
4-гидроксиантипірин
Коньюгація 4-гідроксиантипірину з глюкуроновой кислотою,
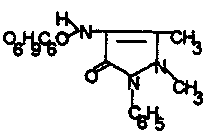
4-гідроксиантипіринглюкорунід
Гідроксилювання в пара положенні одного з двох фенільних радикалів бутадіону.

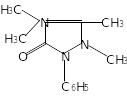 Назва
препарата
Назва
препарата