
- •1. Опішить сучасні уяви на будову і властивості металевих розплавів
- •2. Як тріщиностійкість пов’язана з діаграмою стану сплавів?
- •3.Як визначаються масові витрати сталі через стакан-дозатори?
- •4. Розкрийте сутність основних масообмінних процесів які відбуваються при вторинному окислені металу під час його розливання?
- •5. Охарактеризуйте складові коефіцієнта витрат металу із сталерозливного ковша
- •7. Як експериментально та аналітично визначається глибина рідкої лунки безперервної заготовки?
- •8. За якими умовами можливе концентраційне переохолодження рідкого розплаву?
- •10. Наведіть основні типи мблз, їх переваги та недоліки
- •12. Як пов’язана ліквація з градієнтом температур та інтервалом кристалізації?
- •11. Наведіть схему мблз, розкрити призначення основних конструктивних узлів
- •13. Як поверхневе тяжіння та в’язкість сталі впливають на кристалізацію сталі?
- •14. Які вимоги ставляться до конфігурації сталерозливних стаканів?
- •17. Розкрийте особливості утворення слідів гойдання на поверхні безперервно литої заготовки.
- •15. Зіставити хім.. Неоднорідність зливків спок, напів спок та кіп сталі (справочнік)
- •16. Розкрийте термодинамічні основи зародження і зростання кристалів.
- •19.Розкрити механізм формування позацентрової ліквації.
- •18. Охарактеризуйте склад і значення коеф. Твердіння зливків і безперервно литих заготовок
- •20. Розкрити механізм утворення вістової ліквації.
- •1. Характеристика топлива доменной плавки и основные требования к нему. Функции кокса в процессе выплавки чугуна
- •3. Заменители металлургического кокса, их характеристики, и эффективность применения в доменнной плавке?
- •2. Характеристика десульфурации чугуна в доменной печи, факторы определяющие ее эффективность.
- •4. Охарактеризовать технологические и экономические преимущества использования пут. Дайте оценку его эффективности по сравнению с природным газом?
- •6. Охарактеризовать поведение извести в доменной печи
- •5. Характеристика процесса коксования угольной шихты в коксовой камере
- •7. Какими условиями достигается необходимое распределение шихты по поперечному сечению доменной печи?
- •8. Приведите и охарактеризуйте виды чугунов, которые выплавляют в доменной печи?
- •11. Физико-химические процессы происходящие в фурменной зоне доменной печи?
- •9. Основные требования к качеству железных руд?
- •10. Охарактеризовать способы окускования железных руд, их сущность?
- •12. Описать назначение, сущность и технологическую схему производства агломерата?
- •14. Охарактеризуйте противоток материалов и газов в доменной печи, его рациональную организацию?
- •13. Охарактеризуйте качество и принципиальные расхождения между агломератом и окатышами как сырье для доменных печей?
- •15. Опишите назначение, сущность и технологическую схему производства окатышей?
- •16. Какое предназначение и сущность основных методов обогащения железных руд и их эффективность?
- •2 0. Проведите диаграмму равновесного состояния оксидов железа и газа н2. Приведите реакции восстановления оксидов железа газом н2?
- •17. Описать технологическую схему доменного производства?
- •19. Проведите диаграмму равновесного состояния оксидов железа и газа со. Приведите реакции восстановления оксидов железа газом со?
- •1. Проаналізуйте класифікацію електричних плавильних печей.
- •2.Проаналізуйте особливості та область застосування електричних печей опору.
- •3.Проаналізуйте принцип дії, типи та особливості застосування індукційних плавильних печей.
- •5. Проаналізуйте основні елементи конструкції і механізми дугової сталеплавильної печі.
- •7. Проаналізуйте способи завантаження шихти в дсп.
- •8. Проаналізуйте металевий лом як шихтовий матеріал для виплавки сталі в дсп.
- •9. Проаналізуйте шлакоутворювальні матеріали електроплавки.
- •14. Проаналізуйте особливості використання кисню під час виплавки сталі в дсп.
- •10. Проаналізуйте стадії плавлення шихти в дсп.
- •11. Проаналізуйте матеріали, що використовують для легування та розкиснення електросталі.
- •12.Проаналізуйте методи виплавки сталі в дугових печах.
- •13. Проаналізуйте особливості технології виробництва сталі з використанням надпотужних дсп.
- •15.Проаналізуйте завдання і особливості технології відновлювального періоду плавки в дсп.
- •16. Проаналізуйте особливості виплавки неіржавіючих сталей в дсп.
- •18. Проаналізуйте технологічні вимоги, що висувають до флюсів ешп.
- •20. Проаналізуйте переваги та недоліки дугових печей постійного струму.
- •17. Наведіть схему процесу ешп та проаналізуйте особливості технології плавки.
- •19. Наведіть схему процесу вдп та проаналізуйте особливості технології плавки.
- •1.Охарактеризуйте вплив температури на розчинність та межу розчинності кисню у рідкому залізі.
- •20.Опишить характер залежності активності та концентрації розчиненого у металі кисню від концентрації розкислювача.
- •2.Обгрунтуйте відсутність можливості протікання реакції окиснення вуглецю у однорідному обємі рідкого металу.
- •7.Поясніть, чому у періоді чистого кипіння у періоді рудного кипіння мартенівської ванни маса разової присадки залізної руди не повинна перевищувати 1-1,5% від маси металу.
- •4. Охарактеризуйте механізм реакцій які протікають при окислюванні металу при продуванні газоподібним киснем.
- •5. Охарактеризуйте основні закономірності змінювання хімічного складу металу при продуванні газоподібним киснем.
- •11. Поясніть, чим обумовлена суттєво різна ефективність дусульфурації металу в окислювальному та відновлювальному періодах плавки при виробництві сталі в дугових електросталеплавильних печах.
- •6.Охарактеризуйте механізм реакцій які протікають при окислюванні домішок металу киснем газової фази сталеплавильного агрегату.
- •8.Обґрунтуйте потребу у періоді «чистого» кипіння у перебігу доводки плавки в мартенівський печі.
- •9. Обґрунтуйте потребу у присутності певної кількості кремнію та марганцю у складі металевої шихти при виробництві сталі у кисневих конверторах.
- •12. Поясніть, чому при виробництві сталі у лд-конверторах в середині плавки може спостерігатися підвищення вмісту сірки у металі.
- •13. Поясніть залежність швидкості розчинення вапна в сталеплавильних шлаках від вмісту оксидів заліза та марганцю у їх складі.
- •10.Поясніть низьку ефективності десульфурації металу при виробництві сталі у кисневих конверторах і мартенівських печах, а також в окислювальному періоді плавки в дугових електросталеплавильних печах.
- •14. Назвіть способи інтенсифікації шлакоутворення при виробництві сталі в агрегатах з основною футерівкою.
- •16.Поясніть причини виникнення ліквації при кристалізації сталі. Охарактеризуйте вплив умов твердення на розвиток зональної ліквації в сталевих зливках та заготовках.
- •18. Можливі варіанти хімічного складу сталі наведені в таблиці.
- •19.Поясніть головні вимоги до організації процесів глибокого зневуглецювання високо хромистих розплавів.
- •3. Обгрунтуйте переваги та недоліки конверторного виробництва в порівнянні з іншими способами виплавки.
- •2. Як футерується кисневий конвертер?
- •4. Охарактеризуйте шихтові матеріали киснево-конверторної плавки. Переробний чавун та вимоги до нього.
- •5. Охарактеризуйте шихтові матеріали киснево-конверторної плавки. Металургійне вапно.
- •6. Які вимоги пред’являють до стального скрапу киснево-конверторної плавки?
- •7. Обґрунтуйте переваги та недоліки переробки низько-кремнієвих і низько марганцевих чугунів
- •8. Опишіть технологічні періоди к/к плавки та їх послідовність (с. 284)
- •9. Обгрунтуйте особливості шлакоутворення киснев-конверторної плавки
- •10. Якими способами прискорюють шлакоутворення конвертерної плавки?
- •19. Опишіть способи комбінованої продувки в кисневих конвертерах
- •20. Які технологічні особливості комбінованої продувки конвертерної плавки
- •13. Опишіть температурний(тепловой) режим конверторої плавки.
- •11. Охарактеризуйте періоди продувки металу в конверторі (с.286)
- •12. Обґрунтуйте механізм окислення домішок при взаємодії металу з газоподібним киснем?
- •14. Обґрунтуйте дуттєвий режим конверторної плавки
- •18. Опишіть конструкцію продувної фурми при подачі кисню знизу
- •15. Охарактеризуйте матеріальній и тепловий баланси конвертерної плавки
- •17. Як інтенсифікується шлакоутворення при донній продувці металу киснем?
- •16. Обґрунтуйте технологічні особливості продувки металу киснем знизу.
- •Задача 1
- •Решение
- •Задача 3
- •Решение
- •Задача 4
- •Задача 5
- •Задача 6
1.Охарактеризуйте вплив температури на розчинність та межу розчинності кисню у рідкому залізі.
Hастворение газообразного кислорода в жидком железе может быть описано уравнением реакции
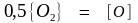 ,
(1.17)
,
(1.17)
Результаты экспериментальных исследований показывают, что стандартное значение изменения энергии Гиббса реакции (1.17) может быть получено из уравнения
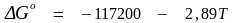 Дж/моль
. (1.21)
Дж/моль
. (1.21)
Из уравнения (1.21) формула для расчета константы равновесия реакции (1.17) может быть получена в виде
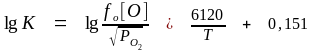 .
(1.22)
.
(1.22)
Из уравнения (1.21) видно, что растворение газообразного кислорода в жидком железе является сильной экзотермической реакцией. Следовательно, согласно уравнению изобары Вант Гоффа, с ростом температуры растворимость кислорода в железе при прочих равных условиях будет уменьшаться.
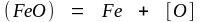 (1.16)
(1.16)
При высоких парциальных давлениях кислорода на поверхности жидкого железа появляется оксидная пленка. В этих условиях концентрация кислорода в металле определяется условиями протекания реакции (1.16) и зависит только от температуры. Константа равновесия реакции (1.16) может быть записана в виде
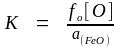 .
(1.23)
.
(1.23)
Если величина коэффициента активности растворенного в железе кислорода близка к единице, в условиях равновесия с чистым оксидом выражение (1.23) может быть приведено к виду
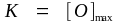 ,
(1.24)
,
(1.24)
где
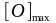 – концентрация кислорода в металле в
равновесии со шлаком из чистого FeO,
%.
– концентрация кислорода в металле в
равновесии со шлаком из чистого FeO,
%.
Результаты экспериментального исследования влияния температуры на растворимость кислорода в железе в равновесии со шлаком из чистого FeO показаны на рисунке 1.4. Анализируя эти данные, следует обратить внимание на то, что с ростом температуры предел растворимости кислорода в металле быстро увеличивается. Это свидетельствует о том, что растворение кислорода в металле из оксида железа в шлаке является сильной эндотермической реакцией.
20.Опишить характер залежності активності та концентрації розчиненого у металі кисню від концентрації розкислювача.
Если
условно обозначить элемент-раскислитель
через Me,
то реакцию осаждающего раскисления в
общей форме можно записать так:
![]()
Константа
равновесия этой реакции
![]()
откуда
![]()
Чем ниже активность продуктов раскисления, тем менее окислен металл после раскисления. При использовании комплексных раскислителей продукты реакции вступают между собой во взаимодействие, в результате чего величина их активности уменьшается.
2.Обгрунтуйте відсутність можливості протікання реакції окиснення вуглецю у однорідному обємі рідкого металу.
Реакция окисления растворенного в металле углерода включает большое количество звеньев, связанных с массопереносом взаимодействующих веществ в объеме металла, шлака и газовой фазы, а также переходом их через поверхности раздела фаз. В качестве примера можно перечислить основные звенья реакции для случая, когда кислород поступает в металл из газовой фазы сталеплавильного агрегата:
– диффузия
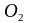 ,
,
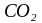 и
и
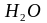 из объема окислительного газа через
пограничный слой к поверхности шлака;
из объема окислительного газа через
пограничный слой к поверхности шлака;
– адсорбция кислорода на поверхности шлака;
– химическая
реакция на поверхности раздела шлак-газ
с образованием ферритов (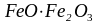 ,
,
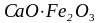 и др.) или ионов
и др.) или ионов
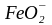 ;
;
– массоотдача ферритов (анионов) через пограничный слой в объем шлака;
– турбулентная диффузия ферритов (анионов) в объеме шлака к границе раздела шлак-металл;
– химическая реакция между ферритами и железом на границе раздела шлак-металл с образованием оксида двухвалентного железа;
– химический
акт распада
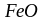 на атомы железа и кислорода и поступление
его в пограничный слой металла;
на атомы железа и кислорода и поступление
его в пограничный слой металла;
– массоотдача кислорода через пограничный слой в основную массу металла;
– турбулентная диффузия кислорода и углерода в объеме металла к возможному месту протекания реакции;
– массоотдача кислорода и углерода в пограничном слое металла у поверхности раздела металл-пузырьки газа;
– адсорбция кислорода и углерода на поверхности пузырей газа;
– химическая реакция между кислородом и углеродом на поверхности пузырей;
– десорбция оксида углерода с поверхности пузырей;
– массоотдача оксида углерода в объем газовой фазы.
По результатам лабораторных исследований был установлен также характер зависимости скорости окисления углерода от содержания его в металле. Показано, что в области высоких концентраций углерода скорость обезуглероживания определяется скоростью поступления кислорода в металл и не зависит от содержания углерода в расплаве. При концентрации углерода менее 0,2 – 0,3% дальнейшее обезуглероживание сопровождается уменьшением скорости окисления углерода при неизменной скорости поступления кислорода в расплав. Эту концентрацию углерода в научно-технической литературе принято называть критической.
Таким образом, в сталеплавильных ваннах при нормальной вязкости металла и шлака скорость окисления углерода при содержании его выше критической концентрации определяется скоростью поступления кислорода в металл и только при содержании углерода менее критических значений наблюдается зависимость скорости окисления углерода от содержания его в металле.
