
- •Химико-технологические системы
- •Содержание
- •Введение
- •1. Химико-технологические процессы и химико-технологические системы
- •1. Термины и определения
- •2. Технологические критерии эффективности химико-технологических систем
- •1. 2. 1. Степень превращения
- •1. 2. 2. Выход продукта
- •1. 2. 4. Производительность и интенсивность
- •1. 2. 5. Избирательность
- •1. 3. Структуры химико-технологических систем
- •1. 3. 1. Хтс с последовательной технологической связью
- •1. 3. 2. Параллельная технологическая связь
- •1. 3. 3. Последовательно-обводная технологическая связь (байпас)
- •1. 3. 4. Обратная (рециркуляционная) технологическая связь
- •1. 3. 5. Перекрестная технологическая связь
- •1. 4. Системный декомпозиционный анализ химико-технологических систем
- •4. 1. Молекулярно-кинетический уровень
- •1. 4. 2. Макрокинетический уровень
- •1. 4. 3. Аппаратный уровень
- •1. 4. 4. Уровень химико-технологической системы
- •1. 4. 4. 1. Синтез химико-технологической системы
- •1. 4. 4. 2. Анализ химико-технологической системы в целом
- •1. 4. 4. 3. Оптимизация химико-технологической системы
- •2. Химическая термодинамика
- •2. 1. Основные понятия и определения
- •2. 2. Первое начало термодинамики
- •2. 2. 1. Работа расширения идеального газа
- •2. 2. 2. Теплота процесса в различных условиях
- •2. 2. 3. Закон Гесса. Расчет тепловых эффектов химических реакций с использованием стандартных теплот образования и сгорания.
- •2. 2. 4. Зависимость тепловых эффектов химических реакций от температуры. Закон Кирхгофа
- •2. 3. Второе начало термодинамики
- •2. 3. 1. Термодинамически обратимые и необратимые процессы.
- •2. 3. 2. Математическое выражение второго начала термодинамики. Энтропия.
- •2. 3. 2. 1. Энтропия и термодинамическая вероятность
- •2. 3. 2. 2. Изменение энтропии как критерий направления процессов.
- •2. 3. 2. 3. Изменение энтропии при нагревании
- •2. 3. 2. 4. Изменение энтропии при фазовых превращениях
- •2. 3. 2. 5. Расчет абсолютной энтропии вещества
- •2. 3. 2. 6. Изменение энтропии при химическом превращении
- •2. 3. 3. Применение второго начала термодинамики к химическим процессам.
- •2. 3. 3. 1. Термодинамические потенциалы
- •2. 3. 3. 2. Уравнение Гиббса-Гельмгольца
- •2. 3. 3. 3. Критерии направления процессов в закрытых системах
- •2. 3. 4. Химический потенциал идеального и реального газа. Термодинамическая активность.
- •2. 3. 5. Уравнение изотермы химической реакции
- •3. Химическое равновесие
- •3. 1. Константы равновесия
- •3. 2. Расчет равновесного состава и равновесного выхода продуктов химической реакции
- •3. 3. Влияние температуры и давления на равновесный выход продуктов реакции. Принцип Ле Шателье.
- •3. 3. 1. Зависимость константы равновесия от температуры. Уравнения изобары химической реакции.
- •3. 3. 2. Влияние давления на равновесный выход продуктов химической реакции.
- •4. Фазовые равновесия
- •4. 1. Основные понятия и определения
- •4. 2. Условия равновесного сосуществования фаз
- •4. 3. Правило фаз Гиббса
- •4. 4. Однокомпонентные системы
- •4. 4. 1. Уравнение Клапейрона-Клаузиуса
- •4. 4. 1. 1. Применение уравнения Клапейрона-Клаузиуса к процессу плавления
- •4. 4. 1. 2. Применение уравнения Клапейрона-Клаузиуса к процессам испарения и возгонки
- •4. 4. 2. Диаграмма состояния однокомпонентной системы
- •4. 5. Метод физико-химического анализа. Диаграммы состав – свойство
- •4. 6. Двухкомпонентные системы
- •4. 6. 1. Бинарные системы взаимно растворимых жидкостей.
- •4. 6. 1. 1. Общая характеристика растворов
- •4. 6. 1. 2. Диаграмма состояния температура кипения – состав для идеального жидкого раствора
- •4. 6. 1. 3. Правило рычага
- •4. 6. 1. 4. Диаграммы температура кипения – состав для неидеальных растворов
- •4. 6. 1. 5. Разделение бинарных растворов
- •4. 6. 2. Системы взаимно нерастворимых жидкостей
- •4. 6. 2. 1. Диаграмма температура кипения состав для двух несмешивающихся жидкостей
- •4. 6. 2. 2. Перегонка с водяным паром
- •4. 7. Трехкомпонентные системы
- •4. 7. 1. Закон распределения
- •4. 7. 2. Экстрагирование
- •Библиографический список
1. 2. 4. Производительность и интенсивность
Производительностью П называют количество n (массу, объем) выработанного продукта или переработанного сырья за единицу времени τ:
![]()
Интенсивность работы реактора I или другого аппарата выражают как отношение производительности к объему реактора Vр:
![]()
1. 2. 5. Избирательность
Избирательность (селективность) – важнейшая характеристика процессов, в которых наряду с основной реакцией образования целевого продукта протекают побочные параллельные или последовательные реакции с образованием нежелательных или менее ценных продуктов. Различают конечную суммарную (интегральную) избирательность и мгновенную (дифференциальную).
Суммарная избирательность Ф определяется как отношение количества исходного вещества i, превратившегося в целевой продукт (j), к общему количеству прореагировавшего исходного вещества.
![]()
ni(j) – количество реагента, перешедшее в целевой продукт
ni – общее количество превратившегося реагента
Например, для параллельных реакций аА®bВ и aA®dD, целевым продуктом которых является вещество В, суммарная избирательность ФВ, выражается в виде:

В принятых обозначениях суммарная избирательность безразмерна и может изменяться от 0 до 1, но ее часто выражают и в процентах. Связь между степенью превращения ХА, выходом продукта Вв(а) и суммарной избирательностью ФВ определяется из выражения:
XAΦB = ВB(A)
Для выбора рациональных приемов управления селективностью проводят анализ влияния управляющих параметров на мгновенную избирательность φB. Мгновенная избирательность измеряется отношением скорости образования целевого продукта wB к скорости потребления исходного реагента на образование всех продуктов реакции wA. Иными словами, мгновенная избирательность равна отношению скорости основной реакции к общей скорости процесса, выраженной через количества исходного реагента:
![]()
Связь между суммарной и мгновенной избирательностями описывается соотношением:
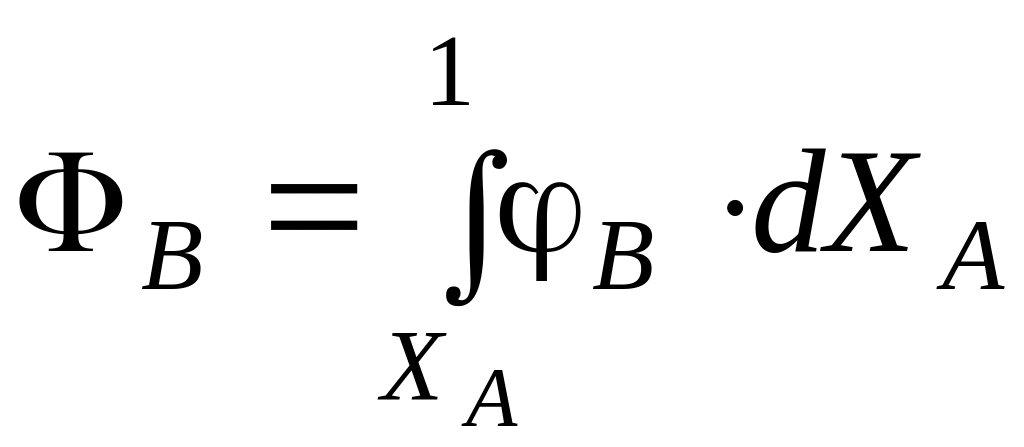
Установив уравнения связи между экономическими и технологическими показателями качества и воздействуя на технологические процессы, можно управлять эффективностью работы реакторов и ХТС, выражая эту эффективность в натуральном или денежном выражении.
1. 3. Структуры химико-технологических систем
Каждый элемент ХТС выполняет определенные функции по преобразованию параметров входящих в него потоков в параметры выходящих потоков. Следовательно, каждый элемент ХТС можно рассматривать в этом смысле как преобразователь или технологический оператор (ТО), качественно и (или) количественно преобразующий параметры входных материальных и энергетических потоков Y1,Y2,,…, Yn в физические параметры выходных материальных и энергетических потоков Z1, Z2,…, Zn. Так, реактор конверсии оксида углерода представляет собой технологический оператор, осуществляющий как качественное (в состав выходного технологического потока входят новые химические компоненты оксид углерода (IV) и водород), так и количественное (увеличение температуры и изменение количественного состава выходного потока) преобразование физических параметров входного технологического потока, включающего оксид углерода (II) и водяной пар.
Типовые технологические операторы – это элементы химического превращения, теплообмена, массообмена, смесители и делители потоков, устройства для повышения и понижения давления, изменения агрегатного состояния вещества. Типовые технологические операторы подразделяются на основные и вспомогательные (рис. 2). С помощью таких операторов можно строить различные структуры ХТС, соединяя операторы различными технологическими связями.
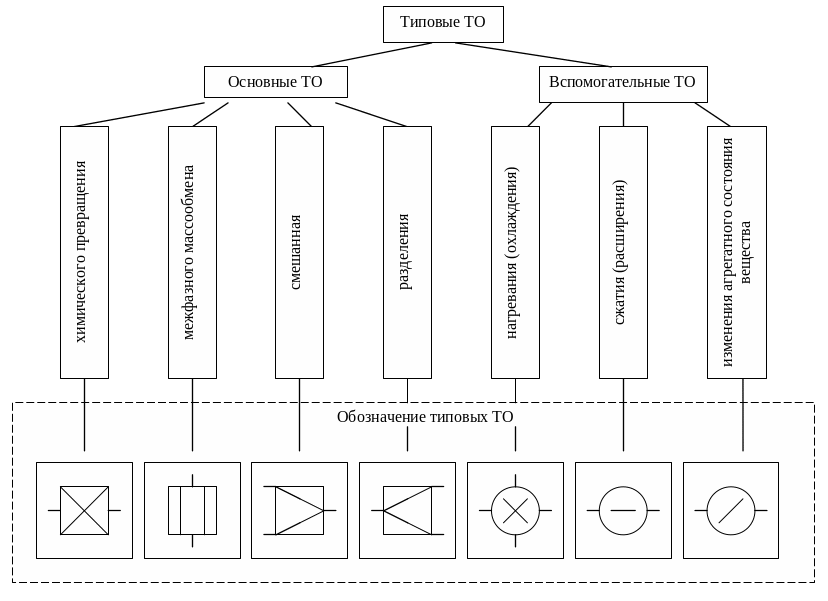
Рис. 2. Классификация технологических операторов.
Математически в самом общем виде технологический оператор можно представить в виде функции:
Y = F(Z, ТПУ),
где Y – обобщенная характеристика параметров состояния выходных технологических потоков;
Z – обобщенная характеристика параметров состояния входных технологических потоков;
ТПУ – обобщенная характеристика технологических параметров управления.
Связи между элементами выступают в виде трубопроводов, по которым передаются материальные и энергетические потоки. Связи могут быть внутренними (между аппаратами внутри ХТС) и внешними, если имеется связь между аппаратами разных ХТС.
При всем многообразии структур ХТС можно выделить основообразующие (типовые) составляющие, комбинации которых и их число обуславливает многообразие структур.
Выделяют несколько структурных составляющих химико-технологических систем с пятью типами связей между аппаратами: последовательной, параллельной, последовательно-обводной (байпас), обратной (рециркуляционной) и перекрестной (рис. 3).
