
- •Химико-технологические системы
- •Содержание
- •Введение
- •1. Химико-технологические процессы и химико-технологические системы
- •1. Термины и определения
- •2. Технологические критерии эффективности химико-технологических систем
- •1. 2. 1. Степень превращения
- •1. 2. 2. Выход продукта
- •1. 2. 4. Производительность и интенсивность
- •1. 2. 5. Избирательность
- •1. 3. Структуры химико-технологических систем
- •1. 3. 1. Хтс с последовательной технологической связью
- •1. 3. 2. Параллельная технологическая связь
- •1. 3. 3. Последовательно-обводная технологическая связь (байпас)
- •1. 3. 4. Обратная (рециркуляционная) технологическая связь
- •1. 3. 5. Перекрестная технологическая связь
- •1. 4. Системный декомпозиционный анализ химико-технологических систем
- •4. 1. Молекулярно-кинетический уровень
- •1. 4. 2. Макрокинетический уровень
- •1. 4. 3. Аппаратный уровень
- •1. 4. 4. Уровень химико-технологической системы
- •1. 4. 4. 1. Синтез химико-технологической системы
- •1. 4. 4. 2. Анализ химико-технологической системы в целом
- •1. 4. 4. 3. Оптимизация химико-технологической системы
- •2. Химическая термодинамика
- •2. 1. Основные понятия и определения
- •2. 2. Первое начало термодинамики
- •2. 2. 1. Работа расширения идеального газа
- •2. 2. 2. Теплота процесса в различных условиях
- •2. 2. 3. Закон Гесса. Расчет тепловых эффектов химических реакций с использованием стандартных теплот образования и сгорания.
- •2. 2. 4. Зависимость тепловых эффектов химических реакций от температуры. Закон Кирхгофа
- •2. 3. Второе начало термодинамики
- •2. 3. 1. Термодинамически обратимые и необратимые процессы.
- •2. 3. 2. Математическое выражение второго начала термодинамики. Энтропия.
- •2. 3. 2. 1. Энтропия и термодинамическая вероятность
- •2. 3. 2. 2. Изменение энтропии как критерий направления процессов.
- •2. 3. 2. 3. Изменение энтропии при нагревании
- •2. 3. 2. 4. Изменение энтропии при фазовых превращениях
- •2. 3. 2. 5. Расчет абсолютной энтропии вещества
- •2. 3. 2. 6. Изменение энтропии при химическом превращении
- •2. 3. 3. Применение второго начала термодинамики к химическим процессам.
- •2. 3. 3. 1. Термодинамические потенциалы
- •2. 3. 3. 2. Уравнение Гиббса-Гельмгольца
- •2. 3. 3. 3. Критерии направления процессов в закрытых системах
- •2. 3. 4. Химический потенциал идеального и реального газа. Термодинамическая активность.
- •2. 3. 5. Уравнение изотермы химической реакции
- •3. Химическое равновесие
- •3. 1. Константы равновесия
- •3. 2. Расчет равновесного состава и равновесного выхода продуктов химической реакции
- •3. 3. Влияние температуры и давления на равновесный выход продуктов реакции. Принцип Ле Шателье.
- •3. 3. 1. Зависимость константы равновесия от температуры. Уравнения изобары химической реакции.
- •3. 3. 2. Влияние давления на равновесный выход продуктов химической реакции.
- •4. Фазовые равновесия
- •4. 1. Основные понятия и определения
- •4. 2. Условия равновесного сосуществования фаз
- •4. 3. Правило фаз Гиббса
- •4. 4. Однокомпонентные системы
- •4. 4. 1. Уравнение Клапейрона-Клаузиуса
- •4. 4. 1. 1. Применение уравнения Клапейрона-Клаузиуса к процессу плавления
- •4. 4. 1. 2. Применение уравнения Клапейрона-Клаузиуса к процессам испарения и возгонки
- •4. 4. 2. Диаграмма состояния однокомпонентной системы
- •4. 5. Метод физико-химического анализа. Диаграммы состав – свойство
- •4. 6. Двухкомпонентные системы
- •4. 6. 1. Бинарные системы взаимно растворимых жидкостей.
- •4. 6. 1. 1. Общая характеристика растворов
- •4. 6. 1. 2. Диаграмма состояния температура кипения – состав для идеального жидкого раствора
- •4. 6. 1. 3. Правило рычага
- •4. 6. 1. 4. Диаграммы температура кипения – состав для неидеальных растворов
- •4. 6. 1. 5. Разделение бинарных растворов
- •4. 6. 2. Системы взаимно нерастворимых жидкостей
- •4. 6. 2. 1. Диаграмма температура кипения состав для двух несмешивающихся жидкостей
- •4. 6. 2. 2. Перегонка с водяным паром
- •4. 7. Трехкомпонентные системы
- •4. 7. 1. Закон распределения
- •4. 7. 2. Экстрагирование
- •Библиографический список
3. 2. Расчет равновесного состава и равновесного выхода продуктов химической реакции
Для расчета равновесного состава была введена универсальная величина – химическая переменная или глубина превращения ξ (кси), равная отношению изменения количества вещества данного реагента или продукта реакции к его стехиометрическому коэффициенту в уравнении химической реакции:
![]() ,
,
где знак “+” используется для продуктов реакции, а знак “ – “ для исходных веществ.
Равновесное количество вещества для каждого участника реакции выразим через глубину превращения:
![]()
Подставив полученное выражение в уравнение, связывающее термодинамическую Ka = и практическую Kn константы равновесия, получим

Решив это уравнение относительно химической переменной ξ, можно рассчитать: равновесные количества вещества каждого участника реакции, равновесные концентрации реагентов, степень превращения исходных веществ и выход продуктов реакции.
3. 3. Влияние температуры и давления на равновесный выход продуктов реакции. Принцип Ле Шателье.
Влияние параметров состояния на химическое равновесие в качественной форме было сформулировано французским физико-химиком Ле Шателье:
Если на систему, находящуюся в равновесии, оказать воздействие извне, то равновесие смещается в сторону того процесса, протекание которого уменьшает оказываемое воздействие.
Количественно состояние равновесия характеризуется константой равновесия, поэтому рассмотрим влияние различных факторов на константу равновесия и равновесный выход продуктов.
3. 3. 1. Зависимость константы равновесия от температуры. Уравнения изобары химической реакции.
Из сопоставления частного уравнения изотермы химической реакции
и уравнения Гиббса-Гельмгольца
![]()
следует, что
![]()
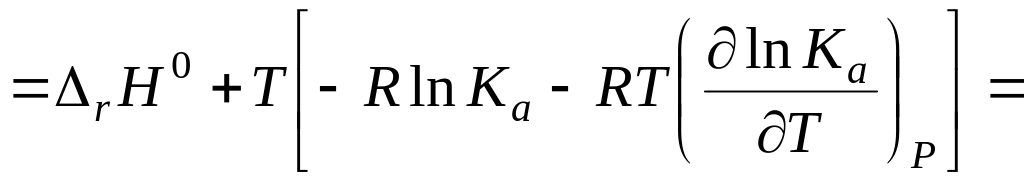
![]()
После приведения подобных членов получим уравнение изобары химической реакции:
![]()
Из дифференциального уравнения изобары химической реакции следует, что зависимость термодинамической константы равновесия Ka от температуры определяется знаком ΔrH. Проанализируем дифференциальное уравнение изобары.
1.
Если тепловой эффект реакции ΔrH
> 0 (реакция эндотермическая), то
производная
![]() > 0, и функция
> 0, и функция
![]() возрастающая. Следовательно,
термодинамическая константа равновесия
Ka
с
ростом температуры увеличивается, и
равновесный выход продуктов растет.
возрастающая. Следовательно,
термодинамическая константа равновесия
Ka
с
ростом температуры увеличивается, и
равновесный выход продуктов растет.
2. Если тепловой эффект реакции ΔrH < 0 (реакция экзотермическая), то производная < 0, и функция убывающая. Следовательно, термодинамическая константа равновесия Ka с ростом температуры уменьшается, и равновесный выход продуктов падает.
3.
Если тепловой эффект реакции ΔrH
= 0, то производная
= 0, и функция
![]() .
Следовательно, термодинамическая
константа равновесия Ka
не зависит от температуры.
Этот случай практически не наблюдается.
.
Следовательно, термодинамическая
константа равновесия Ka
не зависит от температуры.
Этот случай практически не наблюдается.
Анализ уравнения изобары химической реакции показывает полное соответствие с принципом Ле Шателье. Таким образом, уравнение изобары химической реакции является термодинамическим обоснованием принципа Ле Шателье.
3. 3. 2. Влияние давления на равновесный выход продуктов химической реакции.
Влияние давления на химическое равновесие проанализируем с помощью полученного в разд. 3. 1. уравнения
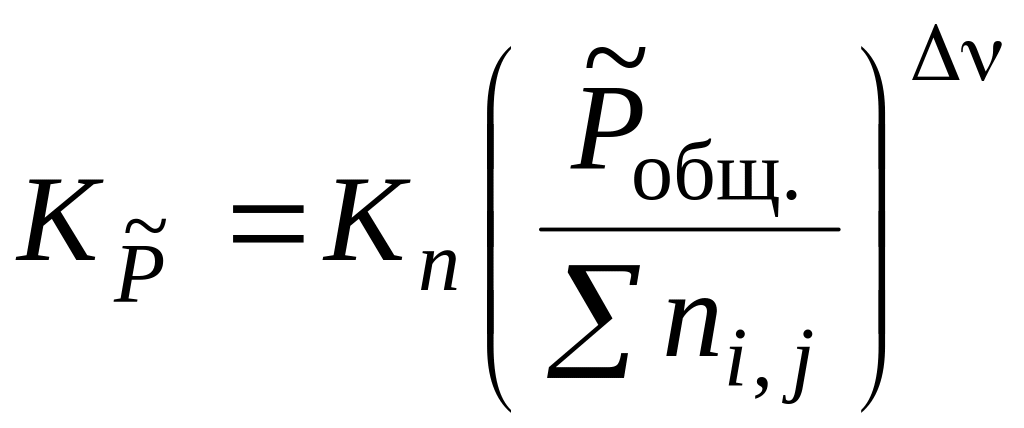
Как было показано ранее, термодинамическая константа равновесия от давления не зависит, следовательно, при P ≤ 50 атм = Ka ≠ f(P). От давления зависит практическая константа равновесия Kn. Эту зависимость удобно анализировать, переписав уравнение в виде:

Из
уравнения видно, что зависимость
практической константы равновесия Kn,
а, следовательно, и равновесного выхода
продуктов, определяется знаком
![]() .
Проанализируем эту зависимость.
.
Проанализируем эту зависимость.
1.
Если
![]() ,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
уменьшится и равновесный выход продуктов
реакции упадет.
,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
уменьшится и равновесный выход продуктов
реакции упадет.
2.
Если
![]() ,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
увеличится и равновесный выход продуктов
реакции возрастет.
,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
увеличится и равновесный выход продуктов
реакции возрастет.
3.
Если
![]() ,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
не изменится, следовательно, давление
в этом случае не влияет на равновесный
выход продуктов реакции.
,
то с увеличением общего давления в
системе практическая константа равновесия
Kn
не изменится, следовательно, давление
в этом случае не влияет на равновесный
выход продуктов реакции.
