- •Опорні лекції Статична біохімія
- •Лекція №1. Біохімія як наука. Хімічний склад організму. Хімічний склад харчових продуктів
- •З авдання біохімії:
- •Хімічний склад живих організмів
- •Знаходження води
- •Вміст води в харчових продуктах
- •Вода в продуктах
- •3 Основні групи компонентів, що формують хімічний склад харчового продукту:
- •Всі речовини, які входять до складу харчового продукту поділяють на:
- •Вміст білка в тканинах тварин і в рослинах
- •Функції білків в організмі
- •В торинна структура
- •К ласифікація білків:
- •Ф ізико-хімічні властивості білків:
- •У харчових продуктах білки знаходяться в колоїдному стані:
- •Утворення пластівців
- •Глобулярні
- •Денатурація
- •Коагуляція
- •Утворення гелів
- •Ущільнення гелю, виділення рідини
- •Фібрилярні
- •Зварювання
- •Дезагрегація
- •Методи виділення і очищення білків
- •Методи визначення білків
- •Якісне і кількісне визначення білків
- •Визначення вмісту загального та білкового азоту за методом Кьєльдаля
- •Визначення загального білка за біуретовою реакцією
- •Функціональні властивості білків
- •Лекція № 3. Ліпіди. Жири
- •Вміст жирів у харчових продуктах
- •Хімічні властивості жирів
- •Гідроліз в харчових виробництвах:
- •Фактори, які випливають на процес окислення ліпідів:
- •Методи виділення ліпідів із сировини та харчових продуктів і їх аналіз
- •Метод Сокслета для визначення вмісту сирого жиру
- •Лекція №4. Вуглеводи
- •Найважливіші представники моносахаридів і дисахаридів
- •Властивості моносахаридів Фізичні властивості моносахаридів і дисахаридів:
- •Властивості дисахаридів
- •Найважливіші представники полісахаридів
- •Гомополісахариди
- •Роль харчових волокон (25г на добу):
- •Гетерополісахариди
- •Методи визначення вуглеводів у харчових продуктах
- •Зв’язування ароматичних речовин
- •Утворення продуктів неферментативного потемніння та харчового аромату
- •Структурно-функціональні властивості полісахаридів
- •Речовини полісахаридної природи, які змінюють структуру і фізико-хімічні властивості харчових продуктів
- •Модифіковані целюлози та їх технологічні функції:
Вміст води в харчових продуктах



Плоди і овочі ‑ 70 – 90%.
М’ясо – 52 _ 78%
Риба – 55 ‑ 85%
Молоко – 88%.
Хліб – 35 ‑ 50%
Цукор – 0,14%
Форма зв’язку
води з окремими компонентами продуктів
Характеристика
форми зв’язку
Хімічно
зв’язана вода
Вода, що при
прожарюванні виділяється за рахунок
відщеплення гідроксильних груп від
молекул окремих сполук
Адсорбційно
зв’язана вода
Адсорбується
на поверхні частинок у результаті
гідратації. При нагріванні переходить
у пару.
Осмотично
поглинена вода
Вода, що
знаходиться у просторі структурної
сітки фібрилярних (волокнистих
білків) продуктів, які перебувають
у драглеподібному стані.
Капілярна
вода
Знаходиться
в капілярах, радіус яких порядку
10-5см.
У
свіжих плодах і овочах капілярна і
осмотично зв’язана вода складає до
95%, у м’язах тварин і риб знаходиться
45 – 55% осмотично зв’язаної води, 40 ‑
45% ‑ капілярної води та 6,7 – 7,5% ‑
адсорбційної води.
Різні стани води
у харчових продуктах пов’язані між
собою, між ними не спостерігається
чіткої межі. При переробці й зберіганні
продуктів вода може переходити з
однієї форми в іншу.Вода в продуктах

Харчування – це сукупність процесів, пов’язаних із вживанням та засвоєнням в організмі речовин, що входять до складу їжі.
Харчування включає: послідовні процеси надходження, перетравлювання, всмоктування та засвоєння в організмі харчових речовин, необхідних для покриття енерговитрат, побудови та відновлення клітин і тканин тіла та регуляції функцій організму.
Харчові продукти – це складні системи з єдиною внутрішньою структурою та загальними фізико-хімічними властивостями, характеризуються різноманітністю хімічної природи та складом компонентів, що їх утворюють.
3 Основні групи компонентів, що формують хімічний склад харчового продукту:
Харчова сировина - об’єкти рослинного, тваринного, мікробіологічного, мінерального походження, які використовуються для виготовлення харчових продуктів;
Харчові добавки – природні, або синтезовані речовини, сполуки, які спеціально вводять у харчові продукти в процесі виготовлення з метою надання харчовим продуктам певних (визначених) властивостей або збереження їх якостей;
Біологічно-активні добавки – концентрати природних речовин, або тих, що ідентичні природним біологічно активним речовинам, призначені до безпосереднього прийому з їжею або введення до складу харчових продуктів.
Всі речовини, які входять до складу харчового продукту поділяють на:
Харчові (макронутрієнти), аліментарні – клас головних харчових речовин, які є джерелом енергії та пластичних (структурних) матеріалів; містяться в їжі у відносно великих кількостях (від 1г). Належать білки, вуглеводи, ліпіди.
Харчові (мікронутрієнти)– клас харчових речовин, що біологічно впливають на різноманітні функції організму; містяться в їжі в невеликих кількостях (міллі- и мікрограми).
група "парафармацевтики" – речовини їжі, що спричиняють виражену фармакологічну дію. Належать біофлаваноїди, глікозиди, алкалоїди, ефірні масла, органічні кислоти.
Нехарчові (неаліментарні) речовини – містяться у харчових продуктах, проте не використовуються організмом у процесах життєдіяльності. Належать різноманітні технологічні добавки (ароматизатори, барвники, консерванти, антиоксиданти) та отруйні речовини.
Макронутрієнти: вуглеводи; ліпіди
(в тому числі холестерин); білки.
Нехарчові
речовини: баластні
речовини; ароматичні
речовини; отруйні
речовини. фосфоліпіди; амінокислоти
(в т.ч. незамінні).




Мікронутрієнти: вітаміни
та їх аналоги; мінерали
та мікроелементи; поліненасичені
жирні кислоти; олігосахариди; еубіотики.

речовини,
з яких потім синтезуються біологічно
активні речовини; харчові
волокна.
парафармацевтики: поліфеноли,
органічні кислоти, біогенні аміни,
біфлавоноїди, регуляторні пептиди,
алкалоїди, глікозиди, індоли, алліли,
кумарини, ефірні масла.
Лекція №2. Білки
Основні питання:
Білки, їх амінокислотний склад. Харчова цінність.
Біологічна роль білків в організмі.
Будова і класифікація білків.
Фізичні та хімічні властивості білків.
Колоїдний стан білків у харчових продуктах.
Методи розділення та очищення білків.
Методи визначення білків.
Функціональні властивості білків та методи їх регулювання.
Білки – високомолекулярні органічні сполуки, що побудовані із залишків α-амінокислот, які сполучені між собою пептидними зв’язками в довгі поліпептидні ланцюги (прямі і закручені). Молекулярна маса білків коливається в діапазоні від кількох тисяч (інсулін – 5700) до сотень мільйонів (білок вірусу грипу – 322млн.).
Ф.Кене в 1747 р. – термін “білки”; Н.Мульдер в 1838 р. – термін “протеїни”.
До складу білків входять 20 α-амінокислот. Всі амінокислоти білків за виключенням гліцину є L-стереоізомерами. α-Амінокислоти відрізняються одна від одної структурою і складом групи (бічного ланцюга). |
|
Загальна формула α-амінокислоти |
|
D-амінокислоти не знайдені в білках. Проте, D-форми амінокислот виділені з різних організмів у вільному стані, або у складі пептидів. Вони входять до складу мукопептидів клітинних стінок діяких мікроорганізмів, є компонентами пептидних антибіотиків (граміцидину, актиміцину).
B aмінoкиcлотax містяться дві іоногенні групи тому їх сyмapний зapяд залежить від значення pH середовища.
NH2 – CH2 – COOH ↔ +NH3 – CH2 – COO-
гліцин внутрішня сіль
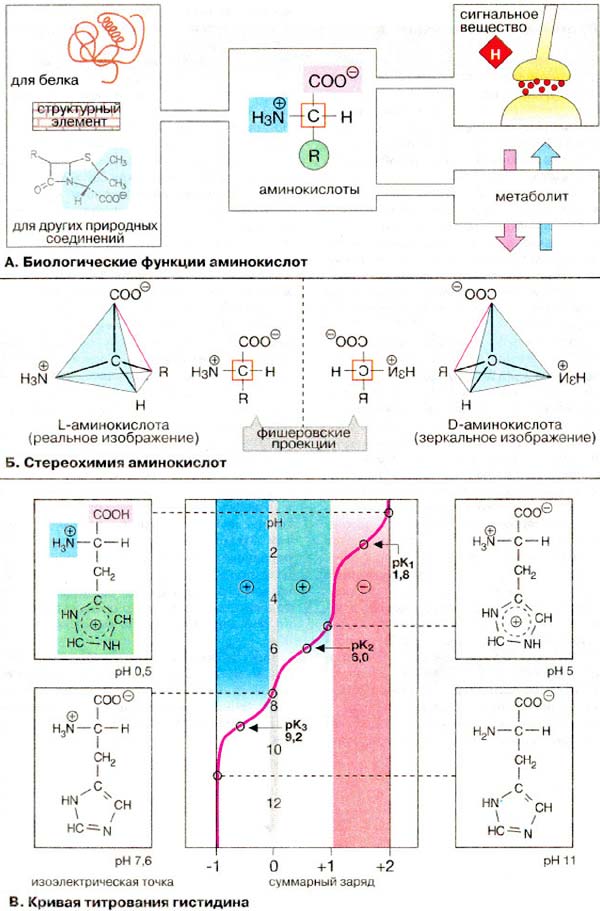
В молекулі гістидину поряд з карбоксильною та аміногрупою наявний імідазольний залишок.
|
Тому при підвищенні рН середовища заряд гістидину змінюється від +2 до -1. При рН = 7,6 сумарний заряд дорівнює нулю, назважаючи на наявність двох повністю іонізованих груп в молекулі гістидину. Величина рН, при якій сумарний заряд дорівнює нулю, називається ізоелектричною точкою. В ізоелектричній точці гістидин є цвіттер-іоном, тобто молекула виявляє властивості як аніона так і катіона. B нейтральній області рН більшість амінокислот також є цвіттер-іонами. |
Біологічна роль амінокислот:
Стpуктуpні елементи пептидів і білків. До складу білків входять 20 протеїногенних амінокислот, які кодуються генетичним кодом, і постійно містяться в білкax.
Структурні елeмeнти інших природних сполук. Aмінoкиcлoти та їх похідні входять до складу коферментів, жовчних кислот, антибіотиків.
Пepeнoсники сигналів. Деякі aмінoкиcлoти є нейромедіаторами або попередниками гормонів і нейромедіаторів.
Метаболіти. Амінoкиcлоти — життєво важливі компоненти харчування. Деякі амінокислоти беруть участь в обміні речовин, слугують донорами азоту. Непротеїногенні aмінoкиcлoти утворюються в якості проміжних продуктів при біоcинтeзі та деградації протеїногенних амінокислот або в циклі сечовини.
Білки є основною азотистою сполукою харчових продуктів, забезпечують до 15% енергоцінності добового раціону. Добова потреба людини в білках – 80-90г, половину з яких повинні складати тваринні білки.
За біологічним значенням амінокислоти поділяють на замінні і незамінні. Незамінні амінокислоти: триптофан, лізин, фенілаланін, лейцин, ізолейцин, метіонін, треонін, валін. Вони не можуть синтезуватися організмом людини, і повинні поступати з їжею. Аргінін і гістидин є незамінними для дитячого організму (у дорослих частково синтезуються).
Вміст білків у харчових продуктах:
м’ясо |
14 ‑ 20% |
|
риба |
13 ‑ 18% |
сир твердий |
22 ‑ 29% |
|
сир кисломолочний |
15 ‑ 16% |
яйця |
12 ‑ 14% |
|
крупи |
7,6 ‑ 4,9% |
соя |
33 ‑ 44% |
|
молоко |
3 ‑ 4% |
хліб пшеничний |
6 ‑ 10% |
|
картопля |
2% |
овочі |
0,5 ‑ 6,5% |
|
фрукти |
0,2 ‑ 1,5% |
Білки становлять структурну і функціональну основу всіх живих організмів. В рослинах вміст білків значно менший, ніж в організмах тварин.