
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
Условия проведения С-алкилирования аренов по Фриделю-Крафтсу определяются структурой субстрата и типом алкилирующего агента.
Алкилирование аренов алкилгалогенидами используется наиболее широко и проводится в безводном инертном растворителе (например, нитробензоле) или в избытке субстрата в присутствии кислот Льюиса:
![]()
Активность алкилгалогенидов увеличивается от первичных к третичным.
Кислота Льюиса определяет, во-первых, строение и полярность электрофильной частицы, атакующей арен. При ее взаимодействии с алкилгалогенидом образуются поляризованный комплекс, ионная пара или карбокатион:
![]()
В связи с этим, во-вторых, кислота Льюиса, определяет скорость реакции, состав продуктов реакции и возможность изомеризации алкилгалогенида и продукта реакции.
Например, состав продуктов метилирования толуола метилбромидом и метилиодидом в одних и тех же условиях разный, поэтому можно предположить, что реакция протекает с участием разных электрофильных частиц. Если бы частицей был катион СН3+, состав продуктов был бы одинаков:

Активный катализатор в большей степени образует карбокатион, который до взаимодействия с ареном успевает изомеризоваться в более устойчивый. В случае малоактивного катализатора основной атакующей частицей является поляризованный комплекс, и изомеризация алкила не наблюдается. Например, при алкилировании бензола неопентилхлоридом в присутствии AlCl3 образуется трет.пентилбензол, а в случае FeCl3, — неопентилбензол:

Хлористый алюминий практически всегда вызывает изомеризацию углеродной цепи галогеналкилов.
Алкилирование аренов геминальными ди-, три- и тетрагалогенидами идет в тех же условиях, что и с алкилгалогенидами, с образованием ди- и трифенилметана и их производных:

Однако четыре фенильных ядра к одному атому углерода не присоединяются:
![]()
Алкилирование аренов алкенами ведут в присутствии протонных или апротонных кислот в безводном инертном растворителе или в избытке субстрата аналогично алкилированию галогенидами.

Образование электрофильных частиц проходит по схеме:

Согласно другой точке зрения кислота Льюиса в присутствии протонсодержащих веществ (следы воды, спирт и др.) сначала превращается в протонную кислоту, которая и катализирует процесс:

Радикалы при двойной связи повышают ее нуклеофильность и скорость взаимодействия с катализатором, поэтому, чем больше радикалов, тем активнее алкены в реакциях с аренами.
Этим способом получают этил- и изопропилбензол (из бензола, этилена и пропилена), который служит сырьем для синтеза органических веществ.

Алкилированием бензола неразветвленными, содержащими от 10 до 15 атомов углерода алкенами (или алкилхлоридами) в присутствии фтороводорода или хлорида алюминия, с последующим сульфированием образовавшихся продуктов, получают биологически мягкие поверхностно-активные вещества:

Алкилирование аренов спиртами применяют сравнительно редко, и ведут в присутствии сильных протонных кислот (серной и фосфорной), а также хлорида алюминия, алюмосиликата и др. Реакцию проводят как в жидкой, так и в паровой фазе.
![]()
Электрофильные частицы образуются по следующим схемам:
![]()
или

Реакционная способность спиртов в этих реакциях увеличивается от первичных к третичным.
В качестве примеров можно привести синтез бутилоксианизола, который ведут в присутствии фосфорной кислоты, и метилирование фенола метанолом в парах:


Иногда вместо спиртов используют их сложные эфиры. Так, алкилирование бензола проводят -бутиролактоном в присутствии хлорида алюминия:
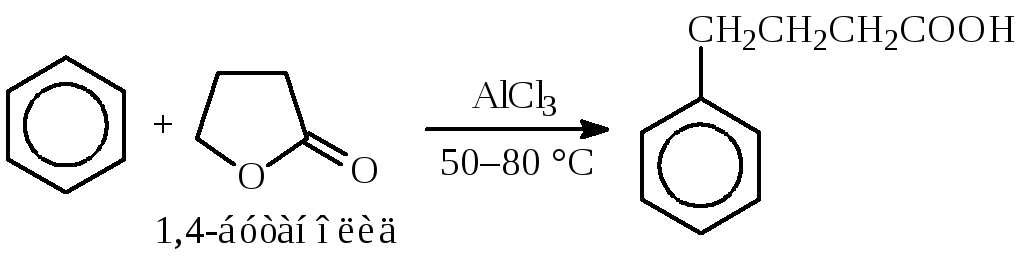
3. С-Алкилирование алифатических субстратов
Алкилирование алифатических соединений по атому углерода часто встречается в химической промышленности.
В синтезе лекарственных веществ среди других методов наибольшее значение имеет алкилирование малонового (МЭ), ацетоуксусного (АУЭ), циануксусного эфиров (ЦУЭ) и других подобных соединений. Общая химическая схема алкилирования этих веществ может быть представлена следующим образом:

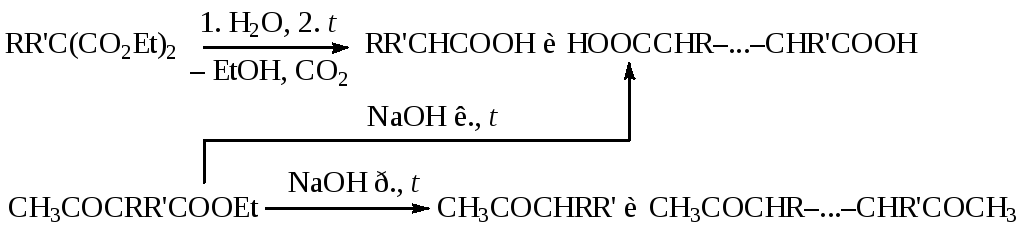
При последовательном действии на малоновый (ацетоуксусный, циануксусный) эфир металлического натрия или алкоголята натрия и алкилгалогенида один или оба водорода метиленовой группы замещаются на атомы натрия, а затем на радикал.
Замещенный малоновый эфир после гидролиза и декарбоксилирования превращается в одноосновные и двухосновные кислоты. Расщепление производных ацетоуксусного эфира концентрированной щелочью приводит к кислотам, а разбавленными щелочами или кислотами — к кетонам.
Механизм алкилирования чаще всего рассматривают как нуклеофильное замещение, уходящей группы в алкилирующем реагенте (SN2) либо присоединению по двойной связи и др.
Алкилирующими агентами в этой реакции чаще всего являются алкилгалогениды, непредельные соединения и диметилсульфат.
Например, этилбромидом алкилируют малоновый эфир и этиловый эфир фенилциануксусной кислоты:
![]()

Диметилсульфатом в присутствии алкоголятов алкилируют бензилиденцианоуксусный эфир:

При получении -формилмасляной кислоты малоновый эфир алкилируют акролеином в среде четыреххлористого углерода в присутствии метилата натрия:

