
- •Направление подготовки - 240100.62 «Химическая технология»
- •Атом углерода, его особенности, валентные состояния
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •Мезомерный эффект – используется для характеристики электронного облака π –связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
- •7. Нитрование разбавленной азотной кислотой
- •Глава 3. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизмах реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы (синтез простых эфиров)
- •Замена атома галогена на меркапто и алкил(арил)тиогруппы (синтез тиоспиртов и тиоэфиров)
- •Замена атома галогена на аминогруппы (синтез аминов)
- •Замена атома галогена на цианогруппу (синтез нитрилов кислот)
- •Замена атома галогена на группу -so3Na (синтез сульфокислот)
- •Замена атома галогена на группу –no2 (синтез нитросоединений)
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •Глава 5. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором (непрероывный метод)
- •2. Окисление растворов бромида натрия гипохлоритом натрия (периодический):
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
7. Сульфирование комплексными соединениями триоксида серы
С органическими основаниями серный ангидрид образует комплексы с переносом заряда:
![]()
Между молекулой донора (L) и SO3 образуется донорно-акцепторная (координационная) связь.
Устойчивость комплексов серного ангидрида повышается с увеличением электронодонорных свойств лиганда. При этом их сульфирующая активность уменьшается.

Электронодонорные свойства (сила основания) лигандов уменьшаются в ряду: третичные амины > пиридин > сульфоксиды > триалкилфосфаты > эфиры.
Комплексы серного ангидрида с третичными аминами NAlk3.SO3 являются наиболее устойчивыми и наименее реакционноспособными соединениями. Они практически не диссоциируют в инертных средах (спиртах, полигалогенидах, алканах). При использовании их в качестве сульфирующих агентов во многих случаях требуется дополнительное введение оснований.
Комплексом SO3·NAlk3 сульфатируют гидроксисоединения, например, полисахариды, в водно-щелочной среде. Этот процесс является нуклеофильным замещением SN2 и во всех случаях сохраняется высокая селективность реакции:

Комплексы серного ангидрида с пиридином (Py·SO3) (А.П. Терентьев с сотр.) также практически не диссоциируют в инертных растворителях. До недавнего времени ими сульфировали ацидофобные соединения.
Однако этот метод имеет ряд существенных недостатков: невысокий выход продукта и низкая селективность процесса; необходимы избыток сульфирующего агента (Py·SO3) и относительно жесткие условия сульфирования (> 100 °С); большая длительность процесса (10—72 ч.) и проведение реакции под давлением; сложность очистки продукта реакции от токсичного пиридина, который образует с продуктом реакции соли RSO3Py.
Диссоциируемые комплексы серного ангидрида являются достаточно устойчивыми и активными сульфирующими агентами.
-
В случае сильно диссоциированных комплексов (комплексы SO3 c простыми и сложными эфирами) сульфирование проходит, главным образом, за счет SO3, образующегося при диссоциации комплекса. Механизм сульфирования аренов в инертной среде при избытке реагента классический, при мольном соотношение реагентов реализуется пиросульфатная схема.
-
В случае слабодиссоциируемых комплексов (комплексы SO3 с амидами, сульфоксидами и триалкилфосфатами) — сульфирование проходит как молекулой SO3, так и поляризованным комплексом.
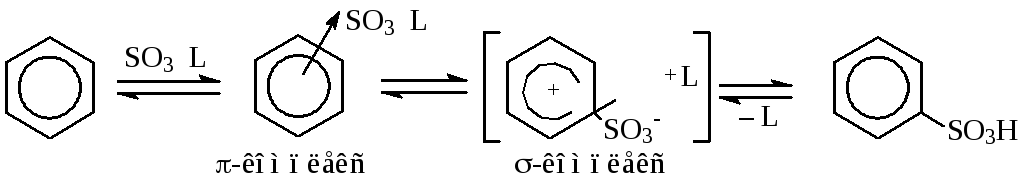
В переходном состоянии при образовании связи атома серы с углеродом арена (при образовании -комплекса) лиганд отщепляется.
Разработанные Б.В.Пассетом с сотр. методы позволяют сульфировать замещенные пятичленные гетероциклы с одним гетероатомом в мягких условиях с выходом 85—95 %.
Глава 2. Процессы нитрования органических соединений
Органические вещества, содержащие нитрогруппу, называются нитросоединениями. Наиболее важным методом их получения является нитрование — непосредственное замещение атома водорода в органическом соединении группой –NO2. Как правило, на нитрогруппу замещают атом водорода, расположенный при углероде (С-нитрование). Кроме этого к процессам нитрования относят также реакции замены атома водорода в гидроксильной и аминогруппах с получением нитратов RONO2 и N-нитраминов RNHNO2 (О- и N- нитрование). Субстратом, в основном, служат карбоциклические и гетероциклические ароматические соединения. Алифатические соединения нитруются значительно реже. Среди них чаще всего встречаются спирты, гликоли, полисахариды. Нитрующими агентами являются азотная кислота и ее смеси с разными реагентами, чаще всего, с кислотами. Основным побочным процессом при нитровании является окисление.
Другие способы получения нитросоединений (например, нуклеофильной заменой галогена) имеют значительно меньшее значение.
Нитросоединения (С-, N- и О-) — это жидкости или кристаллические вещества, плохо растворимые в воде, хорошо в органических растворителях, большей частью взрывоопасные. Мононитросоединения не обладают взрывчатыми свойствами, однако нитрогруппы значительно увеличивают скорость их термического разложения. Динитросоединения уже являются взрывчатыми веществами. С увеличением числа нитрогрупп в молекуле соединения взрывчатые свойства его усиливаются. Алифатические нитросоединения могут существовать в двух таутомерных формах (аци-нитро-таутометрия). Практически все нитросоединения токсичны.
Вместе с тем, нитрогруппа имеется в молекуле многих ценных лекарственных веществ. И хотя биологическое действие этих препаратов определяется не только нитрогруппой, установлено, что она вмешивается в процессы окислительного фосфорилирования в организмах паразитов в большей степени, чем в организме больного человека. В связи с этим среди нитросоединений много противомикробных и противопаразитарных средств, например, фурацилин, левомицетин, п-нитробензилпенициллин и др.
Органические нитраты обнаруживают сосудорасширяющее и спазмолитическое действие на организм (нитроглицерин, нитросорбид).
Кроме того, нитросоединения являются промежуточными продуктами в синтезе лекарственных веществ и витаминов.
