
- •Часть 1
- •Изучаемые вопросы:
- •1. Предмет химии. Значение химии в изучении природы и развитии техники
- •Атомная масса (атомный вес) природного элемента. Изотопный состав элементов. Дефект массы.
- •2. Основные количественные законы химии
- •Вопросы для самоконтроля
- •Литература
- •Лекция 3-5 (6 ч)
- •Тема 3. Агрегатное состояние вещества
- •Изучаемые вопросы:
- •3.1. Общая характеристика агрегатного состояния вещества
- •3.2. Газообразное состояние вещества. Законы идеальных газов. Реальные газы
- •3.3. Характеристика жидкого состояния вещества
- •3.4. Характеристика твёрдого состояния
- •Характеристики некоторых веществ
- •3.5. Типы кристаллических решёток
- •Вопросы для самоконтроля:
- •Вопросы для самостоятельной работы:
- •Литература:
- •Лекция 6-8 (6 ч)
- •Тема 1. Строение вещества. Периодическая система элементов д. И. Менделеева
- •Изучаемые вопросы:
- •1.1. Современная модель строения атома
- •1.2. Квантовые числа
- •Орбитальное квантовое число 0 1 2 3 4
- •1.3. Строение многоэлектронных атомов
- •1.4. Периодические свойства элементов
- •1.5. Периодическая система элементов д. И. Менделеева
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 9-11 (6 ч)
- •Тема 2. Химическая связь и взаимодействия между молекулами
- •Изучаемые вопросы:
- •2.1. Общая характеристика химической связи
- •2.2. Типы химической связи
- •2.3.Типы межмолекулярных взаимодействий
- •2.4. Пространственная структура молекул
- •Число гибридных орбиталей равно числу исходных. При смешении s и р-орбиталей образуется две sp-гибридных орбитали, угол между осями которых равен 180°.
- •Метод валентных связей
- •Метод молекулярных орбиталей
- •Химическая связь в комплексных соединениях
- •Координационная теория Вернера
- •Номенклатура комплексных соединений
- •Диссоциация комплексных соединений
- •Природа химической связи в комплексах
- •Вопросы для самоконтроля:
- •Вопросы для самостоятельной работы:
- •Литература:
- •Лекции 12-13 (4 ч)
- •Тема 4. Энергетика химических процессов
- •Изучаемые вопросы:
- •4.1. Общие понятия термодинамики
- •4.2. Первый закон (начало) термодинамики. Внутренняя энергия системы. Энтальпия системы
- •4.3. Термохимия. Тепловые эффекты химических реакций
- •4.4. Закон Гесса и следствия из него
- •I путь.
- •II путь.
- •4.5. Основные формулировки второго закона (начала) термодинамики
- •4.6. Принцип работы тепловой машины. Кпд системы
- •4.7. Свободная и связанная энергии. Энтропия системы
- •4.8. Энергия Гиббса, энергия Гельмгольца и направленность химических реакций
- •Для определения температуры (Тр), выше которой происходит смена знака энергии Гиббса реакции, можно воспользоваться условием
- •Вопросы для самоконтроля:
- •Литература:
- •Лекции 14-15 (4 ч)
- •Тема 5. Химическая кинетика и катализ
- •Изучаемые вопросы:
- •5.1. Понятие о химической кинетике
- •5.2. Факторы, влияющие на скорость химических реакций. Закон действующих масс
- •5.3. Классификация химических реакций по молекулярности и по порядку
- •5.4. Кинетические уравнения реакци первого и второго порядка
- •Поле интегрирования
- •5.5. Теория активизации молекул. Уравнение Аррениуса
- •5.6. Особенности каталитических реакций. Теории катализа
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 16 (2 ч)
- •Тема 6. Химическое равновесие
- •Изучаемые вопросы:
- •6.1. Обратимые и не обратимые реакции. Признаки химического равновесия
- •6.2. Константа химического равновесия
- •6.3. Факторы, влияющие на химическое равновесие. Принцип Ле-Шателье
- •6.4. Правило фаз Гиббса. Диаграмма состояния воды
- •Правило фаз для воды имеет вид
- •6.5. Понятие о химическом сродстве веществ. Уравнения изотермы, изобары и изохоры химических реакций
- •Вопросы для самоконтроля:
- •Лекции 15-17 (6 ч)
- •Тема 7. Растворы. Дисперсные системы
- •Изучаемые вопросы:
- •7.1. Сольватная (гидратная) теория растворения
- •7.2. Общие свойства растворов
- •7.3. Типы жидких растворов. Растворимость
- •7.4. Свойства слабых электролитов
- •7.5. Свойства сильных электролитов
- •7.6. Классификация дисперсных систем
- •7.7. Получение коллоидно-дисперсных систем
- •7.8. Устойчивость коллоидных растворов. Коагуляция. Пептизация
- •7.9. Свойства коллоидно-дисперсных систем
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 13 (2ч)
- •Тема 8. Кислотно-основные и окислительно-восстановительные свойства вещества
- •Изучаемые вопросы:
- •8.1. Особенности обменных процессов
- •8.2. Особенности окислительно-восстановительных процессов
- •Вопросы для самоконтроля:
- •Литература:
- •Лекции 14-15 (4 ч)
- •Тема 9. Электрохимические системы
- •Изучаемые вопросы:
- •9.4. Электродвижущая сила гальванического элемента.
- •9.1. Общие понятия электрохимии. Проводники первого и второго рода
- •9.2. Понятие об электродном потенциале
- •9.3. Гальванический элемент Даниэля-Якоби
- •9.4. Электродвижущая сила гальванического элемента
- •9.5. Классификация электродов
- •9.6. Поляризация и перенапряжение
- •9.7. Электролиз. Законы Фарадея
- •9.8. Коррозия металлов
Лекция 13 (2ч)
Тема 8. Кислотно-основные и окислительно-восстановительные свойства вещества
Цель лекции: ознакомится с особенностями обменных и окислительно-восстановительных процессов, рассмотреть гидролиз солей и константу гидролиза, теории электролитической диссоциации, протонную и электронную теории кислот и оснований; дать определение степени окисления и правила расчета СО; познакомиться с методами составления уравнений окислительно-восстановительных реакций: электронного баланса и полуреакций (электронно-ионный метод); показать направление окислительно-восстановительных реакций.
Изучаемые вопросы:
8.1. Особенности обменных процессов.
8.2. Особенности окислительно-восстановительных процессов.
8.1. Особенности обменных процессов
Химические реакции разделяются на обменные и окислительно-восстановительные (Ox-Red). Если в реакции не происходит изменение степени окисления, то такие реакции называются обменными. Они возможны при условии, что образуется осадок, малодиссоциирующее вещество или выделяется газ.
Типы обменных химических процессов в водной среде: реакции нейтрализации – процесс между кислотой и щелочью:
HCl + NaOH → NaCl + H2O,
взаимодействие между кислотой и солью:
HCl + AgNO3 → HNO3+ AgCl↓,
реакции между щелочью и солью:
Ba(OH)2 + K2SO4 → BaSO4↓ + KOH,
реакции между двумя растворимыми солями:
AgNO3 + KCl → KNO3 + AgCl↓,
гидролиз солей – реакции обмена между водой и растворенными в ней солями. Гидролизу подвергаются растворимые соли, образованные сильными кислотами и слабыми основаниями (а); слабыми кислотами и сильными основаниями (б); слабыми кислотами и слабыми основаниями (в):
а) NH4Cl + H2O NH4OH + HCl
или в ионном виде:
NH4+ + Cl- + H2O NH4OH + H+ + Cl-
в сокращенном ионном виде:
NH4+ + H2O NH4OH + H+ (pH <7 – среда кислая)
константа равновесия этой системы:
KС
=
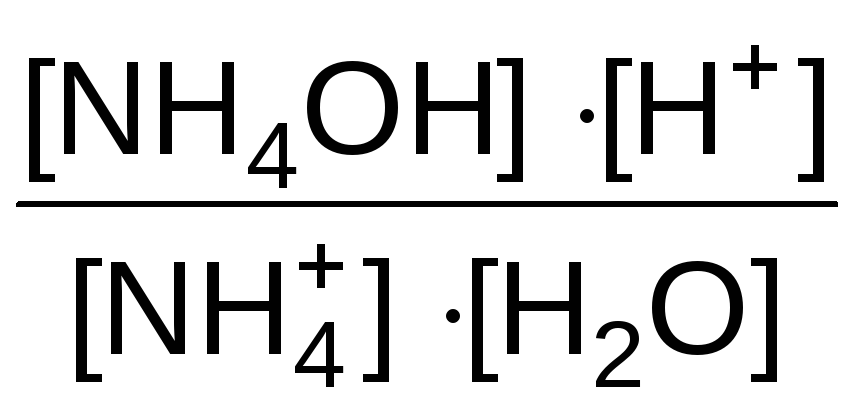
Поскольку концентрация воды при гидролизе изменяется очень мало, то ее принимают постоянной и, умножая на константу равновесия, получают константу гидролиза Kг:
KС[H2O]
= Kг
=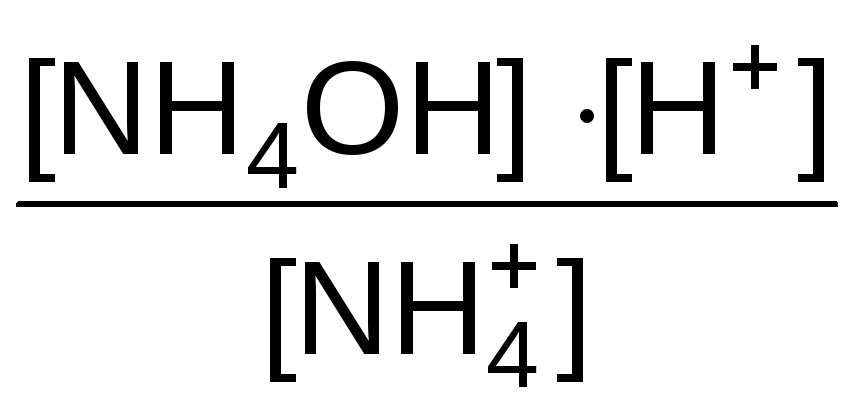 (8.1)
(8.1)
Умножим числитель и знаменатель уравнения (8.1) на концентрацию OH—ионов:
KГ
=
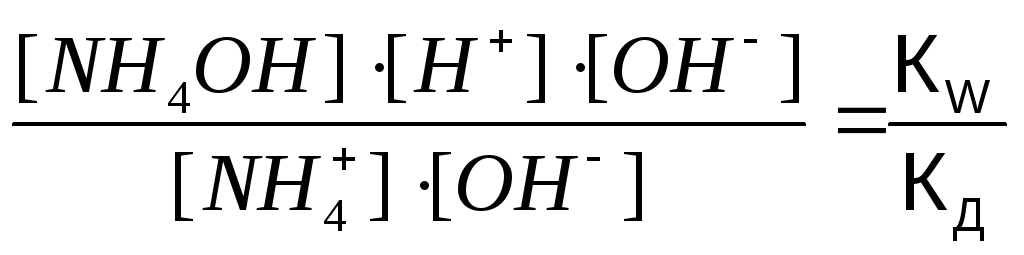 (8.2)
(8.2)
Константа гидролиза соли зависит от природы соли, температуры. Показателем глубины протекания гидролиза является степень гидролиза (β), которая представляет собой отношение концентрации гидролизованных молекул Cгидр к исходной концентрации растворенных молекул электролита:
β = Сгидр/С; (С = β.Сгидр) (8.3)
Степень гидролиза, как правило, невелика. Например, 0,1 моль/дм3 CH3COONa при 298К β = 10-4. Это связано с тем, что вода – слабый электролит и равновесие смещается в сторону исходных веществ. С увеличением температуры и снижением концентрации соли степень гидролиза снижается (гидролиз – эндотермический процесс).
Уравнение (8.1) с учетом (8.3) принимает вид:
KГ
=
![]() (8.4)
(8.4)
Если β << 1, то
Kг = β2C (8.5)
Следовательно
β
=![]() (8.6)
(8.6)
Используя последнее уравнение можно найти концентрацию ионов водорода, а, следовательно, и pH раствора:
[H+]
= βC
=
![]() pH
= -lg
pH
= -lg![]() (8.7)
(8.7)
б) Гидролиз ацетата натрия:
CH3COONa + H2O CH3COOH + NaOH
CH3COO- + H2O CH3COOH + OH- (pH 7 – щелочная среда)
Степень гидролиза и константа гидролиза в данном случае описываются теми же уравнениями (8.2), (8.3) и (8.4), но лишь с тем исключением, что в уравнениях (8.2) и (8.4) входит константа диссоциации слабой кислоты.
Равновесную концентрацию гидроксид ионов рассчитывают по уравнению:
[OH-]
= βC
=![]() (8.8)
(8.8)
Отсюда
рH
= pKв-
pOH
= pKв
– lg![]() (8.9)
(8.9)
Если гидролизу подвергается многоосновный анион, то гидролиз протекает по стадиям:
CO![]() +
H2O
HCO
+
H2O
HCO![]() +
OH-
+
OH-
HCO![]() + H2O
H2CO
+ H2O
H2CO![]() +
OH-
+
OH-
константа гидролиза
по первой ступени значительно выше, чем
константа гидролиза по последней
ступени. Например, для гидролиза CO![]() ,
при 298 К:
,
при 298 К:
КГ1 = 2.10-4; К Г2 = 2,2.10-8.
Поэтому при расчете концентрации иона [ОН-] или [Н+], второй и третьей ступенью обычно пренебрегают. Для расчета константы гидролиза по первой ступени входит константа диссоциации слабого электролита по первой ступени:
CO![]() +
H2O
HCO
+
H2O
HCO![]() +
OH-
+
OH-
равна
![]()
в) Рассмотрим гидролиз растворимой соли, образованной слабой кислотой и слабым основанием:
NH4F + H2O NH4OH + HF
или в ионной форме
NH4+
+ F-
+ H2O
NH4+
+ OH-
+ H+
+ F-
(pH![]() 7,
среда нейтральна)
7,
среда нейтральна)
![]() (8.9)
(8.9)
Степень гидролиза и концентрация ионов водорода в этом случае не зависит от исходной концентрации соли:
![]() (8.10)
(8.10)
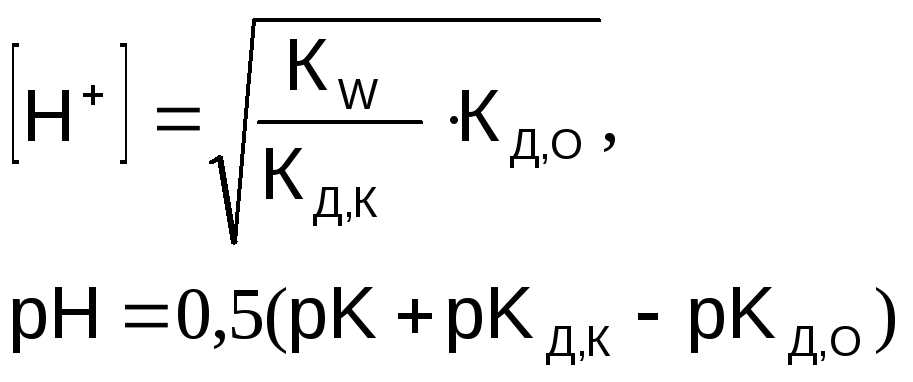 (8.11)
(8.11)
(8.12)
Как видно, в зависимости от соотношения pКД,К и pКД,О среда может иметь как кислую, так и основную реакцию.
Таким образом, при гидролизе солей, образованных слабыми кислотами или (и) основаниями, происходит подщелачивание или подкисление раствора, степень гидролиза возрастает с разбавлением раствора при увеличении температуры.
Теории кислот и оснований. При объяснении кислотно-основных взаимодействий применяют различные подходы; большинство теорий не противоречат друг другу, но имеют различные области применения. Наиболее известны теория, основанная на механизме электролитической диссоциации, протонная и электронная теории кислот и оснований.
Согласно теории
электролитической диссоциации,
применимой к водным растворам, кислотой
является
электролит, который диссоциирует с
образованием ионов Н![]() (или
гидроксония Н3О+).
Сильные кислоты (НСl,
НNО3,
Н2SО4
и др.) диссоциируют практически полностью,
у слабых кислот диссоциирована лишь
часть молекул. О силе кислот можно судить
по константе диссоциации. Чем больше
константа диссоциации, тем больше
диссоциирована кислота.
(или
гидроксония Н3О+).
Сильные кислоты (НСl,
НNО3,
Н2SО4
и др.) диссоциируют практически полностью,
у слабых кислот диссоциирована лишь
часть молекул. О силе кислот можно судить
по константе диссоциации. Чем больше
константа диссоциации, тем больше
диссоциирована кислота.
Электролит,
диссоциирующий с образованием ОН![]() ,
называют основанием.
Сильные основания (LiOH,
NaOH,
KOH
и др.) диссоциируют полностью, у слабых
оснований диссоциации подвергается
лишь часть молекул.
,
называют основанием.
Сильные основания (LiOH,
NaOH,
KOH
и др.) диссоциируют полностью, у слабых
оснований диссоциации подвергается
лишь часть молекул.
Амфотерные электролиты диссоциируют как кислоты (2H+ + [Zn(OH)4]-2), и как основания ([Zn(H2O)2]+2 + OH-), например:
2H+ + [Zn(OH)4]-2 Zn(OH)2 + H2O [Zn(H2O)2]+2 + OH-
При взаимодействии гидроксида цинка, например, с азотной кислотой образуется нитрат цинка:
Zn(OH)2 + 2НNО3 = Zn(NО3)2 + 2H2O
при взаимодействии же с гидроксидом калия – цинкат калия:
Zn(OH)2 + 2KOH = K2[Zn(OH)4]
К амфотерным электролитам так же относятся гидроксиды алюминия Al(OH)3, свинца Pb(OH)2, олова Sn(OH)2 и др. Амфотерность электролитов объясняется малым различием связей R-OH и O-H.
Теория электролитической диссоциации неприменима к взаимодействиям, не сопровождающимся диссоциацией на ионы. Например, аммиак, реагируя с безводным фтором водорода, образует соль фторид аммония NH3 + HF = NH4F. Аммиак, не имея в своем составе гидроксидной группы, ведет себя как основание.
Протонная теория кислот и оснований Д. Брендстеда (1923) применима как к водным, так и неводным средам. Согласно протонной теории, кислоту считают донором протона, а основание – акцептором протонов. При взаимодействии кислота отдает, а основание принимает протон. Соотношение между основанием и кислотой можно представить схемой:
Основание + Протон Кислота
Основание и кислота, связанные данным соотношением, называются сопряженными. Взаимодействие между кислотой и основанием согласно протонной теории проходит по схеме:
Кислота1 + Основание2 Кислота2 + Основание1
В зависимости от партнера, то или иное вещество может быть или кислотой, или основанием. Например, вода по отношению к аммиаку является кислотой, по отношению к фториду водорода – основанием, а при диссоциации – и как кислота, и как основание:
H2O + NH3 OH- + NH4+
HF + H2O F- + OH3+
H2O + H2O OH- + OH3+
кислота основание основание кислота
Кислотно-основные свойства, согласно протонной теории, количественно характеризуются протонным сродством, или энергией, которая выделяется при присоединении протона к молекуле или иону. Роль основания играет тот партнер, у которого протонное сродство выше.
Электронная теория кислот и оснований выдвинута Дж. Льюисом (1924). Согласно этой теории, кислота является акцептором, а основание – донором электронов. Если в состав кислоты входит водород, то она называется водородной, а если не входит, то – апротонной. Взаимодействие кислоты и основания по Льюису, приводит к образованию ковалентной связи по донорно-акцепторному механизму:
![]()
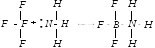
Кислота основание продукт нейтрализации
Электронная теория охватывает более широкий круг соединений, чем протонная теория.
Таким образом, кислотно-основные взаимодействия объясняются теорией электролитической диссоциации, протонной или электронной теориями.
