
- •Часть 1
- •Изучаемые вопросы:
- •1. Предмет химии. Значение химии в изучении природы и развитии техники
- •Атомная масса (атомный вес) природного элемента. Изотопный состав элементов. Дефект массы.
- •2. Основные количественные законы химии
- •Вопросы для самоконтроля
- •Литература
- •Лекция 3-5 (6 ч)
- •Тема 3. Агрегатное состояние вещества
- •Изучаемые вопросы:
- •3.1. Общая характеристика агрегатного состояния вещества
- •3.2. Газообразное состояние вещества. Законы идеальных газов. Реальные газы
- •3.3. Характеристика жидкого состояния вещества
- •3.4. Характеристика твёрдого состояния
- •Характеристики некоторых веществ
- •3.5. Типы кристаллических решёток
- •Вопросы для самоконтроля:
- •Вопросы для самостоятельной работы:
- •Литература:
- •Лекция 6-8 (6 ч)
- •Тема 1. Строение вещества. Периодическая система элементов д. И. Менделеева
- •Изучаемые вопросы:
- •1.1. Современная модель строения атома
- •1.2. Квантовые числа
- •Орбитальное квантовое число 0 1 2 3 4
- •1.3. Строение многоэлектронных атомов
- •1.4. Периодические свойства элементов
- •1.5. Периодическая система элементов д. И. Менделеева
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 9-11 (6 ч)
- •Тема 2. Химическая связь и взаимодействия между молекулами
- •Изучаемые вопросы:
- •2.1. Общая характеристика химической связи
- •2.2. Типы химической связи
- •2.3.Типы межмолекулярных взаимодействий
- •2.4. Пространственная структура молекул
- •Число гибридных орбиталей равно числу исходных. При смешении s и р-орбиталей образуется две sp-гибридных орбитали, угол между осями которых равен 180°.
- •Метод валентных связей
- •Метод молекулярных орбиталей
- •Химическая связь в комплексных соединениях
- •Координационная теория Вернера
- •Номенклатура комплексных соединений
- •Диссоциация комплексных соединений
- •Природа химической связи в комплексах
- •Вопросы для самоконтроля:
- •Вопросы для самостоятельной работы:
- •Литература:
- •Лекции 12-13 (4 ч)
- •Тема 4. Энергетика химических процессов
- •Изучаемые вопросы:
- •4.1. Общие понятия термодинамики
- •4.2. Первый закон (начало) термодинамики. Внутренняя энергия системы. Энтальпия системы
- •4.3. Термохимия. Тепловые эффекты химических реакций
- •4.4. Закон Гесса и следствия из него
- •I путь.
- •II путь.
- •4.5. Основные формулировки второго закона (начала) термодинамики
- •4.6. Принцип работы тепловой машины. Кпд системы
- •4.7. Свободная и связанная энергии. Энтропия системы
- •4.8. Энергия Гиббса, энергия Гельмгольца и направленность химических реакций
- •Для определения температуры (Тр), выше которой происходит смена знака энергии Гиббса реакции, можно воспользоваться условием
- •Вопросы для самоконтроля:
- •Литература:
- •Лекции 14-15 (4 ч)
- •Тема 5. Химическая кинетика и катализ
- •Изучаемые вопросы:
- •5.1. Понятие о химической кинетике
- •5.2. Факторы, влияющие на скорость химических реакций. Закон действующих масс
- •5.3. Классификация химических реакций по молекулярности и по порядку
- •5.4. Кинетические уравнения реакци первого и второго порядка
- •Поле интегрирования
- •5.5. Теория активизации молекул. Уравнение Аррениуса
- •5.6. Особенности каталитических реакций. Теории катализа
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 16 (2 ч)
- •Тема 6. Химическое равновесие
- •Изучаемые вопросы:
- •6.1. Обратимые и не обратимые реакции. Признаки химического равновесия
- •6.2. Константа химического равновесия
- •6.3. Факторы, влияющие на химическое равновесие. Принцип Ле-Шателье
- •6.4. Правило фаз Гиббса. Диаграмма состояния воды
- •Правило фаз для воды имеет вид
- •6.5. Понятие о химическом сродстве веществ. Уравнения изотермы, изобары и изохоры химических реакций
- •Вопросы для самоконтроля:
- •Лекции 15-17 (6 ч)
- •Тема 7. Растворы. Дисперсные системы
- •Изучаемые вопросы:
- •7.1. Сольватная (гидратная) теория растворения
- •7.2. Общие свойства растворов
- •7.3. Типы жидких растворов. Растворимость
- •7.4. Свойства слабых электролитов
- •7.5. Свойства сильных электролитов
- •7.6. Классификация дисперсных систем
- •7.7. Получение коллоидно-дисперсных систем
- •7.8. Устойчивость коллоидных растворов. Коагуляция. Пептизация
- •7.9. Свойства коллоидно-дисперсных систем
- •Вопросы для самоконтроля:
- •Литература:
- •Лекция 13 (2ч)
- •Тема 8. Кислотно-основные и окислительно-восстановительные свойства вещества
- •Изучаемые вопросы:
- •8.1. Особенности обменных процессов
- •8.2. Особенности окислительно-восстановительных процессов
- •Вопросы для самоконтроля:
- •Литература:
- •Лекции 14-15 (4 ч)
- •Тема 9. Электрохимические системы
- •Изучаемые вопросы:
- •9.4. Электродвижущая сила гальванического элемента.
- •9.1. Общие понятия электрохимии. Проводники первого и второго рода
- •9.2. Понятие об электродном потенциале
- •9.3. Гальванический элемент Даниэля-Якоби
- •9.4. Электродвижущая сила гальванического элемента
- •9.5. Классификация электродов
- •9.6. Поляризация и перенапряжение
- •9.7. Электролиз. Законы Фарадея
- •9.8. Коррозия металлов
7.9. Свойства коллоидно-дисперсных систем
Все свойства коллоидно-дисперсных систем можно разделить на три основные группы: молекулярно-кинетические, оптические и электрокинетические.
Рассмотрим молекулярно-кинетические свойства коллоидных растворов, к ним относят:
Броуновское движение – непрерывное хаотичное движение частиц по всему объему. Причем расстояние, на которое перемещается частица в данном направлении за определенное время (называемое смещением) будет тем больше, чем меньше вязкость дисперсионной среды и размер частиц, и чем выше температура.
Другое молекулярно-кинетическое свойство – это диффузия. Диффузия – это самопроизвольный процесс выравнивания концентраций по всему объему под влиянием броуновского движения. Причем скорость диффузии возрастает с ростом температуры и уменьшением размера частиц и вязкости дисперсионной среды, т. е. от тех же факторов, что и смещение при броуновском движении.
Третье молекулярно-кинетическое свойство коллоидных растворов – это осмотическое давление. Оно очень мало и с трудом поддается измерению. Это связано с тем, что осмотическое давление коллоидных растворов определяется не молярной концентрацией ( = CRT) находящегося в дисперсионной среде вещества, а числом частиц в единице объема, которое много меньше, чем концентрация.
По оптическим свойствам коллоидные растворы существенно отличаются от истинных растворов низкомолекулярных веществ и грубодисперсных систем. Это связано с тем, что в коллоидных растворах размер частиц соизмерим с длиной волны падающего света, поэтому наиболее характерными оптическими свойствами коллоидно-дисперсных систем являются опалесценция, эффект Фарадея-Тиндаля, адсорбция света поверхность коллоидных частиц.
Опалесценция – это явление рассеяния света мельчайшими частицами (самосвечение каждой частицы). Поэтому окраска золей в отраженном и проходящем свете будет различной. Например, белые золи в проходящем свете имеют красно-желтую окраску, а в отраженном – голубоватую.
Эффект Фарадея-Тиндаля (1857): образование светового конуса при прохождении луча света через коллоидный раствор. Для того, чтобы решить, является раствор коллоидным или нет, необходимо проверить его на эффект Фарадея-Тиндаля.
Окраска коллоидно-дисперсных систем связана с адсорбцией света поверхности частиц. Если тело способно поглощать все длины волн падающего света, то оно называется абсолютно черным; если тело отражает свет, то оно называется белым. Большинство тел способно поглощать лишь часть спектра, т. е. они обладают избирательной адсорбцией, и этим объясняется интенсивная окраска коллоидно-дисперсных систем, которая во много раз превышает интенсивность окраски истинных растворов.
К электрокинетическим свойствам относят электроосмос и электрофорез.
Электроосмос – это явление перемещения жидкости в электрическом поле относительно неподвижной твердой поверхности (движение частиц дисперсионной среды).
Электрофорез – явление перемещения твердых частиц в электрическом поле относительно неподвижной жидкости к электроду, знак которого противоположен заряду перемещающихся частиц (движение частиц дисперсной фазы).
Эти явления впервые были обнаружены Ф. Ф. Рейссом (1909) при воздействии постоянного электрического тока на диспергированную в воде глину (рис. 9). Под действием электрического тока, отрицательно заряженные частицы глины перемещаются к аноду с зарядом «+», а дисперсная среда, имеющая положительно заряженные ионы водорода (H+) перемещается в сторону катода, с зарядом «-». При этом в трубке с анодом уровень жидкости уменьшается и раствор мутнеет, а в трубке с катодом уровень жидкости увеличивается и она остается прозрачной.
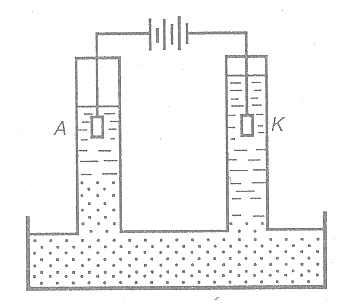
Рис 9. Схема устройства
для демонстрации электрофореза
Коллоидные растворы в природе и технике. В природной воде содержится часть примесей в коллоидном состоянии. Поэтому воду, используемую для коммунальных нужд, электростанций, строительства подвергают обработке, вызывающей коагуляцию коллоидных частиц. Дымовые газы электростанций, металлургических заводов и других предприятий представляют собой аэрозоли. Для их коагуляции применяется электрогазоочистка методом электрофореза при очень высоких напряжениях поля. Можно разделить коллоидные частицы и ионы через мембрану, проницаемую для молекул и ионов и непроницаемую для коллоидных частиц. Такой метод разделения называется диализом. Он, например, лежит в основе аппарата «искусственная почка».
Вместе с тем, коллоидные растворы находят очень широкое применение в технике, медицине и сельском хозяйстве. Многие лекарственные вещества, пищевые продукты, парфюмерные товары, средства борьбы с сельскохозяйственными вредителями и сорняками применяются в коллоидном состоянии. В коллоидном состоянии находятся многие составные части живых организмов: кровь, лимфа, внутриклеточная жидкость. Поэтому для лечения некоторых болезней широко используется введение в организм лекарств методом электрофореза.
Таким образом, в коллоидном состоянии могут находиться многие вещества. Электрический заряд и гидратная (сольватная) оболочка коллоидных частиц обеспечивает устойчивость коллоидных систем, а также придает им особые электрические и кинетические свойства. Снятие электрического заряда и удаление гидратной оболочки частиц приводит к разрушению коллоидных систем.
