
Vnutrennie_bolezni_6-e_izd_Makolkin
.pdf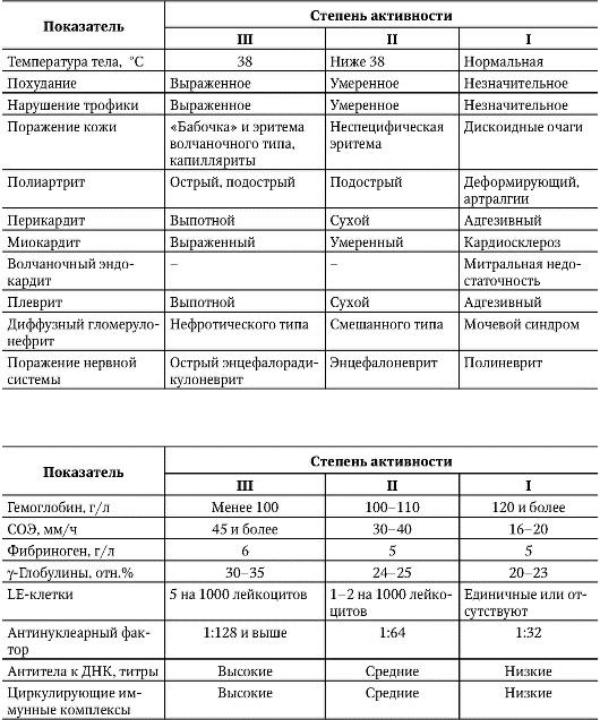
Таблица 7-1. Критерии активности патологического процесса при системной красной волчанке (Насонова В.А., 1989)
Окончание табл. 7-1
Диагностика
В случаях классического течения СКВ-диагностика проста и основана на обнаружении «бабочки», рецидивирующего полиартрита и полисерозита, составляющих клиническую диагностическую триаду, дополняемую присутствием LE-клеток или АНФ в диагностических титрах. Вспомогательное значение имеет молодой возраст больных, связь с родами, абортами, началом менструальной функции, инсоляцией и инфекционными заболеваниями. Значительно сложнее установить диагноз в других случаях, особенно если вышеперечисленные классические диагностические признаки
721
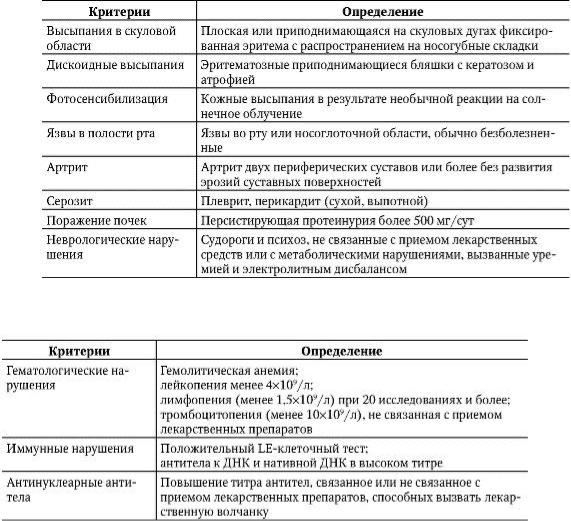
отсутствуют. В этой ситуации помогают диагностические критерии, разработанные Американской ревматологической ассоциацией (АРА) в 1982 г. и пересмотренные в 1992 г. (табл. 7-2).
Таблица 7-2. Диагностические критерии системной красной волчанки (АРА)
Окончание табл. 7-2
Диагноз достоверен при обнаружении соответствия четырем критериям или более. Если присутствует менее четырех критериев, то диагноз СКВ сомнителен, и требуется динамическое наблюдение за больным. Такой подход имеет четкое обоснование: он предостерегает от назначения таким больным глюкокортикоидов, так как с такими же симптомами могут протекать и другие заболевания (в том числе паранеопластический синдром), при которых их применение противопоказано.
Дифференциальная диагностика
СКВ следует дифференцировать с целым рядом заболеваний. Насколько велик перечень органов и систем, вовлекаемых в патологический процесс при СКВ, настолько же обширен и список заболеваний, которые можно ошибочно диагностировать у больного. СКВ может в большей степени имитировать различные патологические состояния. Это особенно часто случается в дебюте заболевания, а также при доминирующем поражении одного-двух органов (систем). Например, обнаружение в начале болезни поражения плевры можно расценить как плеврит туберкулезной этиологии; миокардит можно
722
трактовать как ревматический или неспецифический. Особенно много ошибок допускают, если СКВ дебютирует гломерулонефритом. В подобных случаях ставят диагноз только гломерулонефрита.
СКВ чаще всего приходится дифференцировать от ОРЛ (ревматизмом), ИЭ, хронического активного гепатита (ХАГ), геморрагических диатезов (тромбоцитопенической пурпуры) и других болезней из группы ДЗСТ.
Необходимость дифференциальной диагностики с ревматизмом возникает, как правило, у подростков и юношей в дебюте заболевания - при возникновении артрита и лихорадки. Ревматический артрит отличается от волчаночного большей остротой симптомов, преимущественным поражением крупных суставов и скоротечностью. Не следует придавать дифференциально-диагностического значения предшествующему инфекционному поражению (ангине), поскольку оно может послужить неспецифическим фактором, вызывающим развитие клинических признаков СКВ. Диагноз ревматизма становится достоверным с момента возникновения признаков поражения сердца (ревмокардит). Последующее динамическое наблюдение позволяет обнаружить формирующийся порок сердца, тогда как при СКВ, если и формируется недостаточность митрального клапана, то она выражена незначительно и не сопровождается отчетливыми гемодинамическими нарушениями. Митральная регургитация выражена незначительно. В отличие от СКВ, в острой стадии ревматизма отмечают лейкоцитоз. АНФ не обнаруживают.
Дифференциальная диагностика между СКВ и РА затруднительна в начальной стадии болезни, что связано со сходством клинической картины: возникает симметричное поражение мелких суставов кисти, в процесс вовлекаются новые суставы, характерна утренняя скованность. Дифференциальная диагностика основана на преобладании при РА
впораженных суставах пролиферативного компонента, раннем развитии гипотрофии мышц, приводящих в движение пораженные суставы, и стойкости суставных поражений. Эрозии суставных поверхностей при СКВ отсутствуют, но служат характерным признаком РА. Высокий титр РФ характерен для РА. При СКВ его обнаруживают редко и
вневысоком титре. Исключительно сложна дифференциальная диагностика СКВ и висцеральной формы РА. Уточненная диагностика в обоих случаях не влияет на характер лечения (назначение глюкокортикоидов).
При ХАГ могут возникать системные нарушения в виде лихорадки, артрита, плеврита, кожных высыпаний и гломерулонефрита. Можно обнаружить лейкопению, тромбоцитопению, LE-клетки и АНФ. При проведении дифференциальной диагностики следует учитывать:
•ХАГ чаще развивается в среднем возрасте;
•в анамнезе у больных ХАГ есть указания на перенесенный вирусный гепатит;
•при ХАГ обнаруживают выраженные изменения структуры и функции печени
(цитолитический и холестатический синдром, признаки печеночной недостаточности, гиперспленизм, портальная гипертензия);
• при СКВ поражение печени возникает не всегда и протекает в виде гепатита легкого течения (с умеренными признаками цитолитического синдрома);
723
• при ХАГ обнаруживают различные маркеры вирусного поражения печени (противовирусные антитела и вирусный антиген).
При первичном ИЭ быстро возникает поражение сердца (недостаточность аортального или митрального клапана), а антибактериальная терапия дает отчетливый эффект. LEклетки, антитела к ДНК, АНФ, как правило, отсутствуют. При своевременном проведении бактериологического исследования обнаруживают рост патогенной микрофлоры.
При тромбоцитопенической пурпуре (идиопатической или симптоматической) отсутствуют многие синдромы, наблюдаемые при СКВ, типичные лабораторные признаки (LE-клетки, АНФ, антитела к ДНК) и лихорадка.
Наиболее сложна дифференциальная диагностика с другими заболеваниями из группы ДЗСТ. Такие состояния, как ССД и ДМ, могут иметь множество общих черт с СКВ. Это обстоятельство усугубляет возможность обнаружения при этих заболеваниях АНФ и LEклеток, хотя и в меньшем титре. Основные дифференциально-диагностические признаки - более частое и выраженное поражение внутренних органов (особенно почек) при СКВ, совершенно иной характер поражения кожи при ССД и четкий миопатический синдром при ДМ. В ряде случаев поставить правильный диагноз позволяет только длительное динамическое наблюдение за больным. Иногда на это уходит много месяцев и даже лет (особенно при хроническом течении СКВ с минимальной степенью активности).
Формулировка развернутого клинического диагноза СКВ должна учитывать все рубрики, приведенные в рабочей классификации заболевания. Диагноз должен отражать:
•характер течения болезни (острое, подострое, хроническое), а при хроническом течении (обычно - моноили олигосиндромном) следует указать ведущий клинический синдром;
•активность процесса;
•клинико-морфологическую характеристику поражения органов и систем с указанием стадии функциональной недостаточности (например, при люпус-нефрите - стадия почечной недостаточности, при миокардите - существование или отсутствие сердечной недостаточности, при поражении легких - существование или отсутствие дыхательной недостаточности и др.);
•указание на проводимое лечение (например, глюкокортикоидами);
•осложнения лечения (если они есть).
Лечение
Учитывая патогенез заболевания, больным СКВ рекомендовано комплексное патогенетическое лечение. Его задачи:
•подавление иммунного воспаления и иммунокомплексных нарушений (неконтролируемого иммунного ответа);
•предупреждение осложнений иммуносупрессивной терапии;
724
•лечение осложнений, возникающих в процессе проведения иммуносупрессивной терапии;
•воздействие на отдельные, резко выраженные синдромы;
•удаление из организма ЦИК и антител.
Прежде всего, необходимо исключить психоэмоциональные стрессы, инсоляцию, активно лечить сопутствующие инфекционные заболевания, употреблять нежирную пищу с высоким содержанием полиненасыщенных жирных кислот, кальция и витамина Д. В период обострения болезни и на фоне лечения цитостатическими препаратами необходима активная контрацепция. Не следует принимать контрацептивы с высоким содержанием эстрогенов, поскольку они вызывают обострение заболевания.
Для подавления иммунного воспаления и иммунокомплексных нарушений при лечении СКВ применяют основные иммуносупрессоры: глюкокортикоиды короткого действия, цитостатические препараты и аминохинолиновые производные. Длительность лечения, выбор препарата, а также поддерживающие дозы определяются:
•степенью активности заболевания;
•характером течения (остротой);
•обширностью вовлечения в патологический процесс внутренних органов;
•переносимостью глюкокортикоидов или цитостатиков, а также существованием или отсутствием осложнений иммуносупрессивной терапии;
•существованием противопоказаний.
В начальных стадиях болезни при минимальной активности процесса и преобладании в клинической картине поражения суставов глюкокортикоиды следует назначать в небольших дозах (преднизолон в дозе менее 10 мг/сут). Больные должны находиться на диспансерном учете, чтобы при возникновении первых признаков обострения заболевания врач мог своевременно назначить лечение глюкокортикоидами в оптимальной дозе.
При хроническом течении болезни с преимущественным поражением кожи в течение многих месяцев можно применять хлорохин (в дозе 0,25 г/сут) или гидроксихлорохин.
При возникновении признаков высокой активности и генерализации процесса с вовлечением в него внутренних органов необходимо немедленно перейти на более эффективное иммуносупрессивное лечение глюкокортикоидами: назначают преднизолон в дозе 1 мг/сут и более. Длительность приема высоких доз колеблется от 4 до 12 нед. Снижение дозы следует проводить постепенно, под тщательным клинико-лабораторным контролем. Поддерживающие дозы (по 5-10 мг/сут) больные должны принимать в течение многих лет.
Таким образом, основной метод лечения СКВ - применение глюкокортикоидов. При их использовании следует придерживаться следующих принципов:
• начинать лечение только при подтверждении диагноза СКВ (при подозрении применять эти препараты не следует);
725
•доза глюкокортикоидов должна быть достаточной для подавления активности патологического процесса;
•лечение подавляющей дозой следует проводить до достижения выраженного клинического эффекта (улучшение общего состояния, нормализация температуры тела, улучшение лабораторных показателей, положительная динамика органных изменений);
•после достижения эффекта следует постепенно переходить на поддерживающие дозы;
•обязательна профилактика осложнений лечения глюкокортикоидами. Для предупреждения побочного действия глюкокортикоидов применяют:
•препараты калия (оротовая кислота, калия хлорид, калия и магния аспарагинат);
•анаболические средства (метандиенон в дозе 5-10 мг);
•мочегонные (салуретики);
•гипотензивные препараты (ингибиторы АПФ);
•антацидные средства.
При развитии тяжелых осложнений назначают:
•антибиотики (при вторичной инфекции);
•противотуберкулезные препараты (при развитии туберкулеза, чаще - легочной локализации);
•препараты инсулина, диетическое питание (при сахарном диабете);
•противогрибковые средства (при кандидозе);
•противоязвенное лечение (при образовании стероидной язвы).
Во время лечения глюкокортикоидами возникают ситуации, когда необходимо введение экстравысоких доз преднизолона (внутривенно капельно в дозе 1000 мг в течение 30 мин на протяжении трех дней):
•резкое увеличение (всплеск) активности процесса (III степень), несмотря на, казалось бы, оптимальное лечение;
•резистентность к дозам, с помощью которых ранее достигали положительного эффекта;
•выраженные органные изменения (нефротический синдром, пневмонит, генерализованный васкулит, цереброваскулит).
Подобная пульс-терапия приостанавливает образование иммунных комплексов вследствие торможения синтеза антител к ДНК. Снижение концентрации последних, вызванное глюкокортикоидами, приводит к образованию иммунных комплексов меньших размеров (в результате диссоциации более крупных).
726
Значительное подавление активности процесса после проведения пульстерапии позволяет в дальнейшем назначать небольшие поддерживающие дозы глюкокортикоидов. Пульс-терапия наиболее эффективна у больных молодого возраста с небольшой длительностью заболевания.
Лечение глюкокортикоидами не всегда оказывается успешным, что обусловлено:
•необходимостью снижения дозы при развитии осложнений, несмотря на то, что такая терапия эффективна у конкретного больного;
•непереносимостью глюкокортикоидов;
•резистентностью к лечению глюкокортикоидами (обычно обнаруживают достаточно рано).
В подобных случаях (особенно при развитии пролиферативного или мембранозного люпус-нефрита) назначают цитостатики: циклофосфамид (ежемесячное внутривенное болюсное введение в дозе 0,5-1 г/м2 в течение не менее 6 мес, а затем - каждые 3 мес в течение 2 лет) в сочетании с преднизолоном в дозе 10-30 мг/сут. В дальнейшем можно вернуться к лечению глюкокортикоидами, так как резистентность к ним обычно исчезает.
Для лечения менее тяжелых, но резистентных к глюкокортикоидам симптомов болезни назначают азатиоприн (по 1-4 мг/кг в сутки) или метотрексат (по 15 мг/нед) и циклоспорин (в дозе менее 5 мг/кг в сутки) в сочетании с невысокими дозами преднизолона (по 10-30 мг/сут).
Критерии оценки эффективности применения цитостатиков:
•уменьшение или исчезновение клинических признаков;
•исчезновение стероидорезистентности;
•стойкое снижение активности процесса;
•предотвращение прогрессирования люпус-нефрита. Осложнения цитостатической терапии:
•лейкопения;
•анемия и тромбоцитопения;
•диспептические явления;
•инфекционные осложнения.
При снижении числа лейкоцитов менее 3,0х109/л дозу препарата следует снизить до 1 мг/кг массы тела. При дальнейшем нарастании лейкопении препарат отменяют и на 50% увеличивают дозу преднизолона.
Широкое распространение получили экстракорпоральные методы лечения - плазмаферез и гемосорбция. Они позволяют удалять из организма ЦИК, повысить чувствительность клеточных рецепторов к глюкокортикоидам и уменьшить интоксикацию. Их применяют
727
при генерализованном васкулите, тяжелом органном поражении (люпус-нефрит, пневмонит, цереброваскулит), а также при выраженных иммунных нарушениях, плохо поддающихся лечению глюкокортикоидами.
Обычно экстракорпоральные методы применяют в сочетании с пульстерапией или, при ее неэффективности, самостоятельно. Следует отметить, что при цитопеническом синдроме экстракорпоральные методы не применяют.
Больным с высоким титром антифосфолипидных антител в крови, но без клинических признаков антифосфолипидного синдрома, назначают небольшие дозы ацетилсалициловой кислоты (по 75 мг/сут). При подтвержденном антифосфолипидном синдроме, сопровождающемся клиническими признаками, применяют гепарин натрия и малые дозы ацетилсалициловой кислоты.
Для лечения мышечно-скелетных нарушений (артриты, артралгии, миалгии) и умеренно выраженного серозита можно применять обычные дозы НПВС.
Прогноз
В последние годы в связи с применением эффективных методов лечения прогноз улучшился: через 10 лет после установления диагноза выживаемость составляет 80%, а через 20 лет - 60%. У 10% больных, особенно при поражении почек (смерть наступает вследствие прогрессирования ХПН) или цереброваскулите, прогноз остается неблагоприятным.
Профилактика
Так как этиология СКВ неизвестна, первичную профилактику не проводят. Тем не менее выделяют группу риска, к которой относят, прежде всего, родственников больных, а также лиц, страдающих изолированным кожным поражением (дискоидная волчанка). Они должны избегать инсоляции, переохлаждения, не должны подвергаться прививкам, получать грязелечение и другие бальнеопроцедуры.
СИСТЕМНАЯ СКЛЕРОДЕРМИЯ
ССД - системное заболевание соединительной ткани и мелких сосудов, характеризующееся воспалением и распространенными фиброзно-склеротическими изменениями кожи и внутренних органов. Это определение болезни отражает существо ССД - фиброзную трансформацию соединительной ткани, служащей каркасом внутренних органов, составным элементом кожи и кровеносных сосудов. Безудержное развитие фиброза связано с избыточным коллагенообразованием вследствие нарушения функционирования фибробластов.
Распространенность ССД различна в разных географических зонах и этнических группах, в том числе и проживающих в одном регионе. Первичная заболеваемость колеблется от 3,7 до 19,0 случаев на 1 млн населения в год. ССД чаще регистрируют среди женщин (соотношение 5:7,1) в возрасте 30-60 лет.
728
Этиология
Причина развития болезни неизвестна. Придают значение вирусам, так как существуют косвенные свидетельства их роли в возникновении ССД: в пораженных тканях обнаружены вирусоподобные включения и повышенный титр антивирусных антител. Установлена семейно-генетическая предрасположенность к ССД, так как у родственников больных обнаруживают изменения белкового обмена в виде гипергаммаглобулинемии, синдрома Рейно, а иногда и ССД.
К неблагоприятным факторам, способствующим манифестации болезни и ее обострениям, следует отнести факторы внешней среды (длительный контакт с поливинилхлоридом, кремниевой пылью), применение лекарственных средств (блеомицин, триптофан), а также охлаждение, травмы, нарушение нейроэндокринных функций и воздействие профессиональных вредностей в виде вибрации.
Патогенез
В основе патогенеза лежит нарушение процесса взаимодействия различных клеток (эндотелиальных, гладкомышечных клеток сосудистой стенки, фибробластов, Т- и В- лимфоцитов, моноцитов, тучных клеток, эозинофилов) друг с другом и компонентами соединительнотканного матрикса. Результатом всего перечисленного служит селекция популяции фибробластов, устойчивых к апоптозу и функционирующих в автономном режиме максимальной синтетической активности, что активирует неофибриллогенез и способствует изменению гликопротеидов основного вещества соединительной ткани. В результате развиваются фиброзно-склеротические изменения соединительной ткани. Одновременно происходит дисрегуляция иммунного ответа организма на внедрение вируса, что выражается в гиперпродукции антител к собственным тканям (аутоантитела). Затем формируются иммунные комплексы, оседающие в микроциркуляторном русле и внутренних органах, что приводит к развитию иммунного воспаления. Выраженность иммунных и аутоиммунных нарушений при ССД не столь велика, как при СКВ.
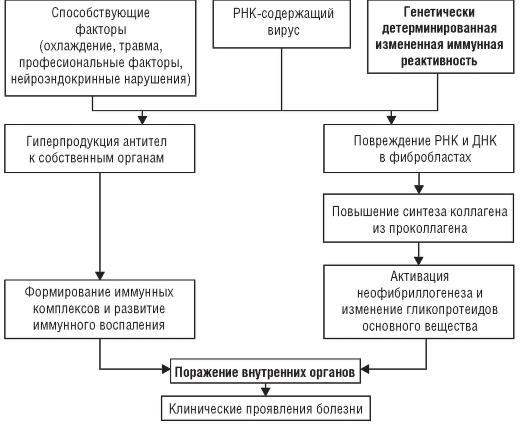
Фиброзно-склеротические изменения соединительной ткани, поражение сосудов и внутренних органов в результате иммунного воспаления обусловливают многообразие клинических признаков заболевания (рис. 7-1).
Классификация
В нашей стране принята рабочая классификация ССД, учитывающая характер течения, стадию развития болезни и клинико-морфологическую характеристику поражения органов и систем.
• Характер течения:
-быстро прогрессирующее;
-хроническое.
• Стадия:
-начальная;
-генерализованная;
729
- терминальная.
Рис. 7-1. Патогенез системной склеродермии
• Клинико-морфологическая характеристика поражения:
-кожи и периферических сосудов - плотный отек, индурация, гиперпигментация, телеангиэктазии, синдром Рейно;
-опорно-двигательного аппарата - артралгии, полиартрит, псевдоартрит, ПМ, кальциноз, остеолиз;
-сердца - миокардиодистрофия, кардиосклероз, порок сердца (чаще всего - недостаточность клапана);
-легких - интерстициальная пневмония, склероз, адгезивный плеврит;
-пищеварительной системы - эзофагит, дуоденит, спруподобный синдром;
-почек - истинная склеродермическая почка, хронический диффузный гломерулонефрит, очаговый гломерулонефрит;
-нервной системы - полиневрит, нейропсихические расстройства, вегетативные сдвиги.
• Выраженность уплотнения кожи оценивают пальпаторно по 4-балльной системе:
-0 - уплотнения нет;
730
