- •Лабораторная работа 1 Основные классы неорганических соединений
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 2 Определение молярной массы эквивалентов цинка
- •Теоретическое введение
- •Выполнение работы
- •Данные опыта и результаты расчетов Таблица 2.1
- •Давление насыщенного водяного пара при различных температурах
- •Примеры решения задач
- •Лабораторная работа 3 Определение теплоты реакции нейтрализации
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •После подстановки справочных данных из табл.Iполучаем:
- •Таким образом, тепловой эффект реакции равен –853,8 кДж, а составляет –822,2 кДж/моль.
- •Подставляем в формулу справочные данные из табл.Iи получаем:
- •Используя справочные данные табл.Iполучаем:
- •Решение. ВычисляемDh0х.Р.ИDs0х.Р.:
- •Энергию Гиббса при соответствующих температурах находим из соотношения
- •При сгорании 1 л с2н4 (н.У.) выделяется 59,06 кДж теплоты. Определить стандартную энтальпию образования этилена. (Ответ: 52,3 кДж/моль).
- •№ 3.3. А) Сожжены с образованиемH2o(г) равные объемы водорода и ацетилена, взятые при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз? (Ответ:5,2).
- •Лабораторная работа 4 Скорость химической реакции
- •Теоретическое введение
- •Выполнение работы
- •Опыт 2. Зависимость скорости реакции от температуры
- •Примеры решения задач
- •Лабораторная работа 5 Катализ
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 6 Химическое равновесие
- •Теоретическое введение
- •Выполнение работы
- •Для опыта удобно воспользоваться реакцией
- •Опыт 2. Влияние температуры на химическое равновесие
- •Примеры решения задач
- •Лабораторная работа 7 Определение концентрации раствора кислоты
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •4,37 Моль/кг
- •Лабораторная работа 8 Реакции в растворах электролитов
- •Теоретическое введение
- •Опыт 1. Сравнение химической активности кислот
- •Опыт 2. Реакции, идущие с образованием осадка
- •Опыт 3. Реакции, идущие с образованием слабого электролита
- •Опыт 4. Реакции, идущие с образованием газа
- •Опыт 5. Амфотерные электролиты
- •Примеры решения задач
- •Лабораторная работа 9 Гидролиз солей
- •Теоретическое введение
- •Выполнение работы
- •Опыт 2. Смещение равновесия гидролиза при разбавлении раствора
- •Опыт 3. Смещение равновесия гидролиза при изменении температуры
- •Опыт 4. Реакции обмена, сопровождаемые гидролизом
- •Примеры решения задач
- •Лабораторная работа 10 Коллоидные растворы
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 11 Окислительно-восстановительные реакции
- •Теоретическое введение
- •2O−2 – 4ē → o20 ½3 − окисление
- •Выполнение работы Опыт 1. Влияние среды на окислительно-восстановительные реакции
- •Опыт 3. Реакция диспропорционирования
- •Опыт 4. Внутримолекулярная реакция (групповой)
- •Примеры решения задач
- •Лабораторная работа 12 Коррозия металлов
- •Теоретическое введение
- •Выполнение работы Опыт 1. Влияние образования гальванической пары на процесс растворения металла в кислоте
- •Опыт 2. Роль защитной пленки в ослаблении коррозии
- •Примеры решения задач Электродные потенциалы. Гальванические элементы. Коррозия металлов
- •Стандартные электродные потенциалы (jo) при 25oС и электродные реакции для некоторых металлов
- •Для первого электрода:
- •Для второго электрода:
- •Лабораторная работа 13 Электролиз
- •Теоретическое введение
- •Выполнение работы Опыт 1. Электролиз раствора иодида калия
- •Опыт 2. Электролиз раствора сульфата натрия
- •Опыт 3. Электролиз раствора сульфата меди
- •Опыт 4. Электролиз с растворимым анодом
- •Примеры решения задач
- •Лабораторная работа 14 Химические свойства металлов
- •Теоретическое введение
- •Выполнение работы
- •Опыт 4. Действие щелочи на металлы
- •Лабораторная работа 15 Комплексные соединения
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 16
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 17 Жёсткость воды
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 18 Алюминий, олово, свинец
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 19 Металлы подгрупп меди и цинка
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 20 Хром
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 21 Марганец
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 22 Железо, кобальт, никель
- •Теоретическое введение
- •Выполнение работы
- •Опыт 3. Получение и свойства гидроксида никеля (II)
- •Опыт 6. Получение комплексных соединений кобальта
- •Опыт 7. Получение комплексных соединений никеля
- •Лабораторная работа 23 Галогены
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 24 Кислород. Пероксид водорода
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 25 Сера
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 26 Азот
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 27 Углерод. Кремний
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 28 Углеводороды
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 29 Спирты, альдегиды, кетоны
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 30 Органические кислоты
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 31 Распознавание высокомолекуляных материалов
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 32 Получение фенолоформальдегидных смол
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 33 Качественный анализ металлов
- •Выполнение работы
- •Лабораторная работа 34 Качественные реакции на анионы
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 35 Количественное определение железа в растворе его соли
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Библиографический список
- •Приложение а
- •Требования к оформлению отчета по лабораторной работе
- •Растворимость солей и оснований в воде
- •Периодическая система
- •Элементов д.И. Менделеева Таблица 3
Лабораторная работа 32 Получение фенолоформальдегидных смол
Цель работы: изучить способы получение полимеров.
Задание: реакцией поликонденсации получить новолачную и резольную фенолоформальдегидную смолу. Выполнить требования к результатам опытов, оформить отчет, решить задачу.
Теоретическое введение
Фенолоформальдегидные смолы получают реакцией поликонденсации фенола С6Н5ОН и формальдегида СН2О. В зависимости от соотношения компонентов и условий процесса поликонденсации образуются новолачные или резольные смолы.
Новолачные смолы образуются при небольшом избытке фенола с катализатором – соляной кислотой. Реакция идет по схеме:
|
(n + 2) |
+ |
n |
|
|
+ |
n |
Новолачная смола имеет линейное строение и при нагревании размягчается, при охлаждении затвердевает, т.е. является термопластичным полимером.
Резольные смолы получают при небольшом избытке формальдегида со щелочным катализатором. Эта смола имеет трехмерное сетчатое строение и не размягчается при нагревании, т.е. является термореактивным полимером.
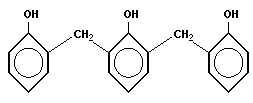
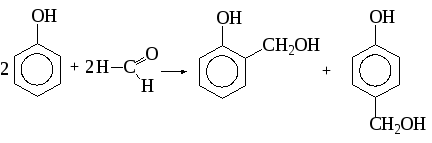
При взаимодействии фенола и формальдегида сначала образуется смесь орто- и пара-производных фенола, которые при дальнейшем взаимодействии образуют трехмерные сетчатые структуры:
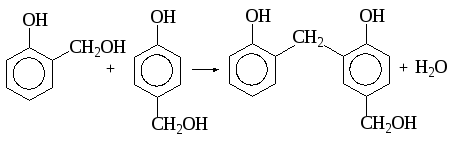
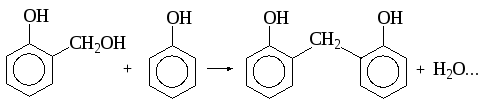
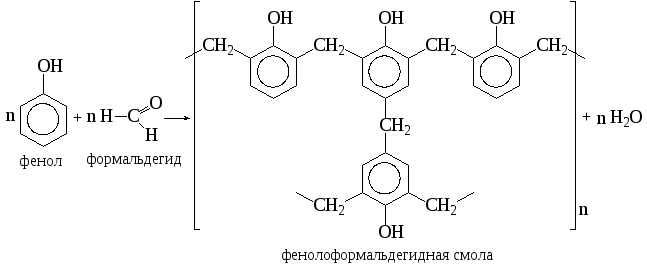
Выполнение работы
Опыт 1. Получение новолачной смолы
Поместить в пробирку 2 г кристаллического фенола, добавить туда же
3-4 мл 40 %-ного раствора формалина. Смесь взболтать до полного растворения и добавить 2-3 капли концентрированной соляной кислоты. Пробирку погрузить в водяную баню (90 оС) и время от времени перемешивать содержимое пробирки стеклянной палочкой. Когда начнется бурная реакция (через 5-10 мин), вынуть пробирку из водяной бани и погрузить в холодную воду до прекращения реакции. Затем пробирку снова поместить в водяную баню (90 оС) и держать там до разделения смеси на два слоя. После этого дать пробирке остыть и осторожно слить верхний водный слой, а смоляной продукт несколько раз промыть водой, а затем разделить его на две пробирки. В одну пробирку добавить спирт и слегка подогреть на водяной бане. Другую часть смолы нагреть на пламени спиртовки.
Требования к результатам опыта:
1. Составить схему реакции поликонденсации фенола с формальдегидом.
2. Отметить, растворяется ли смола в спирте.
3. Отметить поведение смолы при нагревании.
Опыт 2. Получение резольной смолы
В круглодонную колбу на 50 мл поместить 2,5 г фенола и 3,6 мл формалина. Смесь взболтать до полного растворения и добавить 0,5 мл 25 %-ного раствора аммиака.
Колбу с содержимым соединить с обратным холодильником, нагревать на водяной бане при 90 оС в течение 15-20 мин до отчетливого расслоения смеси (верхний – водяной слой, нижний – смоляной). Слить содержимое в фарфоровую чашку (в вытяжном шкафу!) и дать отстояться. Слить верхний водный слой. Половину полученной смолы (резита) перенести стеклянной палочкой в чистую пробирку и нагреть на пламени. Плавится ли смола? Охладить пробирку, проверить полученную смолу на растворимость в спирте.
Требования к результатам опыта:
1. Объяснить затвердевание смолы при нагревании.
2. Сделать вывод, какими свойствами – термореактивными или термопласичными обладает резольная смола.
3. Отметить растворимость смолы в спирте.