
- •Лабораторная работа 1 Основные классы неорганических соединений
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 2 Определение молярной массы эквивалентов цинка
- •Теоретическое введение
- •Выполнение работы
- •Данные опыта и результаты расчетов Таблица 2.1
- •Давление насыщенного водяного пара при различных температурах
- •Примеры решения задач
- •Лабораторная работа 3 Определение теплоты реакции нейтрализации
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •После подстановки справочных данных из табл.Iполучаем:
- •Таким образом, тепловой эффект реакции равен –853,8 кДж, а составляет –822,2 кДж/моль.
- •Подставляем в формулу справочные данные из табл.Iи получаем:
- •Используя справочные данные табл.Iполучаем:
- •Решение. ВычисляемDh0х.Р.ИDs0х.Р.:
- •Энергию Гиббса при соответствующих температурах находим из соотношения
- •При сгорании 1 л с2н4 (н.У.) выделяется 59,06 кДж теплоты. Определить стандартную энтальпию образования этилена. (Ответ: 52,3 кДж/моль).
- •№ 3.3. А) Сожжены с образованиемH2o(г) равные объемы водорода и ацетилена, взятые при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз? (Ответ:5,2).
- •Лабораторная работа 4 Скорость химической реакции
- •Теоретическое введение
- •Выполнение работы
- •Опыт 2. Зависимость скорости реакции от температуры
- •Примеры решения задач
- •Лабораторная работа 5 Катализ
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 6 Химическое равновесие
- •Теоретическое введение
- •Выполнение работы
- •Для опыта удобно воспользоваться реакцией
- •Опыт 2. Влияние температуры на химическое равновесие
- •Примеры решения задач
- •Лабораторная работа 7 Определение концентрации раствора кислоты
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •4,37 Моль/кг
- •Лабораторная работа 8 Реакции в растворах электролитов
- •Теоретическое введение
- •Опыт 1. Сравнение химической активности кислот
- •Опыт 2. Реакции, идущие с образованием осадка
- •Опыт 3. Реакции, идущие с образованием слабого электролита
- •Опыт 4. Реакции, идущие с образованием газа
- •Опыт 5. Амфотерные электролиты
- •Примеры решения задач
- •Лабораторная работа 9 Гидролиз солей
- •Теоретическое введение
- •Выполнение работы
- •Опыт 2. Смещение равновесия гидролиза при разбавлении раствора
- •Опыт 3. Смещение равновесия гидролиза при изменении температуры
- •Опыт 4. Реакции обмена, сопровождаемые гидролизом
- •Примеры решения задач
- •Лабораторная работа 10 Коллоидные растворы
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 11 Окислительно-восстановительные реакции
- •Теоретическое введение
- •2O−2 – 4ē → o20 ½3 − окисление
- •Выполнение работы Опыт 1. Влияние среды на окислительно-восстановительные реакции
- •Опыт 3. Реакция диспропорционирования
- •Опыт 4. Внутримолекулярная реакция (групповой)
- •Примеры решения задач
- •Лабораторная работа 12 Коррозия металлов
- •Теоретическое введение
- •Выполнение работы Опыт 1. Влияние образования гальванической пары на процесс растворения металла в кислоте
- •Опыт 2. Роль защитной пленки в ослаблении коррозии
- •Примеры решения задач Электродные потенциалы. Гальванические элементы. Коррозия металлов
- •Стандартные электродные потенциалы (jo) при 25oС и электродные реакции для некоторых металлов
- •Для первого электрода:
- •Для второго электрода:
- •Лабораторная работа 13 Электролиз
- •Теоретическое введение
- •Выполнение работы Опыт 1. Электролиз раствора иодида калия
- •Опыт 2. Электролиз раствора сульфата натрия
- •Опыт 3. Электролиз раствора сульфата меди
- •Опыт 4. Электролиз с растворимым анодом
- •Примеры решения задач
- •Лабораторная работа 14 Химические свойства металлов
- •Теоретическое введение
- •Выполнение работы
- •Опыт 4. Действие щелочи на металлы
- •Лабораторная работа 15 Комплексные соединения
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 16
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 17 Жёсткость воды
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 18 Алюминий, олово, свинец
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 19 Металлы подгрупп меди и цинка
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 20 Хром
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 21 Марганец
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 22 Железо, кобальт, никель
- •Теоретическое введение
- •Выполнение работы
- •Опыт 3. Получение и свойства гидроксида никеля (II)
- •Опыт 6. Получение комплексных соединений кобальта
- •Опыт 7. Получение комплексных соединений никеля
- •Лабораторная работа 23 Галогены
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 24 Кислород. Пероксид водорода
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 25 Сера
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 26 Азот
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 27 Углерод. Кремний
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 28 Углеводороды
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 29 Спирты, альдегиды, кетоны
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 30 Органические кислоты
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 31 Распознавание высокомолекуляных материалов
- •Теоретическое введение
- •Выполнение работы
- •Лабораторная работа 32 Получение фенолоформальдегидных смол
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 33 Качественный анализ металлов
- •Выполнение работы
- •Лабораторная работа 34 Качественные реакции на анионы
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Лабораторная работа 35 Количественное определение железа в растворе его соли
- •Теоретическое введение
- •Выполнение работы
- •Примеры решения задач
- •Библиографический список
- •Приложение а
- •Требования к оформлению отчета по лабораторной работе
- •Растворимость солей и оснований в воде
- •Периодическая система
- •Элементов д.И. Менделеева Таблица 3
Элементов д.И. Менделеева Таблица 3
|
Э Л Е М Е Н Т О В | ||||||
|
VA VB |
VIA VIB |
VIIA VIIB |
VIIIA VIIIB | |||
|
|
(Н)
|
Нe 2 4,0026 1s2 ГЕЛИЙ 2 |
Р Символ элемента Атомный номер
Атомная масса Распределение электронов по уровням | |||
|
N 7 14,006 2s22p3 АЗОТ 2 5 |
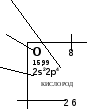
O 8 15,99 2s22p4 КИСЛОРОД 2 6 |
F 9 18,99 2s22p5 ФТОР 2 7 |
Ne 10 20,179 2s22p6 НЕОН 2 8 | |||
|
P 15 30,973 3s23p3 ФОСФОР 2 8 5 |
S 16 32,06 3s23p4 СЕРА 2 8 6 |
Cl 17 35,453 3s23p5 ХЛОР 2 8 7 |
Ar 18 39,946 3s23p6 АРГОН 2 8 8 | |||
|
23 V 3d34s250,941 ВАНАДИЙ 2 8 11 2 |
24 Cr 3d54s1 51,996 ХРОМ 2 8 13 1 |
25 Mn 3d54s2 54,9380 МАРГАНЕЦ 2 8 13 2 |
26 Fe 3d64s2 55,847 ЖЕЛЕЗО 2 8 14 2 |
27 Co 3d74s258,93 КОБАЛЬТ 2 8 15 2 |
28 Ni 3d84s2 58,70 НИКЕЛЬ 2 8 16 2 | |
|
As 33 74,9216 4s24p3 МЫШЬЯК 2 8 18 5 |
Se 34 78,96 4s24p4 СЕЛЕН 2 8 18 6 |
Br 35 79,904 4s24p5 БРОМ 2 8 18 7 |
Kr 36 83,80 4s24p6 КРИПТОН 2 8 18 8 | |||
|
41 Nb 4d45s1 92,906 НИОБИЙ 2 8 18 12 1 |
42 Mo 4d55s1 95,94 МОЛИБДЕН 2 8 18 13 1 |
43 Tc 4d55s2 [98] ТЕХНЕЦИЙ 2 8 18 13 2 |
44 Ru 4d75s1101,07 РУТЕНИЙ 2 8 18 15 1 |
45 Rh 4d85s1 102,905 РОДИЙ 2 8 18 16 1 |
46 Pd 4d105s0 106,4 ПАЛЛАДИЙ 2 8 18 18 0 | |
|
Sb 51 121,75 5s25p3 СУРЬМА 2 8 18 18 5 |
Te 52 127,60 5s25p4 ТЕЛЛУР 2 8 18 18 6 |
I 53 126,90 5s25p5 ИОД 2 8 18 18 7 |
Xe 54 131,30 5s25p6 КСЕНОН 2 8 18 18 8 | |||
|
73 Ta 5d36s2 180,94 ТАНТАЛ 2 8 18 32 11 2 |
74 W 5d46s2183,85 ВОЛЬФРАМ 2 8 18 32 12 2 |
75 Re 5d56s2 186,207 РЕНИЙ 2 8 18 32 13 2 |
76 Os 5d66s2 190,2 ОСМИЙ 2 8 18 32 14 2 |
77 Ir 5d76s2 192,22 ИРИДИЙ 2 8 18 32 15 2 |
78 Pt 5d96s1 195,08 ПЛАТИНА 2 8 18 32 17 1 | |
|
Bi 83 208,98 6s26p3 ВИСМУТ 2 8 18 32 18 5 |
Po 84 [209] 6s26p4 ПОЛОНИЙ 2 8 18 32 18 6 |
At 85 [210] 6s26p5 АСТАТ 2 8 18 32 18 7 |
Rn 86 [222] 6s26p6 РАДОН 2 8 18 32 18 2 | |||
|
105 Db 6d37s2[262] дубний 2 8 18 32 32 11 2 |
106 Sg 6d47s2 [263] сиборгий 2 8 18 32 32 12 2 |
107 Bh 6d57s2 [264] борий 2 8 18 32 32 13 2 |
108 Hs 6d67s2 [265] хассий 2 8 18 32 32 14 2 |
109 Mt 6d77s2[266] мейтнерий 2 8 18 32 32 15 2 |
110 Ds 6d87s2 [271] Дармштадтий 2 8 18 32 32 16 2 | |
Н О И Д Ы
|
65 Tb 158,9254 4f96s2 ТЕРБИЙ |
66 Dy 162,50 4f106s2ДИСПРОЗИЙ |
67 Ho 164,9304 4f116s2 ГОЛЬМИЙ |
68 Er 167,26 4f126s2 ЭРБИЙ |
69 Tm 68,9342 4f136s2 ТУЛИЙ |
70 Yb 173,04 4f146s2 ИТТЕРБИЙ |
71 Lu 174,97 4f145d16s2 ЛЮТЕЦИЙ |
Н О И Д Ы
|
97 Bk [247] 5f86d17s2 БЕРКЛИЙ |
98 Cf [251] 5f107s2 КАЛИФОРНИЙ |
99 Es [252] 5f117s2 ЭЙНШТЕЙНИЙ |
100 Fm [257] 5f127s2 ФЕРМИЙ |
101 Md [258] 5f137s2 МЕНДЕЛЕВИЙ |
102 No [259] 5f147s2 НОБЕЛИЙ |
103 Lr [260] 5f146d17s2 ЛОУРЕНСИЙ |

 аспределение
электронов по застраивающимся и
последующим застроенным подуровням
аспределение
электронов по застраивающимся и
последующим застроенным подуровням