- •Тема 1. Лабораторное оборудование
- •Экспериментальная часть Лабораторная работа. Химическая посуда и оборудование
- •Методика работы
- •Тема 2. Обработка результатов экспериментов Основные определения и термины
- •2.1. Построение и содержание отчета
- •2.2. Правила построения таблиц
- •2.3. Графическое изображение экспериментальных данных
- •Тема 3. Численное выражение состава раствора Основные определения и термины
- •Вопросы для самостоятельной подготовки и контроля
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Тема 4. Индикаторы и титрование Основные определения и термины
- •Экспериментальная часть Лабораторная работа 4.1. Определение активной кислотности растворов по изменению окраски индикаторов
- •Методика работы
- •Лабораторная работа 4.2. Определение концентрации раствора щелочи титрованием
- •Методика работы
- •Лабораторная работа 4.3. Определение концентрации раствора кислоты титрованием
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 5. Химическая кинетика и равновесие Основные определения и термины
- •Экспериментальная часть Лабораторная работа 5.1. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •Методика работы
- •Результаты опытов
- •Лабораторная работа 5.2. Зависимость скорости реакции от температуры
- •Методика работы
- •Лабораторная работа 5.3. Влияние концентрации реагирующих веществ на химическое равновесие
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 6. Буферные растворы Основные определения и термины
- •Экспериментальная часть Лабораторная работа 6.1. Приготовление буферных смесей
- •Методика работы
- •Лабораторная работа 6.2. Влияние разбавления на рН буферного раствора
- •Методика работы
- •Лабораторная работа 6.3. Влияние кислоты и щелочи на рН буферного раствора
- •Методика работы
- •Лабораторная работа 6.4. Определение буферной емкости раствора
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 7. Потенциометрия Основные определения и термины
- •Экспериментальная часть Лабораторная работа 7.1. Определение рН с использованием двойной хингидронной цепи
- •Методика работы
- •Лабораторная работа 7.2. Измерение электродного потенциала окислительно-восстановительного электрода
- •Методика работы
- •Лабораторная работа 7.3. Потенциометрическое титрование
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 8. Кондуктометрия Основные определения и термины
- •Экспериментальная часть Лабораторная работа 8.1. Кондуктометрическое определение электрической проводимости растворов слабых электролитов
- •Методика работы
- •Лабораторная работа 8.2. Кондуктометрическое определение проводимости растворов сильных электролитов
- •Методика работы
- •Лабораторная работа 8.3. Кондуктометрическое титрование
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 9. Физико-химия поверхностных явлений. Хроматография Основные определения и термины
- •Экспериментальная часть Лабораторная работа 9.1. Определение поверхностного натяжения
- •Методика работы
- •Лабораторная работа 9.2. Измерение поверхностного натяжения растворов пав сталагмометрическим методом
- •Методика работы
- •Лабораторная работа 9.3. Влияние растворителя на адсорбцию
- •Методика работы
- •Лабораторная работа 9.4. Адсорбция электролитов, красителей и золей углем
- •Методика работы
- •Лабораторная работа 9.5. Хроматографическое разделение ионов железа, меди и кобальта
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 10. Получение и очистка коллоидных систем Основные определения и термины
- •Экспериментальная часть Лабораторная работа. Получение золей
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 11. Получение и использование эмульсий Основные определения и термины
- •Экспериментальная часть Лабораторная работа. Получение и обращение фаз эмульсий
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Список рекомендуемой литературы
- •Приложения
- •1. Плотность растворов сильных кислот и щелочей
- •2. Интервалы перехода окраски некоторых индикаторов
- •3. Удельная электрическая проводимость , См/м,
- •4. Предельная эквивалентная электрическая проводимость
- •5. Константы диссоциации слабых кислот и оснований
- •6. Стандартные электродные потенциалы
- •7. Буферные ряды
- •8. Поверхностное натяжение и плотность воды
- •9. Физико-химические свойства
- •Оглавление
- •428015 Чебоксары, Московский просп., 15
Вопросы для самостоятельной подготовки и контроля
1. Укажите причину возникновения скачка потенциала на границе металл – раствор.
2. Что понимают под электродным потенциалом? Относительно какого электрода его измеряют?
3. Какую роль выполняют стандартные электроды сравнения? Назовите типы электродов.
4. Что такое ЭДС гальванического элемента? На чем основан компенсационный метод измерения ЭДС?
5. Какие электроды называют окислительно-восстанови-тельными?
6. Что такое окислительно-восстановительный потенциал?
7. Редокс-потенциал. Какие факторы влияют на его значение?
8. Хингидронный электрод. Приведите электрохимическую схему окислительно-восстановительной реакции, протекающей при его работе. Для каких измерений он используется?
9. В чем сущность потенциометрического метода определения рН?
10. Какие индикаторные электроды применяют для определения рН?
11. В чем преимущества стеклянного электрода? Какова его конструкция?
12. В чем заключается потенциометрическое титрование?
13. Как строятся интегральная и дифференциальная кривые потенциометрического титрования?
Тема 8. Кондуктометрия Основные определения и термины
Метод измерения электрической проводимости, иначе называемый кондуктометрией, относится к числу наиболее распространенных и точных способов изучения свойств растворов электролитов.
Электрическая проводимость растворов электролитов – это их способность проводить электрический ток под действием внешнего электрического поля. Она обеспечивается за счет потоков миграции ионов, присутствующих в данном растворе. Электрическая проводимость L представляет собой величину, обратную сопротивлению проводника R:
L = 1/R . (8.1)
В Международной системе единиц (СИ) единицей электрической проводимости является сименс (См). Сименс равен электрической проводимости проводника сопротивлением в 1 Ом (1 См = 1 Ом –1).
Как и для обычных металлических проводников, сопротивление растворов рассчитывается по формуле
![]() ,
(8.2)
,
(8.2)
где – удельное электрическое сопротивление; Ом·м (очевидно, что если l = 1м и S = 1м2, то R = ); l – длина проводника (расстояние между электродами), м; S – площадь поперечного сечения проводника (для растворов – площадь электродов), м2.
Подставив в уравнение (8.1) значение R из уравнения (8.2), получим
![]() , (8.3)
, (8.3)
где 1/ – удельная электрическая проводимость, величина, обратная удельному сопротивлению. Обозначается она буквой . С учетом этого обозначения уравнение (8.3) примет вид
![]() . (8.4)
. (8.4)
Если S = 1 м2, l = 1 м, то L =χ.
Удельная электрическая проводимость раствора электролита – это электрическая проводимость объема раствора, заключенного между двумя параллельными инертными электродами, имеющими площадь по 1 м2 и расположенными на расстоянии 1 м друг от друга. Она характеризует электрическую проводимость 1 м3 раствора, ее единицей является См/м. Удельная электрическая проводимость растворов электролитов зависит от природы электролита и растворителя, концентрации, температуры и других факторов.
Для однозначной характеристики проводящей способности растворов электролитов обычно пользуются значениями эквивалентной и молярной m электрических проводимостей.
Эквивалентная электрическая проводимость представляет собой проводимость раствора, помещенного между двумя параллельными электродами, расположенными на расстоянии 1 метра друг от друга, имеющими такую площадь, что объем раствора между ними содержит 1 моль эквивалента вещества, т.е. молярную массу эквивалента вещества (в случае молярной электрической проводимости m – 1 моль растворенного вещества).
Эквивалентная электрическая проводимость выражается через удельную проводимость :
![]() (8.5)
(8.5)
где V – объем разбавленного раствора, м3, в котором содержится 1 моль эквивалента растворенного вещества, м3/моль; С – молярная концентрация эквивалентов электролита, моль/м3 (1 моль/л = = 103 моль/м3).
В соответствии с представленными определениями и соотношением (8.5) единицей эквивалентной электрической проводимости в СИ является Смм2/моль.
В реальных системах эквивалентная электрическая проводимость зависит от концентрации и разбавления. С разбавлением раствора (уменьшением концентрации) эквивалентная электрическая проводимость увеличивается, достигая при бесконечно большом разбавлении (при С 0) максимального и постоянного для каждого электролита значения. Это значение называется эквивалентной электрической проводимостью при бесконечном (предельном) разбавлении и обозначается или .
В бесконечно разбавленном растворе диссоциация электролита полная (степень диссоциации = 1), ионы значительно удалены друг от друга. Взаимодействие между ионами отсутствует, они движутся независимо в электрическом поле. Поэтому эквивалентная электрическая проводимость при бесконечном разбавлении равна сумме предельных подвижностей ионов:
![]() (8.6)
(8.6)
где + и – – предельные подвижности (или эквивалентные электрические проводимости) катиона и аниона:
![]() (8.7)
(8.7)
где u+ и u– – абсолютные скорости движения ионов при бесконечном разбавлении, м2/(Вс); F – постоянная Фарадея, Кл/моль; F = 96485. Абсолютной скоростью движения иона называется его скорость при единичном градиенте потенциала в 1 В/м. Формула (8.6) выражает закон Кольрауша или закон независимого движения ионов, сущность которого заключается в том, что в растворе электролита катионы и анионы переносят электрический ток независимо друг от друга. Различие в подвижности ионов используется в кондуктометрическом методе анализа. Значения предельных эквивалентных электрических проводимостей (подвижностей) некоторых ионов в водном растворе представлены в прил. 2.
П
Рис.
8.1. Графическое определение
сильных
электролитов
методом
экстрополяции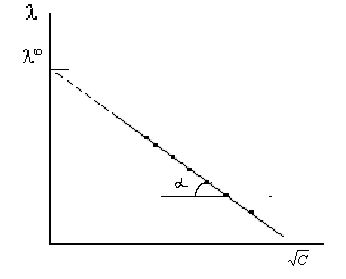
Для
определения λ∞
растворов сильных электролитов наиболее
пригоден метод экстраполяции, поскольку
в области разбавленных растворов (при
С
меньше 10–2
моль/л) λ находится в линейной зависимости
от
![]() (рис. 8.1) в соответствии с эмпирическим
уравнением Кольрауша
(рис. 8.1) в соответствии с эмпирическим
уравнением Кольрауша
![]() (8.8)
(8.8)
где
A
– постоянная, зависящая от природы
растворителя, температуры и валентного
типа электролита; А
= tg
α.Эквивалентная
электрическая проводимость сильных
электролитов описывается уравнением
(8.8) в большем интервале концентраций
(до 0,002 моль/л) по сравнению с эквивалентной
электрической проводимостью
слабых электролитов. Линейная экстраполяция
полученной прямой
= f(![]() )
на нулевую концентрацию позволяет
найти λ∞
сильного электролита (как отрезок на
ординате).
)
на нулевую концентрацию позволяет
найти λ∞
сильного электролита (как отрезок на
ординате).
Метод
экстраполяции для слабых электролитов
не пригоден, так как для них зависимость
от
![]() не является линейной. Рассчитать λ∞
слабого электролита можно по закону
Кольрауша, если известна λ∞
сильных электролитов, в состав которых
входит тот или иной ион слабого
электролита. Например, для уксусной
кислоты – типичного слабого электролита:
не является линейной. Рассчитать λ∞
слабого электролита можно по закону
Кольрауша, если известна λ∞
сильных электролитов, в состав которых
входит тот или иной ион слабого
электролита. Например, для уксусной
кислоты – типичного слабого электролита:
![]() .
.
В правой части последнего равенства находятся значения сильных электролитов, которые могут быть определены методом экстраполяции или же вычислены (по данным таблиц в справочной литературе) как сумма предельных подвижностей катионов и анионов.
Данные об электрической проводимости растворов используются для определения степени и константы диссоциации слабых электролитов. Например, степень диссоциации слабого бинарного 1–1-валентного электролита определяется по уравнению Аррениуса
![]() (8.9)
(8.9)
где – экспериментальное значение эквивалентной электрической проводимости при концентрации, к которой относится ; λ∞ – эквивалентная электрическая проводимость при бесконечном разбавлении, рассчитываемая обычно по табличным данным как сумма предельных подвижностей ионов.
Константа диссоциации слабого бинарного 1–1-валентного электролита рассчитывается по результатам измерения электрической проводимости растворов в различных концентрациях по уравнению закона разбавления Оствальда
![]() (8.10)
(8.10)
где Кс – концентрационная (классическая или реальная) константа диссоциации.
Если табличные данные о подвижностях ионов отсутствуют, значения Кс и λ∞ можно найти из экспериментальных данных по электрической проводимости растворов исследуемого электролита в нескольких концентрациях. Для этого придадим уравнению (8.10) вид
![]() (8.11)
(8.11)
и
обе части поделим на
![]() .
После небольших упрощений будем иметь
.
После небольших упрощений будем иметь
![]() (8.12)
(8.12)
Следует отметить, что для сильных электролитов
![]() ,
(8.13)
,
(8.13)
где – коэффициент электрической проводимости.
Коэффициент f принимает значения меньше единицы (так как всегда >). Значение зависит от концентрации электролита и его валентного типа.
Измерение электропроводности растворов называют кондуктометрией. Кондуктометрию используют не только для определения степени и константы диссоциации электролитов, но и для определения концентрации электролитов в растворах, их растворимости.
Кондуктометрическое титрование – это метод определения концентрации по кондуктометрическим кривым титрования. Характер кривых титрования зависит от изменения количества ионов и их подвижности.
Рассмотрим два примера кондуктометрического титрования.
1. Титрование раствора сильной кислоты раствором сильного основания. Рассмотрим титрование соляной кислоты раствором гидроксида натрия
HCl + NaOH = H2O + NaCl
или в ионной форме:
H+ + Cl + Na+ + OH = H2O + Na+ + Cl.
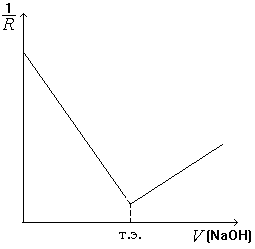
В ходе титрования концентрация ионов С1– остается постоянной, а ионы гидроксония связываются в малодиссоциирующее вещество – воду. Поэтому по мере нейтрализации проводимость раствора уменьшается, а в точке эквивалентности достигает минимума.
Добавление первой порции щелочи после точки эквивалентности приводит к резкому увеличению проводимости. Так как подвижность гидроксильных ионов меньше, чем ионов Н+, увеличение проводимости после точки эквивалентности происходит медленнее, чем ее падение до точки эквивалентности (рис. 8.2).
2. Титрование раствора слабой кислоты раствором сильного основания. Пример такого титрования – взаимодействие раствора уксусной кислоты и раствора гидроксида натрия
СН3СООН + NaOH = CH3COONa + H2O
или в ионной форме:
CH3COOH + Na+ + OH = CH3COO + Na+ + H2O.
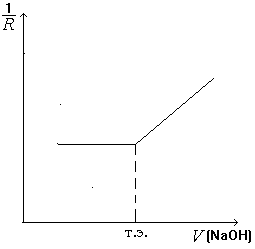
При титровании слабой кислоты щелочью изменение электропроводности происходит вследствие повышения концентрации ионов, так как вместо слабо диссоциированной кислоты образуется ее полностью диссоциированная соль. Электропроводность повышается до эквивалентной точки постепенно, а затем резко – вследствие избытка ионов металла и ОН.
Добавление к раствору после достижения точки эквивалентности первой капли раствора NaOH приводит к значительному увеличению электрической проводимости электролита (рис. 8.3).
|
V[NaOH]
Рис. 8.2. Кривая кондуктометрического титрования сильной кислоты сильным основанием |
V[NaOH]
Рис. 8.3. Кривая кондуктометрического титрования слабой кислоты сильным основанием |