
- •Тема 1. Лабораторное оборудование
- •Экспериментальная часть Лабораторная работа. Химическая посуда и оборудование
- •Методика работы
- •Тема 2. Обработка результатов экспериментов Основные определения и термины
- •2.1. Построение и содержание отчета
- •2.2. Правила построения таблиц
- •2.3. Графическое изображение экспериментальных данных
- •Тема 3. Численное выражение состава раствора Основные определения и термины
- •Вопросы для самостоятельной подготовки и контроля
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Тема 4. Индикаторы и титрование Основные определения и термины
- •Экспериментальная часть Лабораторная работа 4.1. Определение активной кислотности растворов по изменению окраски индикаторов
- •Методика работы
- •Лабораторная работа 4.2. Определение концентрации раствора щелочи титрованием
- •Методика работы
- •Лабораторная работа 4.3. Определение концентрации раствора кислоты титрованием
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 5. Химическая кинетика и равновесие Основные определения и термины
- •Экспериментальная часть Лабораторная работа 5.1. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •Методика работы
- •Результаты опытов
- •Лабораторная работа 5.2. Зависимость скорости реакции от температуры
- •Методика работы
- •Лабораторная работа 5.3. Влияние концентрации реагирующих веществ на химическое равновесие
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 6. Буферные растворы Основные определения и термины
- •Экспериментальная часть Лабораторная работа 6.1. Приготовление буферных смесей
- •Методика работы
- •Лабораторная работа 6.2. Влияние разбавления на рН буферного раствора
- •Методика работы
- •Лабораторная работа 6.3. Влияние кислоты и щелочи на рН буферного раствора
- •Методика работы
- •Лабораторная работа 6.4. Определение буферной емкости раствора
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 7. Потенциометрия Основные определения и термины
- •Экспериментальная часть Лабораторная работа 7.1. Определение рН с использованием двойной хингидронной цепи
- •Методика работы
- •Лабораторная работа 7.2. Измерение электродного потенциала окислительно-восстановительного электрода
- •Методика работы
- •Лабораторная работа 7.3. Потенциометрическое титрование
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 8. Кондуктометрия Основные определения и термины
- •Экспериментальная часть Лабораторная работа 8.1. Кондуктометрическое определение электрической проводимости растворов слабых электролитов
- •Методика работы
- •Лабораторная работа 8.2. Кондуктометрическое определение проводимости растворов сильных электролитов
- •Методика работы
- •Лабораторная работа 8.3. Кондуктометрическое титрование
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 9. Физико-химия поверхностных явлений. Хроматография Основные определения и термины
- •Экспериментальная часть Лабораторная работа 9.1. Определение поверхностного натяжения
- •Методика работы
- •Лабораторная работа 9.2. Измерение поверхностного натяжения растворов пав сталагмометрическим методом
- •Методика работы
- •Лабораторная работа 9.3. Влияние растворителя на адсорбцию
- •Методика работы
- •Лабораторная работа 9.4. Адсорбция электролитов, красителей и золей углем
- •Методика работы
- •Лабораторная работа 9.5. Хроматографическое разделение ионов железа, меди и кобальта
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 10. Получение и очистка коллоидных систем Основные определения и термины
- •Экспериментальная часть Лабораторная работа. Получение золей
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Тема 11. Получение и использование эмульсий Основные определения и термины
- •Экспериментальная часть Лабораторная работа. Получение и обращение фаз эмульсий
- •Методика работы
- •Вопросы для самостоятельной подготовки и контроля
- •Список рекомендуемой литературы
- •Приложения
- •1. Плотность растворов сильных кислот и щелочей
- •2. Интервалы перехода окраски некоторых индикаторов
- •3. Удельная электрическая проводимость , См/м,
- •4. Предельная эквивалентная электрическая проводимость
- •5. Константы диссоциации слабых кислот и оснований
- •6. Стандартные электродные потенциалы
- •7. Буферные ряды
- •8. Поверхностное натяжение и плотность воды
- •9. Физико-химические свойства
- •Оглавление
- •428015 Чебоксары, Московский просп., 15
Экспериментальная часть Лабораторная работа 7.1. Определение рН с использованием двойной хингидронной цепи
Цель работы: измерение ЭДС хингидронной цепи и определение рН заданного раствора.
Реактивы: хингидрон, раствор Вейбеля (с рН=2,04), исследуемый раствор с рН<7 (по заданию преподавателя).
Оборудование: платиновая проволока – 2 шт., химический стакан вместимостью 50 мл – 2 шт., солевой мостик, потенциометр ППТВ-1.
Методика работы
Для определения рН исследуемого раствора компенсационным методом с помощью потенциометра ППТВ-1 измеряют ЭДС двойной хингидронной цепи.
Рассмотрим методику работы на потенциометре ППТВ-1 (рис. 7.1).
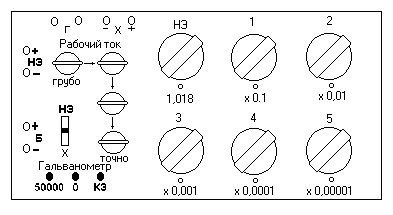
Рис. 7.1. Верхняя панель потенциометра ППТВ-1
На верхней панели потенциометра расположены рукоятки декадных реостатов 1 – 5 и переключателя нормального элемента Вестона «НЭ», а также четыре пары клемм для присоединения источника тока «Б» (аккумулятор), элемента Вестона НЭ, исследуемого элемента «Х», гальванометра «Г»; кнопки для включения в цепь гальванометра с добавочным сопротивлением «50000», без сопротивления «0» и для короткого замыкания «КЗ»; переключателя «НЭ-Х» для включения гальванометра в цепь нормального или исследуемого элемента; три ручки рычажного магазина сопротивлений и ручка реостата, применяемые для регулировки рабочего тока (от грубой до точной).
Порядок работы на потенциометре ППТВ-1
1. Подключают аккумулятор, элемент Вестона, исследуемый элемент, обращая на знаки, и гальванометр.
2. Устанавливают рабочий ток потенциометра. Для этого отмечают температуру опыта и рассчитывают ЭДС насыщенного элемента Вестона при температуре, близкой к комнатной, по формуле
Е = 1,0183 – 4,0 ∙ 10–5(t – 20 °C). (7.4)
Ставят переключатель «НЭ» на контакт, номер которого равен одной десятитысячной вольта в значении ЭДС (если Е = 1,0186, то переключатель «НЭ» ставят на контакт 6).
3. Переключатель «НЭ-Х» ставят в положение «НЭ» и поворотом ручек трехдекадного магазина сопротивления («грубо – точно») добиваются компенсации нормального элемента. Гальванометр включают кратковременным нажатием кнопок «50000» при грубой компенсации и затем «0» при более точной. Добиваются, чтобы ток в цепи гальванометра не шел. Кнопка «КЗ» служит для успокоения гальванометра.
4. Устанавливают переключатель «НЭ-Х» в положение «Х» и вращают рычаги декадных реостатов так, чтобы при нажатии на кнопку «50000» и затем «0» ток через гальванометр не шел.
Значение измеряемой ЭДС определяется суммой цифр, которые видны в окошечках панели, с учетом соответствующих множителей декад. Например, если видны цифры (7×0,1)+ +(8×0,01)+(3×0,001), то измеряемая ЭДС равна 0,783 В.
При работе необходимо соблюдать следующие правила измерения ЭДС гальванических элементов:
1. ЭДС аккумулятора в первое время после включения его в цепь может немного падать. В связи с этим измерение ЭДС целесообразно производить через несколько минут после включения аккумулятора в цепь.
2. Никогда не следует измерять ЭДС исследуемого элемента сразу же после его составления. Окончательное значение ЭДС всегда устанавливается через некоторое время (3-5 мин).
3. Во избежание поляризации гальванического элемента цепь необходимо замыкать ключом на очень короткие промежутки времени.
Для определения рН исследуемого раствора иногда применяют двойную хингидронную цепь, т.е. цепь, составленную из двух хингидронных электродов. Один из этих электродов содержит раствор с известным рН и является поэтому электродом сравнения.
Двойную хингидронную цепь можно записать следующим образом:
(–) Pt|С6Н4О2, С6Н4(ОН)2, Н+(ах)КС1Н+(аст), С6Н4(ОН)2, С6Н4О2Рt (+)
электрод определения электрод сравнения
Рассматриваемая цепь является концентрационной, так как ее электроды отличаются только количеством ионов водорода.
Двойная хингидронная цепь составляется следующим образом (рис. 7.2). В один стакан наливают раствор, рН которого известен (рНст). Обычно в качестве стандартного раствора берут смесь, состоящую из одного объема раствора НС1 концентрации 0,1 моль/л и девяти объемов раствора КС1 концентрации 0,1 моль/л. Такой раствор, именуемый раствором Вейбеля, имеет рН 2,04 при 25 оС. В другой стакан наливают исследуемый раствор, рН которого необходимо определить (рНх).
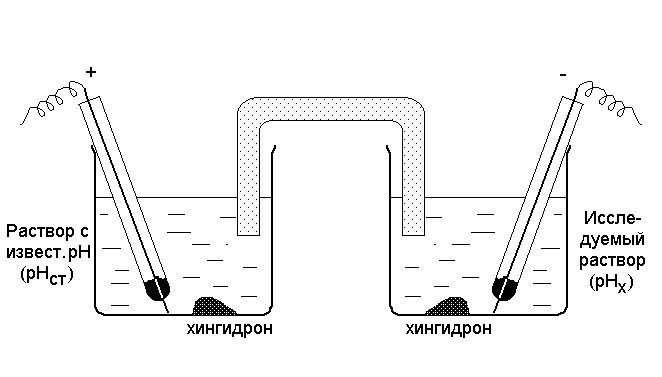
Рис. 7.2. Двойная хингидронная цепь
В оба стакана добавляют хингидрон и вставляют платиновые электроды. В целях устранения диффузионного потенциала цепь соединяется через агар-агаровый мостик с насыщенным раствором КС1.
Знаки электродов в вышеприведенной схеме цепи (рис. 7.2) указаны для случая аст>ах. Если это условие не выполняется, знаки заряда электродов в цепи будут обратными. ЭДС указанной двойной хингидронной цепи составит Е = (ст) – хг .
Подставив в это уравнение значения потенциалов хингидронных электродов, получим
![]()
![]() (7.5)
(7.5)
Отсюда
![]() (7.6)
(7.6)
С учетом того, что в качестве стандартного раствора берется раствор Вейбеля, уравнение (3.4) примет следующий вид:
![]()
![]() (7.7)
(7.7)
При исследовании растворов, в которых активность ионов Н+ больше таковой в растворе электрода сравнения, и следовательно ах>аст, ЭДС цепи составит
![]() .(7.8)
.(7.8)
Отсюда ![]() (7.9)
(7.9)
Таким образом, для определения рН исследуемого раствора необходимо измеряют ЭДС двойной хингидронной цепи компенсационным методом с помощью потенциометра ППТВ-1; вычисляют рН, пользуясь соответственно формулами (7.6) и (7.8). Сравнить полученное рН с табличным значением.
Результаты оформить в виде табл. 7.1.
Таблица 7.1
Результаты эксперимента и расчетов
|
Состав буферной смеси |
ЭДС цепи Е, В |
рН буферной системы | |
|
рассчитанное |
табличное | ||
|
|
|
|
|
