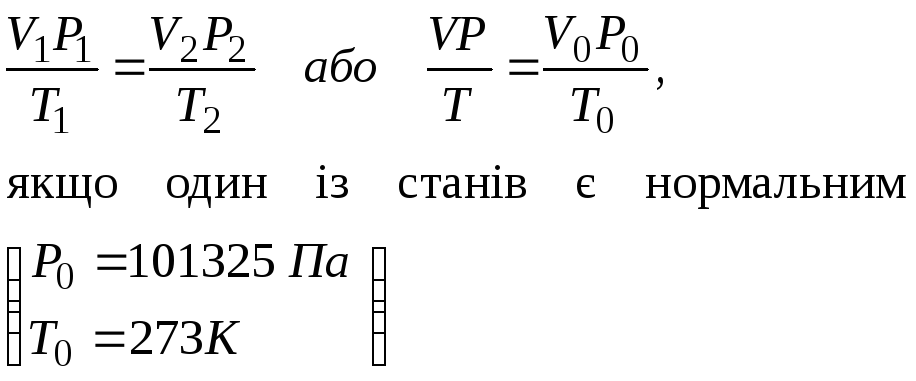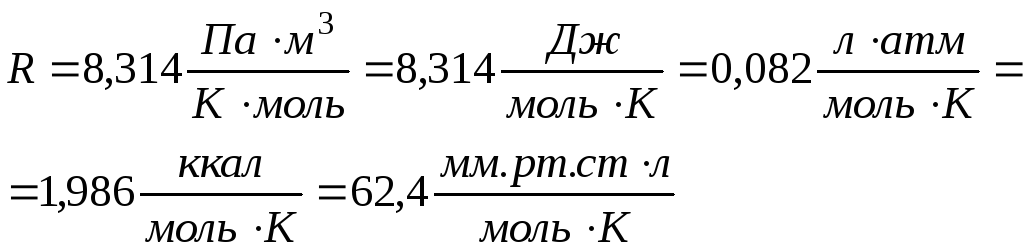- •Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Додаткова література
Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия.- М.: Химия,- 1993.- 592 с.
Общая химия / Под ред. Соколовской Е.М. и Гузея Л.С.- М.: Изд-во МГУ,- 1989.- 640 с.
Ахметов Н.С. Общая и неорганическая химия.- М.: Высш. шк.,- 2002.- 743 с.
Глинка Н.Л. Задачи и упражнения по общей химии.- Л.: Химия,- 1986.- 279 с.
Каличак Я.М. Кінжибало В.В., Котур Б.Я. та інш. «Хімія», задачі, вправи, тести.- Львів: Світ,- 2001.- 176 с.
Гольбрайх З.Е. Сборник задач и упражнений по химии.- М.: Высш. шк.,- 1984.- 224 с.
Основні поняття та закони хімії основні поняття та визначення
|
Моль |
- кількість речовини, яка містить 6,02·1023 структурних одиниць (молекул, атомів, іонів, електронів і т.і.). |
|
Молярна маса |
- маса одного моль речовини (кг/моль, г/моль)
ν= де ν – кількість речовини, моль; m – маса речовини, г; M – молярна маса, г/моль; V – об’єм газу, л; VМ - молярний об’єм газу, л/моль. |
|
Еквівалент |
- реальна або умовна частинка, яка може заміщувати, приєднувати, звільняти чи якимось іншим чином відповідати одному іону водню Н+ в обмінних реакціях або одному електрону в окисно-відновних реакціях. |
|
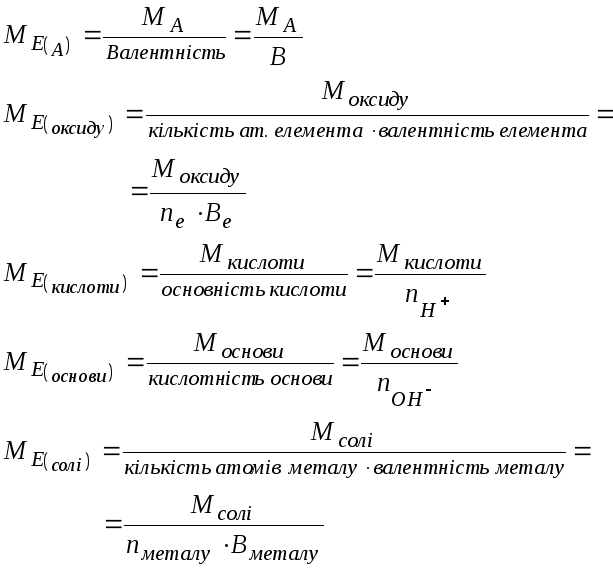
Молярні маси еквівалентів елементів та складних речовин |
|
|
Закон еквівалентів |
- маси реагуючих речовин відносяться між собою як молярні маси їхніх еквівалентів:
|
|
Закон Авогадро |
- рівні об’єми різних газів за однакових умов (температура та тиск) містять однакову кількість молекул.
|
|
Перший наслідок із закону Авогадро |
- один моль будь-якого ідеального газу (не враховуються міжмолекулярні взаємодії та розміри часточок) за певних умов (Р,Т) займає однаковий об’єм. За нормальних умов 1 моль будь-якого газу займає об’єм 22,4 л. |
|
Другий наслідок із закону Авогадро |
- відношення мас рівних об’ємів різних газів за однакових температур дорівнює відношенню їхніх молярних мас:
де
М - молярна маса газу, г/моль;
|
|
Число Авогадро (NА) |
-
число структурних частинок, що містить
у собі 1 моль речовини.
|
|
Закон Гей-Люссака |
- за сталого тиску об’єм
даної маси газу змінюється прямо
пропорційно температурі:
де V- об’єм газу; T– температура.
При постійному об’ємі:
де Р - тиск газу.
|
|
Закон Бойля-Маріотта |
- за сталої температури об’єм даної маси газу змінюється обернено пропорційно тиску:
де V-об’єм газу; P- тиск. |
|
Об’єднаний закон Бойля-Маріотта і Гей-Люссака |
де V - об’єм газу; T – температура. |
|
Рівняння Менделєєва-Клапейрона |
де v– кількість речовини газу; m – маса газу; V – об’єм газу; M – молярна маса газу; Р – тиск газу; R –універсальна газова стала.
|
|
Закон парціального тиску газів (закон Дальтона) |
- загальний тиск газової суміші дорівнює сумі парціальних тисків окремих газів, що утворюють суміш:
де Рі – парціальний тиск і – того газу. |
|
Парціальний тиск
|
- це та частина загального тиску, яка припадає на долю даного газу. |