
- •Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Контрольні завдання
101. Визначити кількість теплоти, що виділиться при згорянні 10 м3(н.у.) метану, якщо термохімічне рівняння має вигляд:
![]() .
.
Відповідь: -397459,82 кДж.
102. При згорянні 11,5 г
рідкого етилового спирту виділилось
308,71 кДж теплоти. Скласти термохімічне
рівняння реакції, в результаті якої
утворюються пари води і вуглекислий
газ. Визначити теплоту утворення
![]() .
.
Відповідь: -277,67 кДж.
103. На основі термохімічного рівняння
![]()
розрахувати об’єм кисню (н.у.), необхідний для згоряння рідкого бензолу з виділенням 313,56 кДж теплоти.
Відповідь: 16,8 л.
104. Розрахувати кількість
теплоти, що виділяється при згорянні 1
кг глюкози
![]() якщо при згорянні 1 моль глюкози з
утворенням газоподібнихСО2
и Н2О виділяється 2538,6
кДж теплоти.
якщо при згорянні 1 моль глюкози з
утворенням газоподібнихСО2
и Н2О виділяється 2538,6
кДж теплоти.
Відповідь: 14103,33 кДж.
105. На основі термохімічного рівняння
![]()
розрахувати кількість теплоти, що виділяється при гашенні 3 г вапна.
Відповідь: 35 кДж.
106. Розрахувати кількість теплоти, що поглинається при утворенні вапна з 300 кг вапняку, виходячи з рівняння
![]()
Відповідь: 532170 кДж.
107. На основі термохімічного рівняння
![]()
визначити масу вапна, при гасінні якого виділяється 35 кДж теплоти.
Відповідь: 30 г.
108. При повному згорянні етилену
![]()
виділилося 6226 кДж теплоти. Розрахувати об’єм кисню (н.у.), що вступив у реакцію.
Відповідь: 371,85 л.
109. При реакції розкладу хлорату калію
![]() кДж
кДж
утворився кисень об’ємом 4,48 л (н.у.). Яка кількість теплоти виділилася при цьому?
Відповідь: 5,95 кДж.
110. Визначити, яка кількість теплоти виділяється при реакції гідратації 200 г оксиду магнію, виходячи з рівняння
![]()
Відповідь: 176,6 кДж.
111. Визначити кількість теплоти, яка поглинається при розкладі 500 г карбонату магнію, виходячи з рівняння
![]() .
.
Відповідь: 603,9 кДж.
112. Визначити масу вапна, потрібного для реакції
![]() ,
,
якщо при цьому виділяється 116536 кДж теплоти.
Відповідь: 100 кг.
113. Визначити кількість
теплоти, яка поглинається при розкладі
506 г магнезиту
![]() ,
виходячи з термохімічного рівняння
,
виходячи з термохімічного рівняння
![]() .
.
Відповідь: 611 кДж.
114. Визначити кількість теплоти, що виділяється при гашенні 650 г повітряного вапна, виходячи з термохімічного рівняння
![]() .
.
Відповідь: 757,9 кДж.
115. Визначити кількість
теплоти , що виділяється при розкладанні
700 г природного ангідриту![]() ,
виходячи з термохімічного рівняння
,
виходячи з термохімічного рівняння
![]() .
.
Відповідь: 2026,4 кДж.
116. Визначити кількість теплоти, що виділяється при утворенні 300 г силікату кальцію, виходячи з термохімічного рівняння
![]() .
.
Відповідь: 226,6 кДж.
117. Визначити масу
вапна
![]() ,
необхідного для реакції
,
необхідного для реакції
![]() ,
,
якщо при цьому виділяється 469 кДж теплоти.
Відповідь: 300 г.
118. Визначити масу
природного ангідриту
![]() ,
якщо при реакції його розкладу
,
якщо при реакції його розкладу
![]()
поглинається 2026,4 кДж теплоти.
Відповідь: 700 г.
119. Визначити масу силікату кальцію, який утворюється за реакцією
![]()
якщо при цьому виділяється 226,6 кДж теплоти.
Відповідь: 300 г.
120. Визначити масу гашеного вапна, яке утворюється за реакцією
![]()
якщо при цьому виділяється 757,9 кДж теплоти.
Відповідь: 650 г.
121. Визначити теплоту розчинення сульфату цинку, виходячи з термохімічних рівнянь:

Відповідь: -77,57 кДж/моль.
122. Розрахувати тепловий ефект реакції відновлення оксиду заліза (II) воднем, виходячи з термохімічних рівнянь:
![]()
![]()
![]() .
.
Відповідь: +27,99 кДж.
123. Тепловий ефект якої реакції є теплотою утворення NO? Розрахувати теплоту утворення NO, виходячи з наступних термохімічних рівнянь:
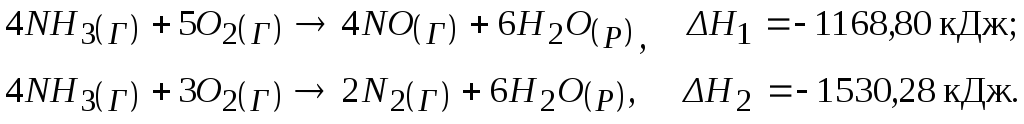
Відповідь: 90,37 кДж.
124. Визначити
теплоту гідратації
![]() ,
якщо теплоти розчинення
,
якщо теплоти розчинення![]() та
та![]() становлять
відповідно –47,7 та 31,0 кДж/моль.
становлять
відповідно –47,7 та 31,0 кДж/моль.
Відповідь: -78,7 кДж/моль.
125. Обчислити теплоту утворення озону з молекулярного кисню на підставі наступних термохімічних рівнянь:
![]()
Відповідь: 94,3 кДж/моль
126. Тепловий ефект якої реакції є теплотою утворення гідроксиду кальцію? Обчислити теплоту утворення гідроксиду кальцію, виходячи з наступних термохімічних рівнянь:
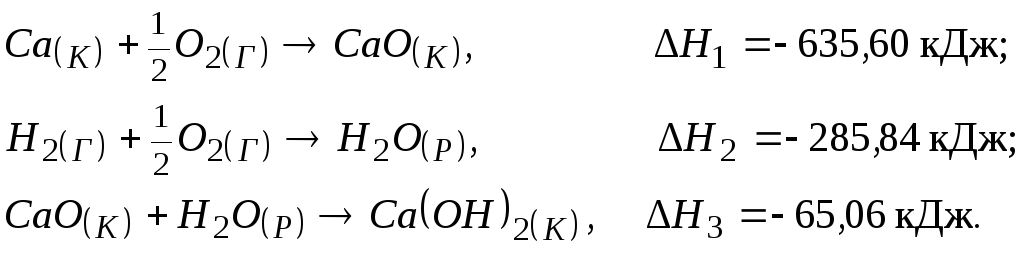
Відповідь:- 986,50 кДж.
127.
Обчислити тепловий ефект реакції
окиснення сірки в
![]() якщо відомі термохімічні рівняння:
якщо відомі термохімічні рівняння:
![]()
Відповідь: 395,8 кДж.
128.
Визначити тепловий ефект реакції
відновлення оксиду заліза
![]() оксидом вуглецю (II),
виходячи з термохімічних рівнянь:
оксидом вуглецю (II),
виходячи з термохімічних рівнянь:

Відповідь: -14,08 кДж.
129.
Обчислити теплоту розчинення
кристалогідрату
![]() якщо теплоти розчинення та гідратації
сульфату магнію становлять відповідно
–84,94 та –85,36 кДж/моль.
якщо теплоти розчинення та гідратації
сульфату магнію становлять відповідно
–84,94 та –85,36 кДж/моль.
Відповідь: 0,42 кДж/моль.
130. Тепловий ефект якої реакції є теплотою утворення оксиду азоту (I)? Визначити теплоту утворення оксиду азоту (I), якщо відомі термохімічні рівняння:
![]()
Відповідь: +82,0 кДж/моль.
131. Визначити тепловий ефект реакції перетворення аморфного кремнію в кристалічний, якщо відомі теплові ефекти процесів:
![]()
Відповідь: -16,8 кДж.
132. Визначити теплоту утворення метану, виходячи з термохімічних рівнянь:
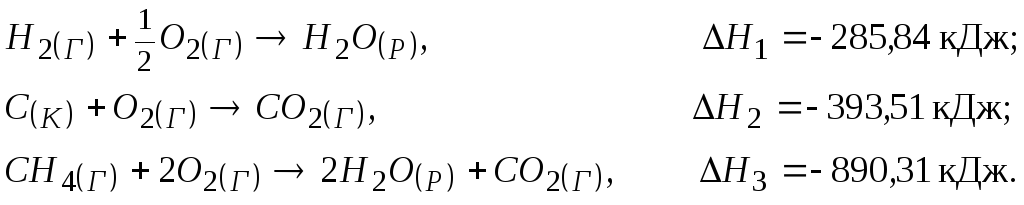
Відповідь: -74,88 кДж/моль.
133.
Розрахувати тепловий ефект реакції
відновлення
![]() воднем на підставі термохімічних
рівнянь:
воднем на підставі термохімічних
рівнянь:
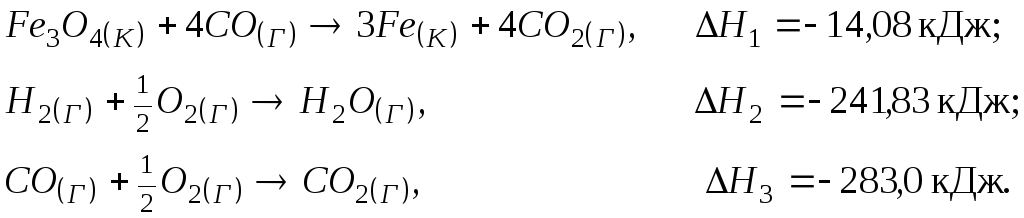
Відповідь: 150,6 кДж.
134.
Розрахувати тепловий ефект реакції
![]() ,
виходячи з термохімічних рівнянь:
,
виходячи з термохімічних рівнянь:
![]()
Відповідь: -170,1 кДж.
135. Обчислити теплоту утворення оксиду заліза (II), виходячи з термохімічних рівнянь:
![]()
Відповідь: -263,68 кДж/моль.
136.
При розчиненні 1 моль безводного карбонату
натрію в достатньо великій кількості
води виділяється 25,10 кДж теплоти, а при
розчиненні кристалогідрату
![]() поглинається 66,94 кДж теплоти. Розрахувати
теплоту гідратації карбонату натрію.
поглинається 66,94 кДж теплоти. Розрахувати
теплоту гідратації карбонату натрію.
Відповідь: -92,04 кДж/моль.
137. На підставі термохімічних рівнянь:
![]()
визначити теплоту утворення оксиду заліза (II).
Відповідь: -263,68 кДж/моль.
138. Визначити тепловий ефект процесу перетворення графіту на алмаз, виходячи з термохімічних рівнянь:
![]()
Відповідь: 1,9 кДж.
139. Виходячи з термохімічних рівнянь:

розрахувати теплоту
утворення
![]() .
.
Відповідь: -285,84 кДж/моль.
140. Розрахувати тепловий ефект реакції
![]()
виходячи з наступних термохімічних рівнянь:
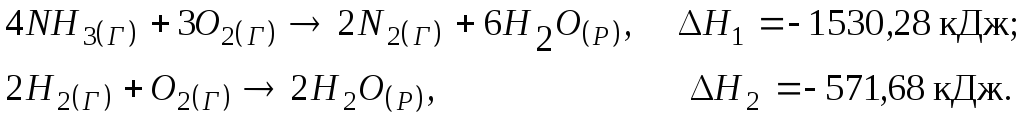
Відповідь: -92,38 кДж.
141. Визначити тепловий ефект реакції
![]() ,
,
якщо відомі теплоти
утворення
![]() і
і![]() .
.
Відповідь: 114,08 кДж.
142. Знайти тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: - 28,31 кДж.
143. Використовуючи термохімічне рівняння
![]() кДж,
кДж,
розрахувати теплоту
утворення СО, якщо відома теплота
утворення
![]() .
.
Відповідь: -110,5 кДж/моль.
144. Визначити тепловий ефект реакції
![]() ,
,
якщо відомі теплоти
утворення
![]() і
і![]() .
.
Відповідь: -808,97 кДж.
145. Знайти теплоту утворення аміаку, використовуючи термохімічне рівняння:
![]() кДж.
кДж.
Відповідь: - 46,2 кДж/моль.
146. Розрахувати тепловий ефект реакції
![]()
за відомими величинами теплот утворення вихідних речовин та продуктів реакції.
Відповідь: - 1102,6 кДж.
147. Визначити тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення речовин.
Відповідь: 95,8 кДж.
148. Знайти тепловий ефект реакції
![]()
за відомими величинами теплот утворення речовин.
Відповідь: - 2366,8 кДж.
149. Розрахувати теплоту
утворення
![]() ,
використовуючи теплоти утворення
,
використовуючи теплоти утворення![]() іСО(Г) та тепловий
ефект реакції
іСО(Г) та тепловий
ефект реакції
![]() кДж.
кДж.
Відповідь: - 62,7 кДж/моль.
150. Визначити тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення речовин.
Відповідь: -84,6 кДж.
151. Знайти
теплоту утворення
![]() ,використовуючи стандартну теплоту
утворення
,використовуючи стандартну теплоту
утворення![]() і тепловий ефект реакції
і тепловий ефект реакції
![]() кДж.
кДж.
Відповідь: -1117,9 кДж/моль.
152. Розрахувати тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення речовин.
Відповідь: -1168,8 кДж.
153. Визначити тепловий ефект реакції
![]()
за величинами стандартних теплот утворення речовин.
Відповідь: 90,37 кДж.
154. Використовуючи термохімічне рівняння
![]() кДж,
кДж,
розрахувати стандартну
теплоту утворення
![]() ,
якщо відома стандартна теплота утворення
,
якщо відома стандартна теплота утворення![]() .
.
Відповідь: - 514,5 кДж/моль.
155. Знайти тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакцій.
Відповідь: - 724,7 кДж.
156. Визначити теплоту утворення етилену, використовуючи термохімічне рівняння
![]() кДж,
кДж,
якщо відомі теплоти
утворення
![]() і
і![]() .
.
Відповідь: 52,28 кДж.
157. Розрахувати тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення речовин.
Відповідь: -538,2 кДж.
158. Використовуючи термохімічне рівняння
![]() кДж,
кДж,
знайти теплоту утворення
![]() .
.
Відповідь: - 19,74 кДж.
159. Визначити тепловий ефект реакції
![]() .
.
Відповідь: 247,3 кДж.
160. Знайти теплоту
утворення аміаку
![]() ,
використовуючи теплоту утворення
,
використовуючи теплоту утворення![]() і тепловий ефект реакції
і тепловий ефект реакції
![]() кДж.
кДж.
Відповідь: -46,19 кДж.
161.
При згорянні 1 л ацетилену (н.у.) виділяється
56,053 кДж теплоти. Обчислити теплотворну
здатність ацетилену
![]() .
.
Відповідь: 56053 кДж/м3.
162.
Визначити теплотворну здатність метану,
якщо теплота згоряння його за стандартних
умов
![]() становить -890,31 кДж/моль.
становить -890,31 кДж/моль.
Відповідь: 39746,0 кДж/м3.
163.
Розрахувати теплоту згоряння
![]() пропану
пропану![]() ,
якщо теплотворна здатність його
становить 99102,2кДж/м3.
,
якщо теплотворна здатність його
становить 99102,2кДж/м3.
Відповідь: -2219,89 кДж/моль.
164. Реакція згоряння бензолу записується термохімічним рівнянням
![]()
Обчислити
теплотворну здатність
![]() .
.
Відповідь: 41893,59 кДж/кг.
165. Визначити, скільки тепла виділиться при згорянні 5 кг вуглецю, якщо теплотворна здатність його становить 32792,5 кДж/кг.
Відповідь: 163962,5 кДж.
166.
Теплота утворення оксиду магнію
![]() дорівнює –601,24 кДж/моль. Обчислити
теплотворну здатність магнію.
дорівнює –601,24 кДж/моль. Обчислити
теплотворну здатність магнію.
Відповідь: 24742,4 кДж/кг.
167.
При згорянні 1 л етану (н.у.)
виділяється 69,64 кДж теплоти. Розрахувати
теплотворну здатність![]()
Відповідь: 69640 кДж/м3.
168.Теплота згоряння метанолу
![]() становить
становить![]() -890,31кДж/моль. Обчислити теплотворну
здатність метанолу.
-890,31кДж/моль. Обчислити теплотворну
здатність метанолу.
