
- •6.Биноминальное распределение. Распределения Пуассона и Гаусса. Флуктуации.
- •8.Распределение Максвелла по абсолютному значению скорости. Характерные скорости.
- •12.Процессы переноса в газах. Теплопередача, диффузия и трение. Взаимодиффузия в газе из различных молекул. Основные особенности явлений переноса в твердых телах и жидкостях.
- •13.Физические явления в разреженных газах. Явления в сосудах, сообщающихся через пористую перегородку.
- •16.Броуновское движение.Вращательное броуновское движение
- •17 Степени свободы молекул. Теорема о равнораспределении энергии по степеням свободы. Внутренняя энергия идеального газа.
- •18.Теплоемкость идеального газа.Расхождение теории теплоемкостей.
- •19.Внутренняя энергия тел.Теплоемкость изотропных и однородных тел.Количество теплоты.
- •21.Работа.Первое начало термодинамики.Равновесные и неравновесные процессы.
- •23. Скорость звука в газах. Уравнение Бернулли.
- •24.Тепловая машина.Кпд цикла.Холодильная Машина.Цикл Карно.Кпд Карно.
- •25.Формулировка Клаузиуса и Томсона(Кельвина) второго начала темодинамики.Первая теорема Карно.Равенство Клаузиуса.
- •26.Энтропия,Энтропия идеального.Вторая теорема Карно.Неравенство Клаузиуса.Изменени энтропии при необратимых процессах.
- •27.Формулировка второго начала темодинамики с помощью энтропии.Роль энтропии в производстве.Статистический характер.
- •28.Термодтнамическое равновесие. Эмпирические шкалы температур Международная практическая шкала Термодинамическая шкала Отрицательные абсолютные температуры
- •29.Понятие о термодинамич потенциалах.Принцип Ле-Шателье-Брауна.
- •30.Силы межмолекулярного взаимодействия.Ионная связь.Ковалентная связь.Силы Ван-дер-Ваальса.Потенциал Ленарда-Джонса.
- •31.Ураынение Ван-дер-Вальса. Изотермы газа Ван-дер-Вальса. Правило Максвела. Метостобильное состояние
- •32. Приведенное уравнения Ван-дер-Вальса. Внутрения энергия газа ванн-дер-Вальса.
- •33. Эффект Джоуля-Томсана
- •34.Переход из газообразного в жидкое. Экспериментальные изотермы.
- •35. Поведение 2-х фазной сис-мы. Ур Клапейрона-Клаузиуса
- •36.Зависимость свойств реальных газов от идеальных..
- •37.Вириальное ур состояния.
- •38.Сжижение газов. Свойство веществ при температуре близктй к 0.
- •39.Свойства и структура жидкостей жидкие кристаллы. Теплоёмкость жидкостей.
- •40.Поверхностное натяжение. Условия равновесия на границе двух жидкостей и на границе жидкость – твердое тело.
- •41.Давление под искривленной поверхностью жидкости. Капиллярные явления.
- •43.Кипение. Перегретая жидкость. Пузырьковая камера. Переохлажденный пар. Камера Вильсона.
- •44.Жидкие растворы. Растворимость. Теплота растворения.
- •45.Идеальные растворы. Закон Рауля. Закон Генри. Зависимость растворимости от температуры.
- •46. Диаграмма состояния раствора. Кипение жидких растворов.
- •48. Фазовые переходы первого и второго рода. Кристаллизация и плавление. Сублимация. Фазовые диаграммы. Полиморфизм.
- •49.Симметрия твердых тел. Кристаллические решетки. Примитивная решетка. Элементы симметрии решетки. Обозначения атомных плоскостей и направлений.
- •50.Теплоёмкость твёрдых тел. Физические процессы в кристаллах при деформациях. Дислокации.
27.Формулировка второго начала темодинамики с помощью энтропии.Роль энтропии в производстве.Статистический характер.
Пусть замкнутая система, т. е. система, изолированная от других, переходит в некотором процессе из состояния 1 в 2 . Возвратим систему с помощью обратимого процесса в состояние 1. При этом, конечно, необходимо ликвидировать изолированность системы. В результате возвращения системы в состояние 1 образовался цикл, к которому можно применить неравенство
К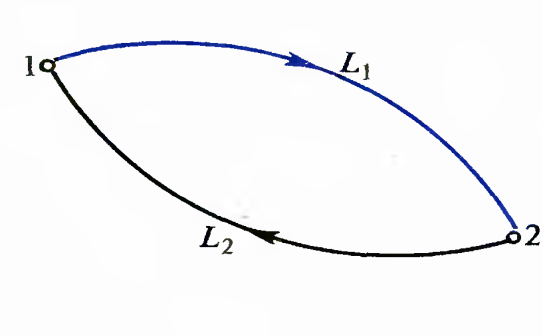 лаузиуса
лаузиуса
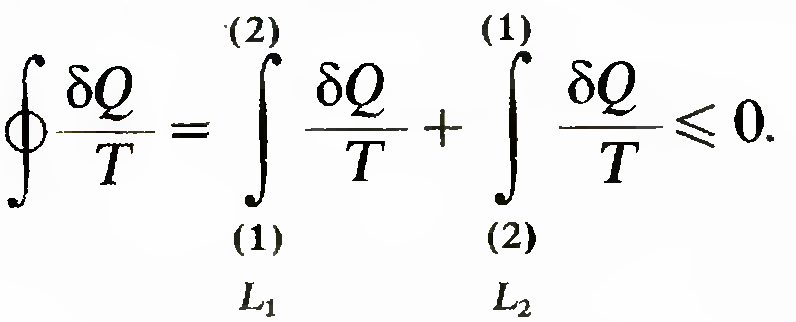
При переходе 1 ->
2 по пути L1 система была изолированной
и, следовательно, bQ в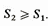 интеграле по L1 равно нулю и равен нулю
интеграл. С другой стороны, в обратимом
переходе по пути из состояния 2 в 1 в
подынтегральном выражении можно
считать, что (бQ/T) = dS. Поэтому получаем.
интеграле по L1 равно нулю и равен нулю
интеграл. С другой стороны, в обратимом
переходе по пути из состояния 2 в 1 в
подынтегральном выражении можно
считать, что (бQ/T) = dS. Поэтому получаем.
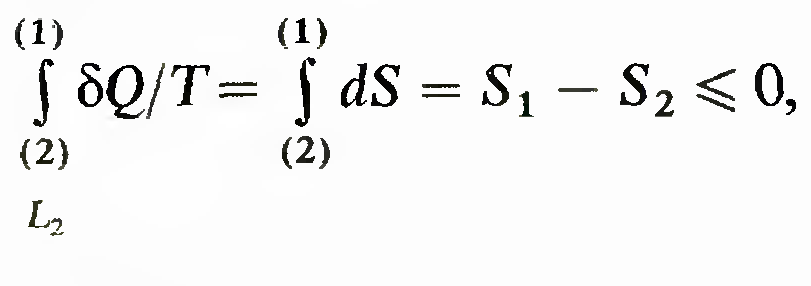 Это
означает, что при переходе замкнутой
системы из состояния 1 с энтропией S1 в
состояние 2 с энтропией S2 энтропия либо
увеличивается, либо остается неизменной.
Это и есть выражение для второго начала
термодинамики. Более кратко второе
начало термодинамики может быть
сформулировано следующим образом: в
процессах изолированной системы энтропия
не убывает. В этом утверждении существенно,
что оно относится к изолированным
системам. В неизолированных системах
энтропия может и возрастать, и убывать,
и оставаться неизменной в зависимости
от характера процесса, неизменной в
изолированной системе энтропия остается
лишь при обратимых процессах. В необратимых
же процессах она возрастает. Поскольку
в предоставленной самой себе (изолированной)
системе процессы идут, как правило,
необратимо, это означает, что практически
энтропия изолированной системы всегда
растет. Рост энтропии означает приближение
системы к состоянию термодинамического
равновесия. Таким образом, первое начало
термодинамики описывает количественные
отношения между величинами, характеризующими
систему, при различных изменениях в
состоянии системы, но ничего не говорит
о направлении этих изменений. Второе
начало указывает направление изменений
в системе, если они должны произойти,
или на отсутствие изменений, если они
не могут произойти.
Это
означает, что при переходе замкнутой
системы из состояния 1 с энтропией S1 в
состояние 2 с энтропией S2 энтропия либо
увеличивается, либо остается неизменной.
Это и есть выражение для второго начала
термодинамики. Более кратко второе
начало термодинамики может быть
сформулировано следующим образом: в
процессах изолированной системы энтропия
не убывает. В этом утверждении существенно,
что оно относится к изолированным
системам. В неизолированных системах
энтропия может и возрастать, и убывать,
и оставаться неизменной в зависимости
от характера процесса, неизменной в
изолированной системе энтропия остается
лишь при обратимых процессах. В необратимых
же процессах она возрастает. Поскольку
в предоставленной самой себе (изолированной)
системе процессы идут, как правило,
необратимо, это означает, что практически
энтропия изолированной системы всегда
растет. Рост энтропии означает приближение
системы к состоянию термодинамического
равновесия. Таким образом, первое начало
термодинамики описывает количественные
отношения между величинами, характеризующими
систему, при различных изменениях в
состоянии системы, но ничего не говорит
о направлении этих изменений. Второе
начало указывает направление изменений
в системе, если они должны произойти,
или на отсутствие изменений, если они
не могут произойти.
С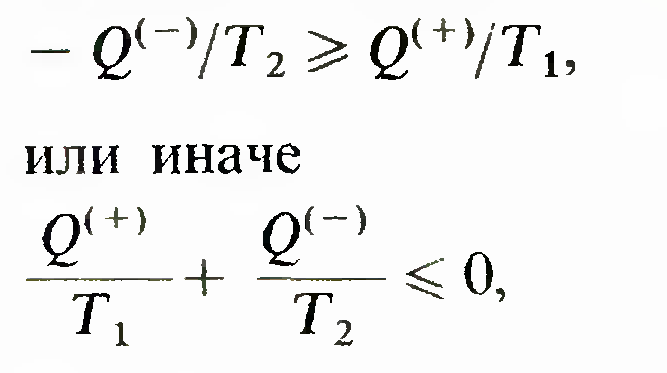 татистический
характер второго начала термодинамики.Энтропия
равна умножен- ному на постоянную
Больцмана логарифму числа микросостояний,
посредством которых реализуется данное
макросостояние . Рост энтропии в
изолированной системе означает движение
системы в направлении наиболее вероятного,
т. е. равновесного, состояния. Однако в
принципе возможны и флуктуации в этом
движении, когда на определенном отрезке
времени система движется в направлении
менее вероятных макросостояний. На этом
отрезке времени энтропия изолированной
системы убывает, а не возрастает или
остается неизменной. Таким образом,
закон неубывания энтропии в изолированной
системе не содержит в себе абсолютного
запрета убывания энтропии. Для малых
систем относительная роль флуктуации
возрастает. Следовательно, в системах
со сравнительно небольшим числом частиц
вероятность нарушения запрета на
убывание энтропии значительнее, чем в
больших. Однако в практическом смысле
закон неубывания энтропии в изолированных
системах не с чрезвычайно малым числом
частиц является абсолютным.Роль
энтропии в производстве работы.
Принцип Кельвина запрещает циклический
процесс, результатом которого было бы
превращение нацело некоторого количества
теплоты в работу в результате контакта
с одним тепловым резервуаром. Формула
для к. п. д. цикла Карно показывает, что
взятое от нагревателя количество теплоты
лишь частично может быть превращено в
работу, причем часть теплоты, превращаемая
в работу, тем больше, чем меньше температура
холодильника. Физической причиной этого
являются требования второго начала
термодинамики. Поскольку энтропия при
любых процессах в замкнутых системах
не убывает, некоторое количество теплоты
не может нацело превратиться в работу
потому, что это означало бы исчезновение
соответствующей энтропии, что противоречит
второму началу термодинамики. Поэтому
при совершении работы в холодильник
должна быть передана по крайней мере
такая же энтропия,какая была взята от
татистический
характер второго начала термодинамики.Энтропия
равна умножен- ному на постоянную
Больцмана логарифму числа микросостояний,
посредством которых реализуется данное
макросостояние . Рост энтропии в
изолированной системе означает движение
системы в направлении наиболее вероятного,
т. е. равновесного, состояния. Однако в
принципе возможны и флуктуации в этом
движении, когда на определенном отрезке
времени система движется в направлении
менее вероятных макросостояний. На этом
отрезке времени энтропия изолированной
системы убывает, а не возрастает или
остается неизменной. Таким образом,
закон неубывания энтропии в изолированной
системе не содержит в себе абсолютного
запрета убывания энтропии. Для малых
систем относительная роль флуктуации
возрастает. Следовательно, в системах
со сравнительно небольшим числом частиц
вероятность нарушения запрета на
убывание энтропии значительнее, чем в
больших. Однако в практическом смысле
закон неубывания энтропии в изолированных
системах не с чрезвычайно малым числом
частиц является абсолютным.Роль
энтропии в производстве работы.
Принцип Кельвина запрещает циклический
процесс, результатом которого было бы
превращение нацело некоторого количества
теплоты в работу в результате контакта
с одним тепловым резервуаром. Формула
для к. п. д. цикла Карно показывает, что
взятое от нагревателя количество теплоты
лишь частично может быть превращено в
работу, причем часть теплоты, превращаемая
в работу, тем больше, чем меньше температура
холодильника. Физической причиной этого
являются требования второго начала
термодинамики. Поскольку энтропия при
любых процессах в замкнутых системах
не убывает, некоторое количество теплоты
не может нацело превратиться в работу
потому, что это означало бы исчезновение
соответствующей энтропии, что противоречит
второму началу термодинамики. Поэтому
при совершении работы в холодильник
должна быть передана по крайней мере
такая же энтропия,какая была взята от
нагревателя. Энтропия, взятая в цикле Карно от нагревателя, равна Q(+)/T 1а переданная холодильнику — равна — Q(-) /Т2. На основании сказанного всегда должно быть
Именно это обстоятельство обусловливает ограниченность к. п. д. действия машины. Максимальный к. п. д. достигается в обратимой машине, поскольку в этом случае холодильнику передается минимально возможная энтропия. Для увеличения максимально возможного к. п. д. необходимо либо повышать температуру нагревателя, либо понижать температуру холодильника. Понижение температуры холодильника ограничено естественными условиями, которые присутствуют в окружающей атмосфере. Можно, конечно, искусственно охладить воздух, но для этого пришлось бы затратить работу и в конечном счете никакого увеличения к. п. д. не получилось бы. Поэтому надо считать, что для производства работы имеется некоторая минимальная заданная температура
