
- •6.Биноминальное распределение. Распределения Пуассона и Гаусса. Флуктуации.
- •8.Распределение Максвелла по абсолютному значению скорости. Характерные скорости.
- •12.Процессы переноса в газах. Теплопередача, диффузия и трение. Взаимодиффузия в газе из различных молекул. Основные особенности явлений переноса в твердых телах и жидкостях.
- •13.Физические явления в разреженных газах. Явления в сосудах, сообщающихся через пористую перегородку.
- •16.Броуновское движение.Вращательное броуновское движение
- •17 Степени свободы молекул. Теорема о равнораспределении энергии по степеням свободы. Внутренняя энергия идеального газа.
- •18.Теплоемкость идеального газа.Расхождение теории теплоемкостей.
- •19.Внутренняя энергия тел.Теплоемкость изотропных и однородных тел.Количество теплоты.
- •21.Работа.Первое начало термодинамики.Равновесные и неравновесные процессы.
- •23. Скорость звука в газах. Уравнение Бернулли.
- •24.Тепловая машина.Кпд цикла.Холодильная Машина.Цикл Карно.Кпд Карно.
- •25.Формулировка Клаузиуса и Томсона(Кельвина) второго начала темодинамики.Первая теорема Карно.Равенство Клаузиуса.
- •26.Энтропия,Энтропия идеального.Вторая теорема Карно.Неравенство Клаузиуса.Изменени энтропии при необратимых процессах.
- •27.Формулировка второго начала темодинамики с помощью энтропии.Роль энтропии в производстве.Статистический характер.
- •28.Термодтнамическое равновесие. Эмпирические шкалы температур Международная практическая шкала Термодинамическая шкала Отрицательные абсолютные температуры
- •29.Понятие о термодинамич потенциалах.Принцип Ле-Шателье-Брауна.
- •30.Силы межмолекулярного взаимодействия.Ионная связь.Ковалентная связь.Силы Ван-дер-Ваальса.Потенциал Ленарда-Джонса.
- •31.Ураынение Ван-дер-Вальса. Изотермы газа Ван-дер-Вальса. Правило Максвела. Метостобильное состояние
- •32. Приведенное уравнения Ван-дер-Вальса. Внутрения энергия газа ванн-дер-Вальса.
- •33. Эффект Джоуля-Томсана
- •34.Переход из газообразного в жидкое. Экспериментальные изотермы.
- •35. Поведение 2-х фазной сис-мы. Ур Клапейрона-Клаузиуса
- •36.Зависимость свойств реальных газов от идеальных..
- •37.Вириальное ур состояния.
- •38.Сжижение газов. Свойство веществ при температуре близктй к 0.
- •39.Свойства и структура жидкостей жидкие кристаллы. Теплоёмкость жидкостей.
- •40.Поверхностное натяжение. Условия равновесия на границе двух жидкостей и на границе жидкость – твердое тело.
- •41.Давление под искривленной поверхностью жидкости. Капиллярные явления.
- •43.Кипение. Перегретая жидкость. Пузырьковая камера. Переохлажденный пар. Камера Вильсона.
- •44.Жидкие растворы. Растворимость. Теплота растворения.
- •45.Идеальные растворы. Закон Рауля. Закон Генри. Зависимость растворимости от температуры.
- •46. Диаграмма состояния раствора. Кипение жидких растворов.
- •48. Фазовые переходы первого и второго рода. Кристаллизация и плавление. Сублимация. Фазовые диаграммы. Полиморфизм.
- •49.Симметрия твердых тел. Кристаллические решетки. Примитивная решетка. Элементы симметрии решетки. Обозначения атомных плоскостей и направлений.
- •50.Теплоёмкость твёрдых тел. Физические процессы в кристаллах при деформациях. Дислокации.
40.Поверхностное натяжение. Условия равновесия на границе двух жидкостей и на границе жидкость – твердое тело.
Свойства и структура жидкостей В твердом теле каждая частица (атом) колеблется около своего положения равновесия, причем в идеальной решетке кристалла все возможные «места» для частиц заняты. Жидкость обладает более «рыхлой» структурой, чем твердое тело, в ней имеются свободные места - «дырки», благодаря чему молекулы могут перемещаться, покидая свое место и занимая одну из соседних свободных «дырок». Тепловое движение в жидкостях носит следующий характер: каждая молекула в течение некоторого промежутка времени колеблется около определенного места равновесия. Молекула равновесия, перемещаясь на отрезок порядка размеров самих молекул. Таким образом, молекулы медленно перемещаются внутри жидкости, пребывая часть времени около определенных мест, находясь в «оседлом» состоянии.Результирующая сила, действующая на молекулу внутри жидкости со стороны других молекул, в среднем равна нулю. Иначе обстоит дело с молекулами, находящимися у поверхности жидкости. На молекулу в поверхностном слое действует с разных сторон неодинаковое число молекул. Силы, с которыми они действуют на молекулу вблизи поверхности, в среднем не будут скомпенсированы, возникнет результирующая сила, направленная внутрь жидкости. Таким образом, на каждую молекулу в поверхностном слое со стороны других молекул действует сила, направленная внутрь жидкости. На весь слой, лежащий у поверхности жидкости, действуют силы, направленные нормально к поверхности внутрь жидкости. Поверхностный слой оказывает на всю жидкость некоторое давление.Условия равновесия на границе двух жидкостей Если на поверхность одной жидкости поместить каплю другой, более легкой жидкости, то возможны два результата в зависимости от соотношения поверхностных натяжений. 1. Величина α13<α23+α12. В этом случае получим dl – элемент длины, направленный вдоль линии соприкосновения трех сред 1, 2 и 3; α13, α23 и α12 – коэффициенты поверхностного натяжения между соответствующими средами. Условием равновесия является обращение в нуль равнодействующих всех сил,
действующих на элемент dl
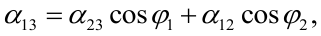


2. Если
α13>α23++α12, то капля растечется по поверхности жидкости. Условия равновесия на границе жидкость-твердое тело Если на поверхность твердого тела поместить каплю жидкости, то возможны три результата. 1. Величина α13<α23+α12. В этом случае, при условии того, что жидкость смачивает твердое тело, получим Условием равновесия является
![]()

2. Величина α13<α23+α12. В этом случае, при условии того, что жидкость не смачивает твердое тело, получим

Условием равновесия является

41.Давление под искривленной поверхностью жидкости. Капиллярные явления.
Всякая изогнутая поверхность жидкости (или пленки) оказывает на нее добавочное давление по сравнению с тем, которое испытывает жидкость с плоской поверхностью. В случае выпуклой поверхности это добавочное давление положительно, а в случае вогнутой – отрицательно. Для добавочного давления можно получить явное выражение, называемое формулой Лапласа:
 где R1 и R2 – главные
радиусы кривизны Рассматриваемой
поверхности жидкости. В случае мыльной
пленки, за счет того что у нее две
поверхности, добавочное давление
удваивается.Капиллярные
явления При
попадании жидкости в капилляр, между
молекулами жидкости и вещества, из
которого изготовлен капилляр, возникает
взаимодействие (притяжение).Высота h,
на которую поднимается вверх жидкость
в смачивающем ее цилиндрическом капилляре
радиусом r, после его соприкосновения
с жидкостью, найдем из соотношений
где R1 и R2 – главные
радиусы кривизны Рассматриваемой
поверхности жидкости. В случае мыльной
пленки, за счет того что у нее две
поверхности, добавочное давление
удваивается.Капиллярные
явления При
попадании жидкости в капилляр, между
молекулами жидкости и вещества, из
которого изготовлен капилляр, возникает
взаимодействие (притяжение).Высота h,
на которую поднимается вверх жидкость
в смачивающем ее цилиндрическом капилляре
радиусом r, после его соприкосновения
с жидкостью, найдем из соотношений


где φ – краевой угол (угол смачивания); ρ – плотность жидкости; g – ускорение свободного падения.
