
- •6.Биноминальное распределение. Распределения Пуассона и Гаусса. Флуктуации.
- •8.Распределение Максвелла по абсолютному значению скорости. Характерные скорости.
- •12.Процессы переноса в газах. Теплопередача, диффузия и трение. Взаимодиффузия в газе из различных молекул. Основные особенности явлений переноса в твердых телах и жидкостях.
- •13.Физические явления в разреженных газах. Явления в сосудах, сообщающихся через пористую перегородку.
- •16.Броуновское движение.Вращательное броуновское движение
- •17 Степени свободы молекул. Теорема о равнораспределении энергии по степеням свободы. Внутренняя энергия идеального газа.
- •18.Теплоемкость идеального газа.Расхождение теории теплоемкостей.
- •19.Внутренняя энергия тел.Теплоемкость изотропных и однородных тел.Количество теплоты.
- •21.Работа.Первое начало термодинамики.Равновесные и неравновесные процессы.
- •23. Скорость звука в газах. Уравнение Бернулли.
- •24.Тепловая машина.Кпд цикла.Холодильная Машина.Цикл Карно.Кпд Карно.
- •25.Формулировка Клаузиуса и Томсона(Кельвина) второго начала темодинамики.Первая теорема Карно.Равенство Клаузиуса.
- •26.Энтропия,Энтропия идеального.Вторая теорема Карно.Неравенство Клаузиуса.Изменени энтропии при необратимых процессах.
- •27.Формулировка второго начала темодинамики с помощью энтропии.Роль энтропии в производстве.Статистический характер.
- •28.Термодтнамическое равновесие. Эмпирические шкалы температур Международная практическая шкала Термодинамическая шкала Отрицательные абсолютные температуры
- •29.Понятие о термодинамич потенциалах.Принцип Ле-Шателье-Брауна.
- •30.Силы межмолекулярного взаимодействия.Ионная связь.Ковалентная связь.Силы Ван-дер-Ваальса.Потенциал Ленарда-Джонса.
- •31.Ураынение Ван-дер-Вальса. Изотермы газа Ван-дер-Вальса. Правило Максвела. Метостобильное состояние
- •32. Приведенное уравнения Ван-дер-Вальса. Внутрения энергия газа ванн-дер-Вальса.
- •33. Эффект Джоуля-Томсана
- •34.Переход из газообразного в жидкое. Экспериментальные изотермы.
- •35. Поведение 2-х фазной сис-мы. Ур Клапейрона-Клаузиуса
- •36.Зависимость свойств реальных газов от идеальных..
- •37.Вириальное ур состояния.
- •38.Сжижение газов. Свойство веществ при температуре близктй к 0.
- •39.Свойства и структура жидкостей жидкие кристаллы. Теплоёмкость жидкостей.
- •40.Поверхностное натяжение. Условия равновесия на границе двух жидкостей и на границе жидкость – твердое тело.
- •41.Давление под искривленной поверхностью жидкости. Капиллярные явления.
- •43.Кипение. Перегретая жидкость. Пузырьковая камера. Переохлажденный пар. Камера Вильсона.
- •44.Жидкие растворы. Растворимость. Теплота растворения.
- •45.Идеальные растворы. Закон Рауля. Закон Генри. Зависимость растворимости от температуры.
- •46. Диаграмма состояния раствора. Кипение жидких растворов.
- •48. Фазовые переходы первого и второго рода. Кристаллизация и плавление. Сублимация. Фазовые диаграммы. Полиморфизм.
- •49.Симметрия твердых тел. Кристаллические решетки. Примитивная решетка. Элементы симметрии решетки. Обозначения атомных плоскостей и направлений.
- •50.Теплоёмкость твёрдых тел. Физические процессы в кристаллах при деформациях. Дислокации.
13.Физические явления в разреженных газах. Явления в сосудах, сообщающихся через пористую перегородку.
Ультраразреженный газ
Если длина свободного пробега молекул превышает линейные размеры сосуда, в котором заключен газ, то такой газ называют ультраразреженным. В таком газе молекулы не сталкиваются друг с другом, поэтому все явления переноса протекают иначе, чем в обычном идеальном газе. Молекулы сталкиваются только со стенками сосуда.
Теплоперенос в ультраразреженном газе
Пусть в газе имеются
две пластинки
с температурами
T1
и T2.
Тогда, для элементарно приращения тепла
можно получить

где S
– площадь
пластинки, а величина
 -называется
коэффициентом
-называется
коэффициентом
теплопроводности ультраразреженного газа. Видно, что эта величина пропорциональна плотности газа: с уменьшением плотности теплопроводность газа стремится к нулю.
Эффузия Если
разделить ультраразреженный газ в
сосуде на две половины перегородкой с
отверстием, то, если размер отверстия
будет меньше длины свободного пробега,
молекулы будут проходить через отверстие
по одиночке. Не сталкиваясь друг с
другом. Такой процесс истечения газа
называется эффузией.
В случае тепловой
эффузии,
когда стенки обеих частей сосуда
находятся при различных температурах
T1
и T2,
условием равновесия будет равенство
числа молекул проходящих в единицу
времени из одной части сосуда в другую.
Следовательно, можно записать :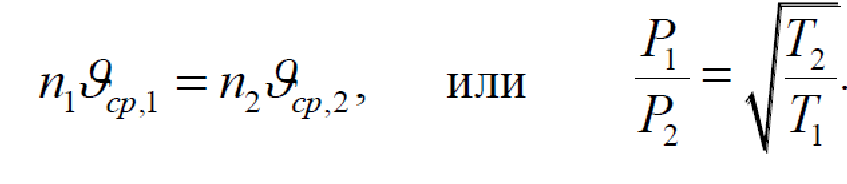
Если имеется смесь двух ультраразреженных газов при одной и той же температуре, то через малое отверстие в первую очередь будут проходить более подвижные, т.е. более легкие молекулы. Такое явление называется изотермической эффузией. Изотермическая эффузия используется, например, при разделении изотопов (легких и тяжелых) молекул одного и того же газа.
14. Распределение Больцмана. Распределение Максвелла - Больцмана. Распределение Гиббса.
Барометрическая формула
Для изменения
давления с высотой, при постоянной
температуре, можно получить следующее
выражение, называемое барометрической
формулой, ![]() ,
где m0
– масса молекулы; h
– высота. С учетом того, что
,
где m0
– масса молекулы; h
– высота. С учетом того, что ![]() получим
получим![]() ,
Барометрическая формула является
частным случаем общего распределения,
называемого распределением Больцмана.
В самом деле, учитывая, что потенциальная
энергия молекулы на высоте h
,
Барометрическая формула является
частным случаем общего распределения,
называемого распределением Больцмана.
В самом деле, учитывая, что потенциальная
энергия молекулы на высоте h
![]() и
и ![]() , получим
, получим ![]() ,
- распределение
Больцмана.
Данное распределение справедливо не
только для гравитационного поля, но и
для любого другого однородного (и не
только) поля сил. Если на идеальный газ
действует потенциальное поле (например,
сила тяжести), то распределение Максвелла
должно быть изменено с учетом распределения
Больцмана. Подставляя распределение
Больцмана в распределение Максвелла,
получим
,
- распределение
Больцмана.
Данное распределение справедливо не
только для гравитационного поля, но и
для любого другого однородного (и не
только) поля сил. Если на идеальный газ
действует потенциальное поле (например,
сила тяжести), то распределение Максвелла
должно быть изменено с учетом распределения
Больцмана. Подставляя распределение
Больцмана в распределение Максвелла,
получим  - распределение
Максвелла-Больцмана.
Распределение Максвелла-Больцмана
является частным случаем общего
распределения, называемого распределением
Гиббса
(полученного в 1901 г.):
- распределение
Максвелла-Больцмана.
Распределение Максвелла-Больцмана
является частным случаем общего
распределения, называемого распределением
Гиббса
(полученного в 1901 г.): где
gi
– статистический вес (кратность
вырождения (повторения)) рассматриваемого
состояния i
системы, имеющей энергию Ei.
Распределение Гиббса широко
где
gi
– статистический вес (кратность
вырождения (повторения)) рассматриваемого
состояния i
системы, имеющей энергию Ei.
Распределение Гиббса широко
применяется для исследования как классических, так и квантовых систем.
15.Барометрическая формула.Экспериментальное подтверждение распределения Больцмана. Атмосфера планет. Потенциальная энергия частицы массы т в поле тяготения шарообразного небесного тела равна

где М — масса тела, г — расстояние от центра тела до частицы, G — гравитационная постоянная. Атмосфера планет, в том числе и Земли, не находится в равновесном состоянии. Например, вследствие того что атмосфера Земли находится в неравновесном состоянии, ее температура не постоянна, как это должно было бы быть, а изменяется с высотой (уменьшается с увеличением высоты). Поскольку в конечном счете все системы стремятся к равновесному состоянию, то атмосфера планет постепенно рассеивается. У некоторых из небесных тел, например у Луны, атмосфера полностью исчезла, другие, например Марс, имеют очень разреженную атмосферу. Таким образом, атмосфера Луны уже достигла равновесного состояния, а атмосфера Марса
уже находится близко к достижению равновесного состояния. У Венеры атмосфера очень плотная и, следовательно,
находится в начале пути к равновесному состоянию. Для количественного рассмотрения вопроса о потере
атмосферы планетами необходимо принять во внимание распределение молекул по скоростям. Силу земного притяжения могут преодолеть лишь молекулы, скорость
которых превосходит вторую космическую. Эти молекулы находятся в «хвосте» распределения Максвелла и их относительное число незначительно. Тем не менее за значительные промежутки времени потеря молекул является чувствительной. Поскольку вторая космическая скорость
у тяжелых планет больше, чем у легких, интенсивность потери атмосферы у массивных небесных тел меньше,
чем у легких, т. е. легкие планеты теряют атмосферу быстрее, чем тяжелые. Время потери атмосферы зависит также от радиуса планеты, температуры, состава атмосферы и т. д. Экспериментальная проверка распределения Больцмана. Опыт перрена
При выводе распределения Больцмана не налагалось никаких ограничений на массу частиц. Поэтому в принципе оно применимо и для тяжелых частиц. Возьмем в качестве этих частиц, например, песчинки. Ясно, что они расположатся в некотором слое у дна сосуда. Строго говоря, это является следствием распределения Больцмана. При больших массах частиц показатель экспоненты столь быстро изменяется с высотой, что равен нулю везде за пределами слоя песка. Что касается пространства внутри слоя, то там надо принять во внимание объем песчинок. Для того чтобы тяжелые частицы не «осели на дно», а распределились в достаточно большом слое по высоте, необходимо, чтобы их потенциальная энергия была достаточно малой. Этого можно достигнуть, помещая частицы в жидкость, плотность которой лишь на немного меньше плотности материала частиц. Обозначив плотность и объем частиц р и t, а плотность жидкости — р0, видим, что сила, действующая на частицу, равна t (р — р0) g. Следовательно, потенциальная энергия такой частицы на высоте h от дна сосуда равна

Поэтому распределение концентрации этих частиц по высоте дается формулой

Чтобы эффект был достаточно хорошо заметен, частицы должны быть достаточно
малыми. Число таких частиц на разных высотах в сосуде считают с помощью
микроскопаБарометрическая
формула.
Поскольку формулой
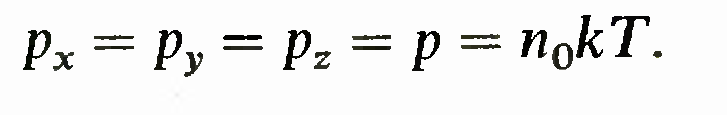
давление однозначно выражается через температуру, то распределение Больцмана

позволяет сразу, без дополнительных вычислений написать распределение давлений при тех же условиях, при которых справедлива эта формула, т. е. в условиях равновесия (T= const). Поэтому в случае изотермической атмосферы распределение давления с высотой h дается для каждой компоненты формулами.

Воздух в основном состоит из кислорода и азота. Поэтому формула для
изменения давления в нем с высотой имеет вид
 Однако
массы молекул азота и кислорода
Однако
массы молекул азота и кислорода
близки друг к другу и это изменение несущественно. Упомянуто же здесь лишь для теоретической полноты картины. Фактически смесь газов в отношении давления можно рассматривать как один газ со средней массой молекул
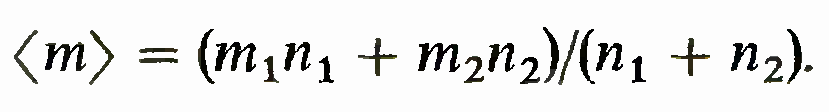
Учитывая, что [m/(kТ)] = ро(r o)/ро-> гДе Ро(ro) и Ро являются плотностью и давлением при h = 0, можно барометрическую формулу записать- в виде.

причем у поверхности Земли принимается р0 = 101,325 кПа. При этом считается, что температура с высотой не изменяется. Если выражать высоту в километрах, то барометрическую формулу удобно также представить в виде (принимая в формуле температуру равной 0°С)

