
- •2 Аминокислоты, входящие в состав белков, их строение и свойства. Биологическая
- •1. Общие структурные особенности аминокислот, входящих в состав белков
- •2. Классификация аминокислот по химическому строению радикалов
- •3. Классификация аминокислот по растворимости их радикалов в воде
- •2.Характеристика пептидной связи
- •4. Вторичная структура белков. Связи стабилизирующие вторичную структуру.
- •1. Классификации шаперонов (ш)
- •2. Роль шаперонов в фолдинге белков
- •8 . Физико-химические свойства белков. Молекулярная масса, размеры и форма, растворимость, гидротация и ионизация. Денатурация, признаки и факторы ее вызывающие.
- •10. Принципы классификации белков. Классификация по составу и биологическим функциям, примеры представителей отдельных классов.
- •11. Иммуноглобулины, классы иммуноглобулинов, особенности доменного строения и
- •13. Классификация и номенклатура ферментов, примеры
- •1. Оксидоредукпшзы
- •2.Трансферты
- •3.Гидролазы
- •4. Лиазы
- •5. Изомеразы
- •6. Лигазы (синтетазы)
- •15. Кинетика ферментативных реакций. Зависимость скорости ферментативной реакции от температуры, рН среды, концентрации ферментов и субстрата. Уравнение Михаэлиса-Ментен, Кm.
- •16. Кофакторы ферментов: ионы металлов их роль в ферментативном катализе. Коферменты как производные витаминов. Коферментные функции витаминов в6, рр, в2 на примере трансаминаз и дегидрогеназ.
- •17. Ингибирование активности ферментов: обратимое (конкурентное и неконкурентное)
- •1. Конкурентное ингибирование
- •2. Неконкурентное ингибирование
- •19. Регуляция каталитической активности ферментов ковалентной модификацией путем фосфорилирования и дефосфорилирования.
- •20. Ассоциация и диссоциация протомеров на примере протеинкиназы а и ограниченный протеолиз при активации протеолитических ферментов как способы регуляции протеолитической активности ферментов.
- •21. Изоферменты: происхождение, биологическое значение, примеры. Определение ферментов и изоферментного спектра плазмы крови с целью диагностики заболеваний.
- •22. Энзимопатии наследственные (фенилкетонурия) и приобретенные (цинга). Применение ферментов для лечения болезней.
- •23. Общая схема синтеза и распада пиримидиновых нуклеотидов. Регуляция. Оротоцидурия.
- •24. Общая схема синтеза и распада пуриновых нуклеотидов. Регуляция. Подагра.
- •27. Гибридизация нуклеиновых кислот. Денатурация и ренативация днк. Гибридизация (днк-днк, днк-рнк). Методы лабораторной диагностики, основанные на гибридизации нуклеиновых кислот.
- •29. Репликация. Принципы репликации днк. Стадии репликации. Инициация. Белки и ферменты, принимающие участие в формировании репликативной вилки.
- •30. Элонгация и терминация репликации. Ферменты. Асимметричный синтез днк. Фрагменты Оказаки. Роль днк-лигазы в формировании непрерывной и отстающей цепи.
- •31. Повреждения и репарация днк. Виды повреждений. Способы репарации. Дефекты репарационных систем и наследственные болезни.
- •32. Транскрипция. Характеристика компонентов системы синтеза рнк. Структура днк-зависимой рнк-полимеразы: роль субъединиц. Инициация процесса. Элонгация, терминация, транскрипция.
- •33. Первичный транскрипт и его процессинг. Рибозимы как пример каталитической активности нуклеиновых кислот. Биороль.
- •34. Генетический код и его свойства. Основные компоненты белоксинтезирующей системы: аминокислоты, аминоацил-т-рнк синтетазы т-рнк, рибосомы, источник энергии, белковые факторы, ферменты.
- •35. Сборка полипептидной цепи на рибосоме. Образование инициаторного комплекса. Элонгация: образование пептидной связи (реакция транспептидации). Транслокация. Транслоказа. Терминация.
- •1. Инициация
- •2. Элонгация
- •3. Терминация
- •36. Особенности синтеза и процессинга секретируемых белков (на примере коллагена и инсулина).
- •37. Биохимия питания. Основные компоненты пищи человека, их биороль, суточная потребность в них. Незаменимые компоненты пищи.
- •38. Белковое питание. Биологическая ценность белков. Азотистый баланс. Полноценность белкового питания, нормы белка в питании, белковая недостаточность.
- •39. Переваривание белков: протеазы жкт, их активация и специфичность, оптимум рН и результат действия. Образование и роль соляной кислоты в желудке. Защита клеток от действия протеаз.
- •40. Всасывание продуктов переваривания. Транспорт ак в клетки кишечника. Особенности транспорта ак в гепатоцитах. Y-глутамильный цикл. Нарушение переваривания и всасывания ак.
- •42. Минеральные вещества пищи, макро- и микроэлементы, биологическая роль. Региональные патологии, связанные с недостатком микроэлементов.
- •43. Биологические мембраны, строение, функции и общие свойства: жидкостность, поперечная ассиметрия, избирательная проницаемость.
- •1. Структура и свойства липидов мембран
- •2. Трансмембранная асимметрия липидов
- •3. Жидкостностъ мембран
- •4. Функции мембранных липидов
- •45. Механизм переноса веществ через мембраны: простая диффузия, пассивный симпорт и антипорт, активный транспорт, регулируемые каналы. Мембранные рецепторы.
- •1. Первично-активный транспорт
- •2. Вторично-активный транспорт
- •46. Эндергонические и экзергонические реакции живой клетки. Макроэргические соединения, определение, пример.
- •4. Сопряжение экзергонических и эндергонических процессов в организме
- •2. Цепь переноса электронов от nadh и fadh2 на кислород
- •50. Образование активных форм кислорода(синглетный кислород, пероксид водорода, гидроксильный радикал). Место образоваия, схемы реакций. Физиологическая роль афк.
- •51. Механизм повреждающего действия активных форм кислорода на клетки (пол, окисление белков и нуклеиновых кислот). Примеры реакций.
- •1. Строение пируватдегидрогеназного комплекса
- •2. Окислительное декарбоксилирование пирувата
- •3. Связь окислительного декарбоксилирования пирувата с цпэ
- •53. Цикл лимонной кислоты: последовательность реакций и характеристика ферментов. Роль цикла в метаболизме.
- •57. Аэробный гликолиз. Последовательность реакций до образования пирувата (аэробный гликолиз). Использование глюкозы для синтеза жиров. Энергетический эффект аэробного распада глюкозы.
- •1. Этапы аэробного гликолиза
- •2. Реакции аэробного гликолиза
- •1. Реакции анаэробного гликолиза
- •60. Гликоген, биологическое значение. Биосинтез и мобилизация гликогена. Регуляция синтеза и распада гликогена. Обмен гликогена в анте- и неонатальном периоде.
- •61. Наследственные нарушения обмена моносахаридов и дисахаридов: галактоземия, непереносимость фруктозы и дисахаридов, эссенциальная фруктоземия. Гликогенозы и агликогенозы.
- •62. Липиды. Общая характеристика. Биологическая роль. Классификация липидов. Высшие жирные кислоты, особенности строения. Полиеновые жирные кислоты. Триацилглицеролы.
- •65. Депонирование и мобилизация жиров в жировой ткани, физиологическая роль этих процессов. Роль инсулина, адреналина и глюкагона в регуляции метобализма жира.
- •67. Биосинтез жирных кислот. Основные стадии процесса. Регуляция обмена жирных кислот.
- •69. Холестерин. Пути поступления, использования и выведения из организма. Уровень холестерина в сыворотке крови. Биосинтез холестерина, его этапы. Регуляция синтеза.
- •74. Непрямое дезаминирование аминокислот. Схема процесса, субстраты, ферменты, кофакторы.
- •1. Синтез и биологическая роль серотонина
- •1. Окислительное дезаминирование
- •2. Непрямое дезаминирование (трансдезаминирование)
- •3. Неокислительное дезамитровате
- •1. Метаболизм феиилаланина
- •2. Особенности обмена тирозина в разных тканях
- •3. Заболевания, связанные с нарушением обмена фенилаланина и тирозина
- •1. Классификация гормонов по химическому строению
- •2. Классификация гормонов по биологическим функциям
- •3. Передача сигналов через рецепторы, сопряжённые с ионными каналами
- •1. Гормон роста, пролактин
- •2. Тиреотропин, лютеинизирующий гормони фолликулостимулирующий гормон
- •3. Группа гормонов, образующихсяиз проопиомеланокортина
- •1. Синтез и секреция антидиуретического гормона
- •2. Механизм действия
- •3. Несахарный диабет
- •1. Механизм действия альдостерона
- •2. Роль системы ренин-ангиотензин- альдостерон в регуляции водно-солевого обмена
- •3. Восстановление объёма крови при обезвоживании организма
- •4. Гиперальдостеронтм
- •1. Синтез и секреция птг
- •2. Роль паратгормона в регуляции обмена кальция и фосфатов
- •3. Гиперпаратиреоз
- •4. Гипопаратиреоз
- •1. Строение и синтез кальцитриола
- •2. Механизм действия кальцитриола
- •3. Рахит
- •2. Биологические функции инсулина
- •3. Механизм действия инсулина
- •1. Изменения метаболизма в печени в абсорбтивном периоде
- •2. Изменения метаболизма в адипоцитах
- •3. Изменение метаболизма в мышцах в абсорбтивном периоде
- •1. Изменения метаболизма в печени
- •2. Изменения метаболизма в жировой ткани
- •1. Инсулинзависимый сахарный диабет
- •2. Инсулинонезависимый сахарный диабет
- •1. Симптомы сахарного диабета
- •2. Острые осложнения сахарного диабета. Механизмы развития диабетической комы
- •3. Поздние осложнения сахарного диабета
- •1. Основные ферменты микросомальных электронтранспортных цепей
- •2. Функционирование цитохрома р450
- •3. Свойства системы микросомального окисления
- •1. Причины, приводящие к увеличению количества ферментов в крови
- •2. Изоферменты
- •3. Энзимодиагностика при инфаркте миокарда
- •1. Простые белки
- •1. Безмиелиновое волокно
- •2. Миелиновое волокно
24. Общая схема синтеза и распада пуриновых нуклеотидов. Регуляция. Подагра.
"Запасные" пути синтеза пуриновых нуклеотидов (реутилизация азотистых оснований и нуклеозидов)
Огромные затраты энергии для синтеза пуриновых нуклеотидов de novo не способны полностью обеспечить субстратами синтез нуклеиновых кислот в период гаструляции и раннего роста ребёнка. Потребность в большом количестве нуклеотидов привела к развитию "запасных" путей синтеза этих "дорогих" молекул. Наибольшее значение в этом процессе имеют ферменты, осуществляющие превращение пуринов в мононуклеотиды с использованием ФРДФ как донора остатка фосфорибозы.
Синтез АМФ и ГМФ из аденина и гуанина
ФРДФ-зависимое фосфорибозилирование пуринов катализируют 2 фермента.
-Аденинфосфорибозилтрансфераза, ответственная за образование АМФ.
-Гипоксантин-гуанинфосфорибозилтрансфераза, катализирующая образование ИМФ и ГМФ из гипоксантина и гуанина соответственно.
Однако в организме при любых ситуациях этот путь синтеза пуриновых нуклеотидов, получивший название "путь спасения", имеет вспомогательное значение.
Нуклеозидкиназы
Нуклеозиды, получающиеся при катаболизме нуклеиновых кислот из нуклеотидов под действием нуклеотидаз, могут повторно фосфорилироваться, образуя нуклеозид-5'-монофосфаты за счёт переноса γ-фосфатного остатка АТФ на соответствующий субстрат. У млекопитающих такой путь пополнения запасов пуриновых нуклеотидов в клетке не имеет существенного значения. Основным ферментом этой группы является аденозинкиназа, которая ускоряет реакцию:
Аденозин + АТФ → АМФ + АДФ.
Из всех способов реутилизации пуринов наиболее активна гипоксантин-гуанинфосфорибозилтрансферазная реакция, поскольку ИМФ, образующийся в этой реакции, вовлекается в синтез АМФ и ГМФ. Использование гипоксантина и гуанина по запасному пути становится жизненно важным событием в клетках, не способных к синтезу пуриновых нуклеотидов de novo.Значение аденинфосфорибозилтрансферазы в повторном использовании аденина менее существенно. По сравнению с аденозином количество аденина в клетках мало, а первый возвращается в фонд нуклеотидов с помощью аденозинкиназы.
Гиперурикемия подагры
Когда в плазме крови концентрация мочевой кислоты превышает норму, то возникает гиперурикемия. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. К характерным признакам подагры относят повторяющиеся приступы острого воспаления суставов (чаще всего мелких) - так называемого острого подагрического артрита. Заболевание может прогрессировать в хронический подагрический артрит.
Поскольку лейкоциты фагоцитируют кристаллы уратов, то причиной воспаления является разрушение лизосомальных мембран лейкоцитов кристаллами мочевой кислоты. Освободившиеся лизосомальные ферменты выходят в иитозоль и разрушают клетки, а продукты клеточного катаболизма вызывают воспаление.
Общий фонд сывороточных уратов в норме составляет ~ 1,2 г у мужчин и 0,6 г у женщин. При подагре без образования тофусов (т.е. подагрических узлов, в которых накапливаются ураты натрия и мочевая кислота) количество уратов возрастает до 2-4 г, а у пациентов с тяжёлой формой болезни, сопровождающейся ростом тофусов, может достигать 30 г.
Подагра - распространённое заболевание, в разных странах ею страдают от 0,3 до 1,7% населения. А поскольку сывороточный фонд уратов у мужчин в 2 раза больше, чем у женщин, то они и болеют в 20 раз чаще, чем женщины.
Как правило, подагра генетически детерминирована и носит семейный характер. Она вызвана нарушениями в работе ФРДФ синтетазы или ферментов "запасного" пути: гипоксантин-гуанин- или аденинфосфорибозилтрансфераз.
К другим характерным проявлениям подагры относят нефропатию, при которой наблюдают образование уратных камней в мочевыводящих путях.
25. Синтез дезоксирибонуклеотидов. Рибонуклеотидредуктазный комплекс. Биосинтез тимидиловых нуклеотидов, роль фолиевой кислоты и фолатредуктазы. Регуляция. Противоопухолевые, антивирусные и антибактериальные препараты как ингибиторы синтеза рибо- и дезоксирибонуклеотидов.
Синтез дезоксирибонуклеотидов идёт с заметной скоростью только в тех клетках, которые вступают в S-фазу клеточного цикла и готовятся к синтезу ДНК и делению. В покоящихся клетках дезоксинуклеотиды практически отсутствуют. Все дезоксинуклеотиды, кроме тимидиловых, образуются из рибонуклеотидов путём прямого восстановления ОН-группы у второго углеродного атома рибозы в составе рибонуклеозиддифосфатов до дезоксирибозы. Тимидиловые нуклеотиды синтезируются из dУМФ особым путём с участием N5,N10-метилен-Н4-фолата.
Рибонуклеотидредуктазный комплекс
Реакцию восстановления НДФ в дезоксипроизводные катализирует рибонуклеотидредук-тазный комплекс, в состав которого входят: собственно рибонуклеотидредуктаза (РНР), белок тиоредоксин и фермент тиоредоксинредуктаза, обеспечивающий регенерацию восстановленной формы тиоредоксина.
Рибонуклеотидредуктаза - олигомерный белок, состоящий из двух В1- и двух В2-субъединиц, и содержит негеминовое железо в качестве кофактора.
Непосредственным донором водорода в реакции восстановления рибозы служит низкомолекулярный белок тиоредоксин. В рабочую часть этого белка входят 2 SH-группы, которые, отдавая водород, окисляются с образованием дисульфидного мостика. Второй фермент комплекса - тиоредоксинредуктаза - катализирует гидрирование окисленного тиоредоксина с использованием NADPH.
При участии комплекса РНР образуются: dАДФ, dГДФ, dУДФ и dЦДФ, которые с помощью НДФ-киназ превращаются в дНТФ, 3 из которых (кроме дУДФ) непосредственно используются в синтезе ДНК.
дНДФ + АТФ → дНТФ + АДФ
Биосинтез тимидиловых нуклеотидов
Тимидин-5'-монофосфат (дТМФ) образуется из дУМФ в реакции, катализируемой тимиди-латсинтазой. Донором метильной группы, появляющейся в 5-положении пиримидинового кольца в молекуле дТМФ, служит кофермент тимидилатсинтазы - N5,N10-метилен-Н4-фолат. С помощью этого кофермента в молекулу дУМФ включается метиленовая группа и восстанавливается в метальную, используя 2 атома водорода от Н4-фолата.
Образование субстрата тимидилатсинтазной реакции - дУМФ осуществляется двумя путями:
-дефосфорилированием дУДФ;
-гидролитическим дезаминированием дЦМФ с помощью дЦМФ дезаминазы. дЦМФ получается при дефосфорилировании дЦДФ - одного из продуктов рибонуклеотидредуктаз-ной реакции. В организме человека это основной путь образования дУМФ.
Скорость синтеза дТМФ зависит также от количества второго субстрата тимидилатсинтазной реакции - N5,N10-метилен-Н4-фолата, пополнение запасов которого осуществляется при участии 2 ферментов: дигидрофолатредуктазы, которая с участием NADPH восстанавливает Н2-фолат в Н4-фолат, и серии гидроксиметилтрансферазы, осуществляющей перенос β-гидроксиметиленовой группы серина на Н4-фолат. У человека дТМФ образуется, главным образом, из дЦДФ.
Противоопухолевые препараты
Синтезировано
очень много аналогов дНТФ, которые
включаются ДНК полимеразами в ДНК и
ингибируют репликацию. К числу мощных
противоопухолевых препаратов принадлежит
5-фторурацил (5-FU) - аналог урацила.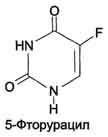
В организме по "запасным" путям 5-FU превращается в 5-Р-УМФ либо в реакции, катализируемой оротатфосфорибозилтрансферазой, либо через промежуточное образование нуклеозида и последующее фосфорилирование. Превращаясь в нуклеозиддифосфат, 5-FU может участвовать в реакции, катализируемой РНР, и восстанавливаться в соответствующее дезоксипроизводное. Под действием фосфатазы 5-Р-дУДФ снова теряет фосфат, и образующийся 5-Р-дУМФ связывается с тимидилатсинтазой и N5, N10-метилен-Н4-фолатом, образуя комплекс, напоминающий промежуточное соединение в реакции превращения дУМФ в дТМФ. Тимидилатсинтаза оказывается полностью блокированной, и синтез дТМФ прекращается:
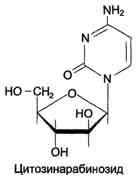
Цитозинарабинозид (или цитарабин) представляет собой соединение, в котором остаток ри-бозы замещён на стериоизомер - арабинозу. Оно используется в химиотерапии рака, в частности, при острой миелоцитарной лейкемии.
В организме препарат может превращаться в дНТФ, ингибировать ДНК полимеразы и снижать скорость репликации.
Аналоги фолиевой кислоты. В обмене нуклеотидов производные Н4-фолата как доноры од-ноуглеродных групп участвуют в формировании пуринового гетероциклического кольца и в ключевой реакции синтеза дТМФ из дУМФ, катализируемой тимидилатсинтазой.
В последнем случае N5,N10-метилен-Н4-фолат служит донором метальной группы и в ходе реакции превращается в Н2-фолат. Для активного синтеза тимидиловых нуклеотидов Н2-фолат должен повторно использоваться, проходя стадию восстановления в Н4-фолат (см. формулу ниже).
Метотрексат и аминоптерин - структурные аналоги фолиевой кислоты - ингибируют дигидрофолатредуктазу и таким образом нарушают синтез пуриновых нуклеотидов и превращение дУМФ в дТМФ, снижая внутриклеточную концентрацию субстратов синтеза ДНК и РНК. Препараты широко используют в химиотерапии опухолей.
Антивирусные и антибактериальные препараты
Азидотимидин (AZT, или зидовидин) представляет собой мощный противовирусный препарат, применяющийся в лечении инфекций, которые сопровождают приобретённые формы иммунодефицита. Будучи структурным аналогом тимиди-на, препарат имеет в З'-положении дезоксирибозы азидогруппу.
AZT может фосфорилироваться и с помощью ДНК-полимераз включаться в растущую молекулу ДНК. Однако присутствие в 3'-положении дезоксирибозы азидогруппы делает синтезирующиеся молекулы ДНК не способными к последующему удлинению. В результате образование новых молекул ДНК прекращается.
Важно, что фосфорилированные производные AZT утилизируются более эффективно вирусной ДНК-полимеразой или так называемой обратной транскриптазой, чем ДНК-полимеразами эукариотов, поэтому препарат наиболее эффективно влияет на размножение вирусов и, в частности, ретровируса, вызывающего ВИЧ-инфекцию.
5-йоддезоксиуридин используют в терапии кератитов и поражений роговицы глаза вирусом герпеса.
Азатиоприн в организме превращается в 6-меркаптопурин, который оказывает мощное иммуносупрессорное действие. Препарат широко используют в трансплантологии для предотвращения развития иммунологических реакций, вызывающих отторжение трансплантата.
26. Первичная структура нуклеиновых кислот. ДНК и РНК – черты сходства и различия состава, локализация в клетке, функции. Вторичная структура ДНК (модель Уотсана и Крика). Связи, стабилизирующие вторичную структуру ДНК. Комплементарность. Правило Чаргаффа. Полярность. Антипараллельность.
Первичная структура ДНК - порядок чередования дезоксирибонуклеозидмонофосфатов (дНМФ) в полинукпеотидной цепи.
Каждая фосфатная группа в полинукпеотидной цепи, за исключением фосфорного остатка на 5'-конце молекулы, участвует в образовании двух эфирных связей с участием 3'- и 5'-углеродных атомов двух соседних дезоксирибоз, поэтому связь между мономерами обозначают 3', 5'-фосфодиэфирной.
Концевые нуклеотиды ДНК различают по структуре: на 5'-конце находится фосфатная группа, а на 3'-конце цепи - свободная ОН-группа. Эти концы называют 5'- и 3'-концами. Линейная последовательность дезоксирибонуклеотидов в полимерной цепи ДНК обычно сокращённо записывают с помощью однобуквенного кода, например -A-G-C-T-T-A-C-A- от 5'- к 3'-концу.
В каждом мономере нуклеиновой кислоты присутствует остаток фосфорной кислоты. При рН 7 фосфатная группа полностью ионизирована, поэтому in vivo нуклеиновые кислоты существуют в виде полианионов (имеют множественный отрицательный заряд). Остатки пентоз тоже проявляют гидрофильные свойства. Азотистые основания почти нерастворимы в воде, но некоторые атомы пуринового и пиримидинового циклов способны образовывать водородные связи.
Первичная структура РНК - порядок чередования рибонуклеозидмонофосфатов (НМФ) в полинуклеотидной цепи. В РНК, как и в ДНК, нуклеотиды связаны между собой 3',5'-фосфодиэфирными связями. Концы полинуклеотидных цепей РНК неодинаковы. На одном конце находится фосфорилированная ОН-группа 5'-углеродного атома, на другом конце - ОН-группа 3'-углеродного атома рибозы, поэтому концы называют 5'- и 3'-концами цепи РНК. Гидроксильная группа у 2'-углеродного атома рибозы делает молекулу РНК нестабильной. Так, в слабощелочной среде молекулы РНК гидролизуются даже при нормальной температуре, тогда как структура цепи ДНК не изменяется.
Сходства: 1.Содержат остатки фосфорной кислоты; 2.Углеводы (рибоза и дезоксирибоза ) находятся в бета-Д-рибофуранозной форме; 3.Биополимеры мономерами, которых являются мононуклеотиды; 4.Содержат по 2 пиримидиновых и по 2 пуриновых оснований. Различия: 1.ДНК-дезоксирибоза, РНК-рибоза; 2.ДНК-тимин, РНК-урацил (Нуклеотид, комплементарный аденину, в РНК не тимин, как в ДНК, а урацил — неметилированная форма тимина) ; 3.ДНК-2 цепочная молекула, РНК- 1 цепочная; 4.Молярная масса молекулы ДНК больше чем РНК.
ДНК содержится преимущественно в ядре, но небольшое ее кол-во содер. в митохондриях и пластидах. РНК содер. в ядре и цитоплазме. ДНК содержит генетическую информацию и определяет особенность белков. С помощью ДНК осуществляется передача наследственных особенностей клетки. РНК непосредственно участвует в биосинтезе белка.
Вторичная структура ДНК. В 1953 г. Дж. Уотсоном и Ф. Криком была предложена модель пространственной структуры ДНК. Согласно этой модели, молекула ДНК имеет форму спирали, образованную двумя полинуклеотидными цепями, закрученными относительно друг друга и вокруг общей оси. Двойная спираль правозакрученная, полинуклеотидньхе цепи в ней антипараллельны(рис. 4-6), т.е. если одна из них ориентирована в направлении 3'→5', то вторая - в направлении 5'→3'. Поэтому на каждом из концов молекулы ДНК расположены 5'-конец одной цепи и 3'-конец другой цепи.
Молекулы ДНК состоят из двух антипараллельных цепей с комплементарной последовательностью нукпеотидов. Цепи закручены относительно друг друга в правозакрученную спираль так, что на один виток приходится примерно 10 пар нуклеотидов.
Все основания цепей ДНК расположены внутри двойной спирали, а пентозофосфатный остов - снаружи. Полинуклеотидные цепи удерживаются относительно друг друга за счёт водородных связей между комплементарными пуриновыми и пиримидиновыми азотистыми основаниями А и Т (две связи) и между G и С (три связи) (рис. 4-7). При таком сочетании каждая пара содержит по три кольца, поэтому общий размер этих пар оснований одинаков по всей длине молекулы. Водородные связи при других сочетаниях оснований в паре возможны, но они значительно слабее. Последовательность нуклеотидов одной цепи полностью комплементарна последовательности нуклеотидов второй цепи. Поэтому, согласно правилу Чаргаффа (Эрвин Чаргафф в 1951 г. установил закономерности в соотношении пуриновых и пиримидиновых оснований в молекуле ДНК), число пуриновых оснований (А + G) равно числу пиримидиновых оснований (Т + С).
Комплементарые основания уложены в стопку в сердцевине спирали. Между основаниями двухцепочечной молекулы в стопке возникают гидрофобные взаимодействия, стабилизирующие двойную спираль.
Такая структура исключает контакт азотистых остатков с водой, но стопка оснований не может быть абсолютно вертикальной. Пары оснований слегка смещены относительно друг друга. В образованной структуре различают две бороздки - большую, шириной 2,2 нм, и малую, шириной 1,2 нм. Азотистые основания в области большой и малой бороздок взаимодействуют со специфическими белками, участвующими в организации структуры хроматина.
Антипараллельность (antiparallel) цепей ДНК: противоположная направленность двух нитей двойной спирали ДНК; одна нить имеет направление от 5' к 3', другая - от 3' к 5'.
Каждая цепь ДНК имеет определенную ориентацию. Один конец несет гидроксильную группу (- ОН), присоединенную к 3'-углероду в сахаре дезоксирибозе, на другом конце цепи находится остаток фосфорной кислоты в 5'-положении сахара. Две комплементарные цепи в молекуле ДНК расположены в противоположных направлениях - антипараллельно: одна нить имеет направление от 5' к 3', другая - от 3' к 5'( рис. 43 ). При параллельной ориентации напротив 3'-конца одной цепи находился бы З'-конец другой.
Ферменты, синтезирующие новые нити ДНК и называемые ДНК-полимеразами, могут передвигаться вдоль матричных цепей лишь в одном направлении от 3'-конца к 5'-концу. Поэтому в процессе репликации одновременный синтез новых цепей идет антипараллельно.
Обе цепи в молекуле ДНК имеют противоположную полярность. Это означает, что межнуклеотидная связь в одной цепи имеет направление 5'–>3', а в другой – 3'–>5'. Подобная направленность цепей имеет важное биологическое значение при репликации и транскрипции молекулы ДНК. Полярность цепи играет важную роль при синтезе ДНК (удлинение цепи возможно только путём присоединения новых нуклеотидов к свободному 3'-концу).
