
Биохимия растений
.pdf
Âклетках некоторых бактерий найден фермент, катализирую˝- щий синтез α-аланина путем декарбоксилирования аспарагиновой кислоты с противоположного конца:
Âходе декарбоксилирования моноаминомонокарбоновых кис˝-
лот осуществляется превращение аминокислот в амины, а при˝ де-
карбоксилировании диаминомонокарбоновых кислот образу˝ются
диамины. Так, например, под действием фермента лизиндекарбоксилазы (4.1.1.18) лизин превращается в диамин, называемый ка-
даверином. В результате аналогичных реакций из орнитина о˝бра-
зуется путресцин, из тирозина — тирамин, из гистидина — ˝гиста-
мин, из валина — изобутиламин. Кадаверин, путресцин, тира˝мин
èнекоторые другие амины токсичны для организма человека˝. Они в большом количестве могут накапливаться при разложении˝ про-
дуктов, богатых белками, под действием микроорганизмов, и˝мею-
щих активные декарбоксилазы аминокислот. Много аминов на˝-
капливается в грибах.
441

В растительных тканях также содержатся амины, которые явл˝я-
ются продуктами обмена аминокислот. Избыточные концентр˝а-
ции аминов наблюдаются при нарушениях обмена азотистых в˝е-
ществ, и в этом случае они могут вызывать токсическое дейс˝твие на растения. Образующиеся из аминокислот амины могут подв˝ер-
гаться различным превращениям, включающим окисление, син˝-
тез алкалоидов, азотистых оснований и других биологическ˝и
активных веществ. Окисление аминов катализируют ферменты
моноаминооксидазы è диаминооксидазы. Продукты этих реакций — аммиак, альдегиды и пероксид водорода:
Альдегиды подвергаются дальнейшему окислению в кислоты˝
по уже известному нам механизму.
Некоторые амины служат источниками образования алкалои˝-
дов. Так, например, из тирамина синтезируется алкалоид гор˝де-
нин, из кадаверина — пиперидин, из путресцина — пиролли˝н (см. с. 573—574).
Компоненты фосфолипидов этаноламин и холин образуются в˝
результате декарбоксилирования аминокислоты серина. По˝д действием сериндекарбоксилазы серин вначале превращается в этаноламин, который далее метилируется с участием метилтрансферазы и дает холин. Донором метильных групп для образования хол˝ина
служит S-аденозилметионин.
442
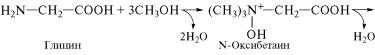
Âпроцессе распада аминокислот продукты их дезаминирова˝- ния и декарбоксилирования через ряд промежуточных стади˝й мо-
гут превращаться в ходе дыхательных реакций в пировиноградную, щавелевоуксусную, α-кетоглутаровую, янтарную кислоты, а
также в ацетил-КоА и пропионил-КоА, которые далее могут оки˝с-
ляться до СО2 è Í2О. Так, было выяснено, что конечные продукты
распада глутаминовой кислоты, пролина, аргинина, гистидин˝а — пировиноградная кислота и ацетил-КоА, а лизина, лейцина, тр˝ип-
тофана — ацетил-КоА. Из метионина, треонина, валина, изоле˝й-
цина образуется пропионил-КоА; из фенилаланина и тирозина˝ — ацетил-КоА и янтарная кислота. Серин, цистеин и α-аланин при распаде дают пировиноградную кислоту, глицин — глиокси˝ло-
вую кислоту, которые затем превращаются в щавелевоуксусную
кислоту. Таким образом, аминокислоты, легко превращаясь в˝ продукты дыхательных реакций, могут использоваться в рас˝ти-
тельном организме как субстраты дыхания.
Вместе с тем аминокислоты, являясь первичными азотистыми˝
продуктами растений, участвуют в синтезе других азотисты˝х веществ. Протеиногенные аминокислоты служат структурными˝
компонентами для построения белковых молекул. Аспарагин˝овая кислота, глицин, глутамин участвуют в синтезе пуриновых н˝укле-
отидов, аспарагиновая кислота — еще и в синтезе пиримиди˝новых нуклеотидов и никотиновой кислоты. Из валина образуются м˝оле-
кулы пантотеновой кислоты и кофермента А, из серина — фос˝фа-
тидилсерины, фосфатидилэтаноламины и фосфатидилхолины,˝ из
треонина — витамин В12, из триптофана — индолилуксусная кислота. Из глицина кроме пуриновых нуклеотидов синтезируют˝ся
хлорофиллы и другие порфирины, а также витамин В12. Êàê áûëî
показано ранее, глицин, цистеин и глутамииновая кислота д˝ают
физиологически активный пептид глютатион.
Ароматические аминокислоты фенилаланин и тирозин испол˝ь- зуются для синтеза ароматических спиртов, альдегидов, кет˝онов и их производных. Они также являются источниками образован˝ия
флавоноидных соединений, таннинов и лигнина (см. гл. 13). При˝
окислении фенилаланина и тирозина синтезируются темноо˝крашенные продукты конденсации — меланины (см. с. 555—556).
Âрезультате метилирования аминокислот происходит обра˝зование их N-метильных производных — бетаинов. Простейший представитель бетаинов — гликокол-бетаин, синтезирующи˝йся путем метилирования аминокислоты глицина:
443

Гликокол-бетаин содержится во многих растительных проду˝к-
тах, но особенно его много накапливается в корнеплодах (до˝ 0,6 %) и листьях (до 3 %) сахарной свеклы. Бетаины, как и метио-
нин, содержат подвижную метильную группу и могут ее перед˝а- вать на другие соединения. Из гликокол-бетаина образуется˝ триметиламин, придающий запах зерну, пораженному головней.
11.3. СВЯЗЫВАНИЕ ИЗБЫТОЧНОГО АММИАКА
При интенсивном дезаминировании аминокислот и других
азотистых веществ в организмах в ходе диссимиляции орган˝ических соединений высвобождается большое количество аммон˝ий-
ной формы азота, которая в высоких концентрациях токсична˝ для растительных тканей. Повышение концентрации аммонийног˝о
азота в растениях наблюдается также при внесении аммоний˝ных форм азотных удобрений. Поступающий в растение из почвы и˝ли
образовавшийся в результате распада азотистых веществ а˝ммо-
нийный азот активно используется для синтеза аминокисло˝т, вступая в реакции восстановительного аминирования с кет˝оаналогами аминокислот. Однако, если концентрация аммонийног˝о
азота в растительных тканях чрезмерно повышается, в дейст˝вие
вступают механизмы связывания аммиака, защищающие расте˝ния от аммиачного отравления.
Как установлено в опытах, признаки аммиачного отравления˝ у растений с нейтральным клеточным соком наблюдаются при с˝о- держании в вегетативной массе свыше 30—40 мг% аммонийного
азота. Более устойчивы к аммиачному отравлению растения с˝ кис-
лым клеточным соком (рН 1,3—4) — щавель, бегония, ревень, пеларгония, осоки, хвощи и др. У этих растений в клеточном сок˝е накапливается много органических кислот (яблочной, щавел˝евой, лимонной, янтарной и др.), которые связывают аммиачный азот˝ в виде аммонийных солей и таким образом предотвращают амми˝ач- ное отравление указанных растений.
444
У большинства культурных растений, хотя они и содержат в своих тканях органические кислоты, являющиеся продуктам˝и дыхательных реакций, реакция клеточного сока близка к нейтр˝альной, поэтому они не способны связывать в виде аммонийных с˝о-
лей большое количество азота, образующегося при распаде а˝зотистых веществ или поступающего в растения из почвы как фак˝тор
азотного питания. У них избыточный аммонийный азот обезвр˝е- живается путем образования амидов дикарбоновых аминоки˝с-
лот — глутамина и аспарагина. На синтез амидов затрачива˝ется
метаболическая энергия, которая высвобождается за счет г˝идро-
лиза АТФ. Реакция синтеза глутамина из глутаминовой кисло˝ты и
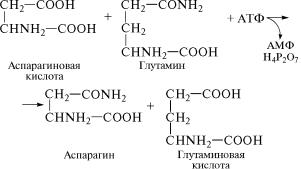
аммиака с участием АТФ под действием фермента глутаминси˝нтетазы была показана ранее. Образование аспарагина катализ˝ирует
фермент аспарагинсинтетаза (6.3.5.4), способная за счет гидроли-
за глутамина осуществлять синтез амидной группировки ас˝пара-
гина в результате следующей реакции:
Кроме аспарагина и глутаминовой кислоты продуктами данного превращения также являются аденозинмонофосфат и ди˝- фосфорная кислота, возникающие в результате гидролиза ма˝кроэргической связи АТФ между первым и вторым остатками фос-˝
форной кислоты. При высоких концентрациях аммонийной
формы азота возможно образование аспарагина непосредст˝венно с участием аммиака по аналогии с реакцией образования глу˝тамина. Однако фермент аспарагинсинтетаза имеет большее сродство к глутамину как донору NH2-групп, чем к NH4+-ионам,
поэтому указанная выше реакция синтеза аспарагина из асп˝арагиновой кислоты и глутамина наиболее типична для растени˝й.
Ферменты глутаминсинтетаза и аспарагинсинтетаза локали˝зованы в цитоплазме.
Динамика содержания амидов в растительных тканях в завис˝и-
мости от направленности проходящих в них биохимических п˝ро-
445
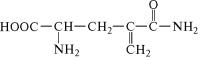
цессов была выяснена в классических исследованиях Э. Шул˝ьце, Д. Н. Прянишникова, А. Чибнелла, В. Л. Кретовича. Было отмеч˝е- но, что при интенсивном дезаминировании азотистых вещест˝в или преимущественном питании растений аммонийной формо˝й
азота в тканях растений наблюдается накопление аспараги˝на и глутамина, причем у большинства растений глутамина содер˝жится
больше, чем аспарагина. У некоторых растений избыточный а˝м- миак связывается главным образом путем его включения в гл˝ута-
мин. К таким растениям относится сахарная свекла, в корнеп˝ло-
дах которой при усиленном питании растений аммонийными с˝о-
лями может накапливаться свыше 5 % глутамина в расчете на с˝у-
хую массу. У других растений при связывании избыточного аммиака наблюдается преимущественное накопление аспара˝гина.
Например, в этиолированных проростках люпина, в которых
очень активно происходит распад азотистых веществ с обра˝зова-
нием аммиака, содержится много аспарагина (до 11 % сухой мас˝-
сы). Также много аспарагина накапливается в корневищах сп˝аржи (до 17 % сухой массы).
Изучение процесса ассимиляции аммонийной формы азота,
поступающей в растения из почвы, показывает, что почти вес˝ь
аммиачный азот превращается в корнях в аммонийный азот ам˝и-
нокислот и амидный азот глутамина и аспарагина. Поэтому б˝олее половины азота, переносимого из корней в вегетативную час˝ть ра-
стений с ксилемным и флоэмным током, представлено амидами˝.
Аспарагин и глутамин, образующиеся при связывании избыто˝чно-
го аммиака, активно участвуют в различных биохимических п˝ро-
цессах как доноры аминных групп и источники образования д˝ругих азотистых веществ.
У некоторых растений основным веществом, в виде которого
связывается избыточный аммиачный азот, является произво˝дное глутамина — γ-метиленглутамин:
Много γ-метиленглутамина содержится в корнях и пасоке ара-
хиса, листьях и луковицах тюльпана, листьях папоротника, п˝роростках бобов, хмеле, горохе.
11.4.СИНТЕЗ МОЧЕВИНЫ
Âклетках растений существует еще один дополнительный ме˝- ханизм обезвреживания избыточной аммонийной формы азот˝а —
связывание его в виде мочевины, которая синтезируется в р˝еакци-
446
ÿõ орнитинового цикла, впервые изученного в 1932 г. в клетках животных Н. А. Кребсом и К. Хензелайтом. Значительное колич˝ество мочевины накапливается в клетках растений, на корнях кото˝рых развивается микориза. Высокое содержание мочевины обнар˝уже-
но в шампиньонах и дождевиках (до 10—13 % сухой массы). Опытным путем было установлено, что концентрация мочеви-
ны в клетках растений увеличивается при диссимиляции азо˝тистых веществ, когда активируются процессы дезаминировани˝я
аминокислот и азотистых оснований, а также при выращивани˝и
растений на растворах аммонийных солей. Мочевина нетокси˝чна
для клеток растений, так как является нормальным продукто˝м об-
мена веществ, который легко включается в биосинтетически˝е реакции.
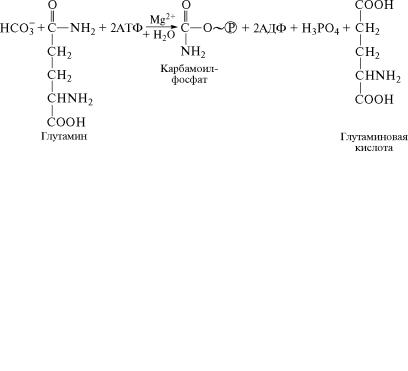
Первый этап синтеза мочевины — образование макроэргиче˝с-
кого соединения карбамоилфосфата из гидрокарбоната и глутами-
на, служащего источником аминной группировки, под действи˝ем
фермента карбамоилфосфатсинтазы (2.7.2.5). Реакция сопряжена с гидролизом двух молекул АТФ и активируется катионами Mg2+:
На следующем этапе с участием фермента орнитин-транскарба- моилазы (2.1.3.3) карбамоилфосфат вступает во взаимодействие с орнитином. Продукты этой реакции — цитруллин и неоргани˝ческий фосфат:
447

Таким образом, уреидогруппа цитруллина образуется из кар˝бонильной группы бикарбоната и амидной группы глутамина, ко˝торая синтезируется в результате связывания избыточного а˝ммиака.
Далее цитруллин реагирует с аспарагиновой кислотой под д˝ей-
ствием фермента аргининосукцинатсинтетазы (6.3.4.5). В активировании уреидогруппы цитруллина принимают участие АТФ и˝ ка-
тионы Mg2+. В ходе этой реакции синтезируется аргининоянтарная кислота.
Затем аргининоянтарная кислота с участием фермента аргининосукцинатлиазы (4.3.2.1) расщепляется на два продукта — аргинин и фумаровую кислоту. Последняя, присоединяя молекулу ˝аммиака под действием аспартатаммиаклиазы, снова превращается
в аспарагиновую кислоту, способную взаимодействовать с н˝овой
молекулой цитруллина. Аргинин в орнитиновом цикле путем г˝идролитического расщепления превращается в орнитин и моче˝вину. Эту реакцию катализирует фермент аргиназа (3.5.3.1):
448
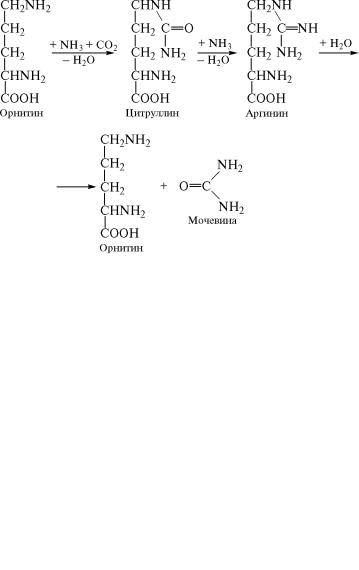
Высвобождающийся при гидролизе аргинина орнитин снова включается в первую реакцию орнитинового цикла, и синтез ˝мо- чевины может продолжаться. Схематически связывание аммиака в реакциях орнитинового цикла можно представить в виде сле˝дую-
щих превращений:
У некоторых растений связывание избыточного аммиака не д˝о-
ходит до образования мочевины, у них наблюдается накоплен˝ие промежуточных продуктов орнитинового цикла — цитрулли˝на
или аргинина. В прорастающих семенах хвойных растений и к˝луб-
нях топинамбура содержится много аргинина, а в корневых к˝лу-
беньках ольхи, пасоке березы и орешника — цитруллина. У э˝тих растений аргинин и цитруллин, по-видимому, являются основ˝ными продуктами связывания избыточного аммиака и они играю˝т
важную роль в обмене азотистых веществ.
Конечный продукт связывания аммиака в реакциях орнитино˝- вого цикла — мочевина — очень легко включается в обмен˝ азотистых веществ растений с участием соответствующих фермент˝ных систем. В листьях и других органах многих растений находи˝тся в
активном состоянии или может активироваться мочевиной ф˝ер-
ìåíò уреаза, катализирующий гидролитическое разложение моче- вины на диоксид углерода и аммиак:
449
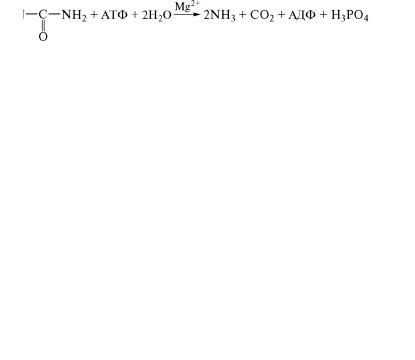
Затем аммиак включается в синтез аминокислот и амидов, ко˝- торые далее могут участвовать в образовании молекул друг˝их азотистых веществ. Фермент уреаза обнаружен у многих растени˝й — огурца, бобов, кукурузы, картофеля, томата, сельдерея.
Однако у ряда растений уреаза отсутствует, однако они спо˝собны ассимилировать мочевину, наносимую на поверхность лис˝тьев
или вводимую в ткани растений экзогенно, с помощью других˝ ферментных систем. Из клеток дрожжей и хлореллы выделен ф˝ер-
ìåíò АТФ-гидролизующая уреаза (3.5.1.45), способный в присут-
ствии АТФ и катионов Mg2+ разлагать мочевину на аммиак и ди-
оксид углерода:
Вместе с тем при изучении ассимиляции мочевины листьями злаковых растений, клетками водоросли хлореллы и пророст˝ками
бобовых, не имеющих уреазы, было отмечено накопление в них˝
значительного количества аргинина и аргининоянтарной к˝исло-
ты. При этом расщепление мочевины на аммиак и диоксид угле˝-
рода не происходило. На основе этих данных была сформулир˝ована гипотеза об обращении реакций орнитинового цикла при в˝ы-
сокой концентрации в клетках растений мочевины, поступаю˝щей
извне в виде некорневой подкормки, инъекций или при выращ˝и-
вании на среде, содержащей мочевину. Синтез аргинина и арг˝и-
ниноянтарной кислоты в соответствии с этой гипотезой мож˝ет осуществляться по следующей схеме:
В результате расщепления аргининоянтарной кислоты могу˝т далее образоваться цитруллин и аспарагиновая кислота. Пр˝и этом цитруллин, превращаясь в орнитин, инициирует продолжение˝
обращения реакций орнитинового цикла, направленное на св˝язы-
вание мочевины и образование аргинина, а аспарагиновая ки˝слота
является основным продуктом этих реакций, который далее в˝клю-
чается в синтез аминокислот, белков и других азотистых ве˝ществ.
450
