
- •Лекція 1 Метаболізм ліпідів: катаболізм триацилгліцеролів, окиснення жирних кислот і гліцеролу. Метаболізм кетонових тіл План:
- •1.1 Біологічна роль, класифікація, будова та функції основних класів ліпідів. Жирно-кислотний склад ліпідів
- •I Прості ліпіди:
- •II Складні ліпіди:
- •Структура сфінгомієліну
- •Структура цераміду
- •Жирно-кислотний склад ліпідів
- •1.2 Основні шляхи внутрішньоклітинного метаболізму ліпідів
- •1.3 Катаболізм триацилгліцеролів: послідовність реакцій, механізми регуляції активності триацилгліцеролліпази, нейрогуморальна регуляція ліполізу
- •1.3.1 Послідовність реакцій ліполізу
- •1.3.2 Молекулярні механізми регуляції ліполізу
- •1.3.3 Нейрогуморальна регуляція ліполізу
- •1.4 Окиснення жирних кислот: послідовність реакцій, енергетика процесу
- •1.4.1 Послідовність реакцій окиснення жирних кислот
- •(5) Тканинне дихання і окислювальне фосфорилювання
- •3 Ферментативні реакції b-окиснення жирних кислот
- •4 Результат 1-го циклу b-окиснення:
- •1.4.2 Енергетичний баланс b-окиснення жирних кислот
- •1.5 Окиснення ненасичених жирних кислот та жирних кислот із непарним числом атомів вуглецю
- •1.6 Метаболізм гліцеролу
- •1.7 Метаболізм кетонових тіл
- •2 Ацетил-КоА
- •Лекція 2 Біосинтез ліпідів. Метаболізм холестеролу. Транспорт, депонування, регуляція та порушення обміну ліпідів
- •2.1 Біосинтез вищих жирних кислот: метаболічні джерела, ферментативні реакції, регуляція синтезу. Елонгація жирних кислот. Утворення моно- і поліненасичених жирних кислот
- •2.1.1 Біосинтез жирних кислот
- •2 Послідовність реакцій синтезу насичених жирних кислот
- •3 Швидкість синтезу жирних кислот контролюється енергетичним станом клітини (співвідношенням атф/адф).
- •2.1.2 Елонгація жирних кислот. Утворення моно- і поліненасичених жирних кислот
- •2.2 Біосинтез триацилгліцеролів
- •2.3 Шляхи обміну фосфоліпідів
2 Послідовність реакцій синтезу насичених жирних кислот
Синтез жирних кислот забезпечує мультиензимний комплекс синтаза жирних кислот (пальмітилсинтаза), що складається з 6 ферментів і специфічного ацилтранспортуючого протеїну (АТП). Всі індивідуальні компоненти комплексу зібрані в компактну структуру. АТП має дві вільні HS-групи. Одна сульфгідрильна група належить залишку цистеїну, а друга – простетичній групі 4-фосфопантотеїну. Функція АТП у біосинтезі жирних кислот анаголічна функції КоА у β-окисненні жирних кислот.
Синтез жирної кислоти починається з приєднання до однієї HS-групи ацилтранспортуючого протеїну ацетильної групи з ацетил-КоА, до другої HS-групи – малонільної групи із малоніл-КоА:
Ацетил-трансацилаза
(
 1)
СН3-СО-S-КоА
+ HS-АТП
СН3-СО-S-АТП
+ HS-КоА
1)
СН3-СО-S-КоА
+ HS-АТП
СН3-СО-S-АТП
+ HS-КоА
Ацетил-КоА Ацетил-АТП
Малоніл-трансацилаза
(
 2) НООС-СН2-СО-S-КоА
+ HS-АТП
2) НООС-СН2-СО-S-КоА
+ HS-АТП
Малоніл-КоА

 НООС-СН2-СО-S-АТП
+ HS-КоА
НООС-СН2-СО-S-АТП
+ HS-КоА
Малоніл-АТП
Конденсація ацетильної та малонільної груп із виділенням СО2 і утворенням ацетоацетильної групи, яка приєднана до однієї НS-групи, а друга НS-група стає вільною:
Ацил-малоніл-АТП
(конденсуючий фермент)
(
 3)
СН3-СО-S-АТП
+ НООС-СН2-СО-S-АТП
3)
СН3-СО-S-АТП
+ НООС-СН2-СО-S-АТП
Ацетил-АТП Малоніл-АТП

 СН3-СО-СН2-СО-S-АТП
+ НS-АТП
+ СО2
СН3-СО-СН2-СО-S-АТП
+ НS-АТП
+ СО2
Ацетоацетил-АПБ
Наступні реакції синтезу протилежні до реакцій β-окиснення жирних кислот.
Відновлення кетогрупи у β-положенні до гідроксильної:
β-Кетоацил-АТП-редуктаза
(
 4)СН3-СО-СН2-СО-S-АТП
+ НАДФН
+ Н+
4)СН3-СО-СН2-СО-S-АТП
+ НАДФН
+ Н+
Ацетоацетил-АПБ

 СН3-СН(ОН)-СН2-СО-S-АТП
+ НАДФ+
СН3-СН(ОН)-СН2-СО-S-АТП
+ НАДФ+
β-Гідроксибутирил-АТП
Дегідратація β-Гідроксибутирил-АТП з утворенням подвійного зв'язку між 2-м і 3-м положеннями:
β-Гідроксиацил-АТП-дегідрогеназа
(
 5)
СН3-СН(ОН)-СН2-СО-S-АТП
5)
СН3-СН(ОН)-СН2-СО-S-АТП
β-Гідроксибутирил-АТП

 СН3-СН=СН-СО-S-АТП
+ Н2О
СН3-СН=СН-СО-S-АТП
+ Н2О
Кротоніл-АТП
Відновлення подвійного зв'язку:
Еноїл-АТП-редуктаза
(
 6)
СН3-СН=СН-СО-S-АТП
+ НАДФН
+ Н+
6)
СН3-СН=СН-СО-S-АТП
+ НАДФН
+ Н+
Кротоніл-АТП

 СН3-СН2-СН2-СО-S-АТП
+ НАДФ+
СН3-СН2-СН2-СО-S-АТП
+ НАДФ+
Бутирил-АТП
Далі цикл реакцій повторюється. У випадку синтезу пальмітинової кислоти (С16) необхідно 7 циклів, у кожному з яких початком є приєднання молекули малоніл-АТП до карбоксильного кінця ланцюга жирної кислоти, що росте. При цьому відщеплюється дистальна карбоксильна група малоніл-АТП у вигляді СО2. Таким чином, ланцюг жирної кислоти послідовно наростає від метильного кінця до карбоксильного.
Основні етапи синтезу жирних кислот наведені на рис.10.
 СН3СО-S-КоА
СО2
АТФ+Н2О
СН3СО-S-КоА
СО2
АТФ+Н2О



 НS-АТП
НS-АТП
НS-КоА Ацетил-КоА АДФ+Н3РО4

НООС-СН2-СО- S-КоА
СН3-СО-S-КоА Малоніл-КоА

 Ацетил-АТП
НS-АТП
Ацетил-АТП
НS-АТП
 НS-КоА
НS-КоА
НООС-СН2-СО- S-АПБ
 Малоніл-АТП
Малоніл-АТП




 СО2
СО2
СН3СОСН2СО-S-АТП
Ацетоацетил-АТП
 НАДФН
+ Н+
НАДФН
+ Н+
НАДФ+
СН3СН(ОН)СН2СО-S-АТП
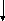 3-Гідроксибутирил-АТП
3-Гідроксибутирил-АТП
 Н2О
Н2О
СН3СН=СНСО-S-АТП
Кротоніл-АТП

 НАДФН
+ Н+
НАДФН
+ Н+
НАДФ+
 СН3СН2СН2СО-S-АТП
СН3СН2СН2СО-S-АТП
Бутирил-КоА

Жирна кислота з парною
кількістю атомів вуглецю
Рисунок 10 – Загальна схема синтезу жирних кислот
Завершується синтез жирної кислоти відщепленням HS-АТП від пальмітоїл-АТП під впливом деацилази:
Деацилаза
С Н3-(СН2)14-СО-S-АТП
+ Н2О
СН3-(СН2)14-СООН
+ НS-АТП
Н3-(СН2)14-СО-S-АТП
+ Н2О
СН3-(СН2)14-СООН
+ НS-АТП
Пальмітоїл-КоА Пальмітинова кислота
Сумарне рівняння синтезу пальмітинової кислоти:
С Н3-СО-S-КоА
+ 7НООС-СН2-СО-S-КоА
+ 14НАДФН + 14Н+
Н3-СО-S-КоА
+ 7НООС-СН2-СО-S-КоА
+ 14НАДФН + 14Н+
Ацетил-КоА Малоніл-КоА
 СН3-(СН2)14-СООН
+ 7СО2
+ 8НS-КоА
+ 14НАДФ+
+ 6Н2О
СН3-(СН2)14-СООН
+ 7СО2
+ 8НS-КоА
+ 14НАДФ+
+ 6Н2О
Пальмітинова кислота
Враховуючи, що на утворення однієї молекули малоніл-КоА з ацетил-КоА використовується одна молекула АТФ і одна молекула СО2, яка потім відщеплюється, сумарне рівняння таке:
 8СН3-СО-S-КоА
+ 7АТФ + 14НАДФН + 14Н+
8СН3-СО-S-КоА
+ 7АТФ + 14НАДФН + 14Н+
Ацетил-КоА
 СН3-(СН2)14-СООН
+ 14НАДФ+
+ 8НS-КоА
+ 7АДФ + 7Н3РО4
+ 6Н2О
СН3-(СН2)14-СООН
+ 14НАДФ+
+ 8НS-КоА
+ 7АДФ + 7Н3РО4
+ 6Н2О
Пальмітинова кислота
Регуляція біосинтезу насичених жирних кислот.
Регуляція синтезу жирних кислот відбувається на рівні ацетил-КоА-карбоксилази і мультиферментного комплексу синтази жирних кислот.
1 Регуляція активності ацетил-КоА-карбоксилази здійсню-ється за рахунок трьох механізмів.
1.1 Алостерична регуляція.
а) Активатором ферменту є цитрат, збільшення кон-центрації якого у постсорбційний період активує анаболічні процеси в клітині, тобто запасання надлишків ацетил-КоА у вигляді жирів. За відсутності активатора ензим малоактивний.
б) Інгібітором ферменту є кінцеві метаболіти – пальмітоїл-КоА та стеароїл-КоА. Кінцеві продукти біосинтезу інгібують власний синтез за принципом негативного зворотного зв'язку.
1.2 Ковалентна модифікація
Активність ензиму регулюється за рахунок ц-АМФ залежного фосфорилювання (неактивна форма ферменту) та дефосфорилювання (активна форма ферменту). Трансформація ферменту в активну та неактивну форму регулюється дією гормонів. Інсулін – активує, адреналін, норадреналін, глюкагон – інгібують ензим.
1.3 Зміна швидкості синтезу ферменту:
а) Ферментна індукція – збільшення синтезу ензиму, яке спостерігається при високовуглеводній дієті або споживанні раціону з низьким вмістом ліпідів.
б) Ферментна репресія – зниження швидкості синтезу ензиму при голодуванні або споживання збагаченого жирами раціону.
2 Регуляція активності мультиензимного комплексу синтази жирних кислот (циклу Лінена) здійснюється за рахунок механізмів:
2.1 Алостеричної регуляції - активація окремих ферментів комплексу фосфорильованими моносахаридами (глюкозо-6-фосфат та ін.); інгібування ферментів кінцевим продуктом біосинтетичного шляху – пальмітоїл-КоА.
2.2 Зміни швидкості синтезу окремих ферментів комплексу в умовах голодування та постсорбтивний період.
