
- •Лекции по общей химии Введение.
- •Основные законы химии.
- •Стехиометрические законы.
- •Газовые законы.
- •3. Уравнение состояния идеального газа (Клапейрона-Менделеева).
- •Строение атома
- •Квантово-механическая модель строения атома
- •Лекция 3. Периодический закон и электронные конфигурации атомов.
- •Радиусы атомов. Потенциал ионизации. Сродство к электрону. Электроотрицательность.
- •Лекции 2, 3 Химическая связь. Метод молекулярных орбиталей (ммо).
- •Рассмотрим молекулы нf и ВеН2, в которых имеет место образование несвязывающих мо. Сравнение методов мвс и ммо.
- •О валентности.
- •Металлическая связь.
- •Ионная связь.
- •Водородная связь.
- •Межмолекулярные взаимодействия.
- •Взаимосвязь между типом хс и свойствами веществ.
- •Стеклообразное состояние вещества.
- •Применение процессов возбуждения электронов для практических целей.
- •Основы химической термоднамики. Функции состояния.
- •Внутренняя энергия
- •Энтальпия.
- •Энтропия.
- •2 Закон (Начало)т/д: в изолированной системе самопроизвольно протекают только такие процессы, которые ведут к росту энтропии.
- •Энергия Гиббса.
- •Энергия Гельмгольца.
- •Кинетика химических реакций.
- •Зависимость скорости реакции от температуры.
- •Катализ.
- •Цепные реакции.
- •Химическое равновесие.
- •Растворы.
- •Свойства разбавленных растворов неэлектролитов (коллигативные свойства – независящие от природы вещества).
- •Осмос и осмотическое давление.
- •Диссоциация кислот, оснований, солей.
- •Протонная теория кислот и оснований Бренстеда и Лоури.
- •Произведение растворимости.
- •Особенности растворов сильных электролитов.
- •Ионные реакции в растворах электролитов.
- •Комплексные соединения.
- •Количественные характеристики процесса гидролиза.
- •Буферные растворы.
- •Окислительно-восстановительные реакции.
- •Окислительно-восстановительная двойственность.
- •Составление уравнений овр.
- •Окислительно-восстановительный (электродный) потенциал.
- •Окислительно-восстановительная способность двух форм электрохимической системы.
- •Эдс как количественная характеристика возможности протекания окислительно-восстановительного процесса.
- •Окислительно-восстановительная способность двух форм электрохимической системы.
- •Уравнение Нернста.
- •1.Взаимодействие металлов с водой.
- •2.Взаимодействие металлов с растворами щелочей.
- •3.Взаимодействие металлов с кислотами, в которых окислитель – катион водорода.
- •4.Взаимодействие металлов с концентрированной серной кислотой.
- •Взаимодействие концентрированной серной с неметаллами-восстановителями.
- •5.Взаимодействие металлов с азотной кислотой (разб. И конц.).
- •Взаимодействие азотной кислоты с неметаллами
- •Взаимодействие металлов с растворами солей.
- •Окислительно-восстановительные свойства воды.
- •Коррозия металлов
- •Газовая коррозия
- •Образование оксидной пленки на металлах
- •Атмосферная коррозия
- •Электрохимическая коррозия
- •Методы защиты от коррозии.
- •1. Модификация самого металла:
- •2.Отделение (предохранение) металла от окружающей среды с помощью защитных покрытий (неметаллических):
- •3.Металлические защитные покрытия.
- •4.Электорохимические методы защиты (суть – заставить разрушаться болванкам).
- •5.Специальная обработка электролита или среды, в которой находится металл (удаление или уменьшение концентрации веществ, вызывающих коррозию).
- •6.Химическая обработка для повышения коррозионной стойкости (пассивация поверхности металла) - то, что не использовалось в выше приведенных методах, часто в расплавах или при повышенных температурах.
- •Измерение э.Д.С. Химических источников тока.
- •Химические источники электрической энергии (хиээ)
- •Аккумуляторы.
- •Типы аккумуляторов
- •Свинцово-кислотные аккумуляторы.
- •Принцип действия
- •Устройство
- •Литий-ионные аккумуляторы.
- •Литиевые элементы различных электрохимических систем
- •Электролиз.
- •Законы электролиза м. Фарадея.
- •Практическое применение электролиза.
- •Электрофорез и электродиализ.
- •Металлы и сплавы.
- •Классификация металлов.
- •Основные методы получения металлов.
- •Получение металлов высокой чистоты.
- •Металлы и сплавы
Окислительно-восстановительная способность двух форм электрохимической системы.
По величине электродных (ОВП) потенциалов можно судить о направленности окислительно-восстановительных процессов и силе окислителя и восстановителя.
Чем меньше алгебраическая величина ОВП (электродного потенциала), тем большими восстановительными свойствами обладает восстановленная форма и меньшими окислительными – окисленная. Т.е., чем меньше алгебраическая величина потенциала, тем выше восстановительная способность этого металла и тем ниже окислительная способность его ионов. Li+ + e = Li Е = - 3,01 В. Следовательно,металлический литий - самый сильный восстановитель, а золото-самый слабый. И наоборот, ион золота Аu3+-самый сильный окислитель, а ион лития - Li+ -самый слабый.
Чем больше величина ОВП, тем сильнее окислительные свойства окисленной формы и слабее восстановительные – восстановленной: F2 + 2e = 2F-. Следовательно молекулярный фтор – самый сильный окислитель, его ион –самый слабый восстановитель. Действительно, все галогенид-ионы, кроме фторид- иона, проявляют восстановительные свойства (реакцию взаимодействия соляной кислоты с сильными окислителями используют для получения хлора).
Направление окислительно-восстановительного процесса.
Таблица стандартных ОВП позволяет определить, в каком направлении должен (с точки зрения термодинамики) пойдет ОВП при смешивании любых двух сопряженных пар окислитель-восстановитель. В качестве окислителя всегда будет выступать окислитель той пары, стандартный потенциал которого более положительный, а в качестве восстановителя – восстановитель той пары, потенциал которого более отрицательный.
Рассмотрим равновесные потенциалы двух сопряженных пар окислитель-восстановитель: Fe3+ + e ↔ Fe2+ Eo = +0,77B
I2 + 2e ↔ 2I- Eo = +0,54B
Окислителем в ниже приведенной реакции будет - Fe3+ , а восстановителем I- ионы иода.
Fe3+ + 2I- = Fe2+ + I2
Абсолютное значение потенциала электрода (ОВП) определить нельзя. Можно лишь сравнивать потенциалы различных электродов друг с другом. Для этого надо два электрода объединить в электрохимическую цепь: металлические части соединяются проводником, а растворы электролитов, в которые они погружены - стеклянной трубкой, заполненной раствором электролита (обычно хлорида калия). Эту трубку называют электролитическим ключом или солевым мостиком. Она обеспечивает ионную проводимость между растворами. Таким образом возникает замкнутая цепь - электролитическая ячейка, состоящая из электрода, потенциал которого надо измерить и нормального водородного электрода (см рис.2), потенциал которого принят равным нулю. Электрохимическая схема такой цепи записывается следующим образом (например, для измерения потенциала цинкового электрода):
Zn|ZnSO4||H2SO4|H2(Pt)
Двойная черта обозначает электролитический контакт двух ионных проводников, который осуществляется через полупроницаемую мембрану или электролитический ключ - стеклянную трубочку (солевой мостик), заполненную раствором электролита (обычно хлоридом калия). Она обеспечивает проводимость между растворами. Металлы соединяют проводником через вольтметр, чтобы измерить электродвижущую силу (ЭДС) цепи. Отклонение стрелки вольтметра покажет значение потенциала цинкового электрода, т.к. потенциал водородного электрода принят равным нулю.
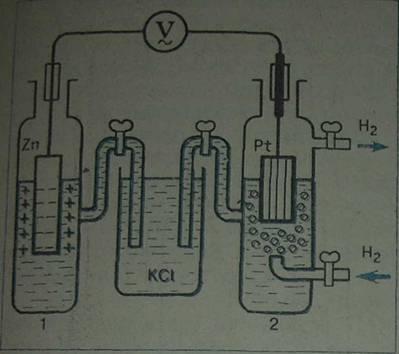
Рис. 2. Электрохимическая цепь со стандартным водородным электродом: -стандартный водородный электрод, 2-исследуемый электрод, 3 - электролитический ключ.
Особенности
измерения электродных потенциалов.
Точно
измерить электродный потенциал достаточно
трудно, так как необходимо, чтобы в
процессе измерения не нарушалось
равновесие на электродах. По этой причине
невозможно получить точное значение Е
с 
помощью обычного вольтметра: если мы замкнем цепь, используя вместо проводника вольтметр, то в ней начнет протекать довольно большой ток, который нарушит равновесие на электродах. Для измерения можно использовать специальные вольтметры с высоким входным сопротивлением (более 1012 Ом). При включении в цепь такого прибора протекающий ток слишком мал для оказания существенного влияния на электродное равновесие. Есть металлы, электродные потенциалы которых имеют отрицательные значения (меньше потенциала водородного электрод), например, алюминий, цинк, железо и др. У других металлов, менее химически активных, значение электродного потенциала положительное - больше потенциала водородного электрода. Электродные потенциалы всех металлов, а также потенциалы других окислительно-восстановительных систем измерены и расположены в порядке возрастания значений ОВП в таблицу стандартных электродных (ОВП) потенциалов. Таблицей можно пользоваться для определения силы окислителя и восстановителя. Если из этой таблицы выписать все металлы и водородный электрод в порядке возрастания значений их электродных потенциалов, мы получим ряд напряжений металлов. Однако этот термин устарел и его лучше не использовать.

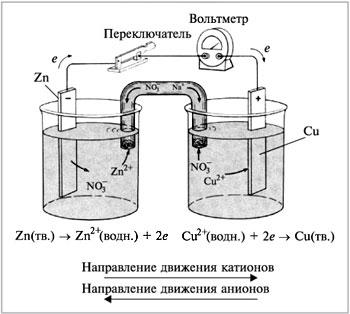
Рис. 3. Электрохимическая цепь или гальванический элемент
По величине электродных (ОВП) потенциалов можно судить о направленности окислительно-восстановительных процессов и силе окислителя и восстановителя. При помощи ряда стандартных электродных потенциалов можно характеризовать некоторые химические свойства металлов, его применяют для выяснения, в какой последовательности восстанавливаются ионы металлов при электролизе.
