
- •Глава 1.Предмет термодинамики.Основные понятия и определения.Особенности термодинамического метода исследования.Термодинамическая форма записи закона сохранения и превращения энергии.
- •Термодинамический метод исследования
- •Глава 2. Первый закон термодинамики. Равновесное состояние системы. Равновесные и неравновесные взаимодействия.
- •Глава 3. Уравнение состояния. Теплоемкость идеальных газов.
- •Критерий стабильности
- •Глава 4. Энтальпия. Расчет изменения внутренней энергии, энтальпии и энтропии. Графический метод в термодинамике
- •Глава 6. Исследование свойств реальных веществ. Термические переменные и связь между ними. Характеристические функции. Дифференциальные соотношения термодинамики.
- •Глава 8. Свойства двухфазных систем. P - V и t - s диаграммы двухфазных систем. Таблицы “Состояние насыщения” и “Вода и перегретый пар”.
- •Глава 9. Диаграмма I - s для парожидкостных систем. Особенности расчета процессов с реальными веществами
- •Глава 10. Уравнение Клапейрона-Клаузиса. Р -е диаграмма фазового равновесия. Особенности фазовых переходов первого и второго рода.
- •Глава 11. Особенности химических и фазовых превращений. Фаза. Ингредиент. Компонент. Условие равновесия многофазной многокомпонентной системы
- •Глава 12. Правило фаз Гиббса. Принцип минимальности характеристических функций
- •Глава 13. Возрастание энтропии и потеря работоспособности системы при протекании в ней необратимых процессов. Второй закон термодинамики
- •Глава 14. Тепловая теорема Нернса (постулат Нернста). Абсолютное значение энтропии. Свойства веществ вблизи абсолютного нуля температуры
- •Глава 15. Термодинамика потока. Течение газа по каналам. Процесс течения в p - V и I - s координатах
- •Глава 16. Скорость звука. Энтальпия и температура торможения. Связь скорости потока со скоростью звука. Влияние формы канала и трения на поток.
- •Глава 17. Течение газа через отверстие в стенке сосуда и через сопло Ловаля. Дросселирование. Кривая инверсии
- •Глава 18.Сжатие газов и паров.
- •Глава 19 . Циклы холодильных машин
- •Глава 20. Цикл теплового насоса
Глава 20. Цикл теплового насоса
В процессе работы холодильной установки теплота перекачивается к горячему источнику, повышая его температуру. Таким образом, холодильный цикл можно использовать в целях отопления. Работающая таким образом холодильная установка представляет собой тепловой насос. Тепловой насос забирает теплоту не из охлаждаемой емкости, а из окружающей среды. За счет затраты работы в обратном цикле температура теплоносителя повышается. Эффективность теплового насоса оценивается величиной отопительного коэффициента j
![]() , (20.1)
, (20.1)
где q 1 - количество теплоты, сообщенное нагреваемому объекту; ац- работа, подводимая в цикле.
Если в целях отопления использовать определенную холодильную машину с холодильным коэффициентом e, то
q
1 = q
2 + ац ,e=
![]() ,
,
j=e+ 1 (20.2)
Следовательно, чем выше холодильный коэффициент, тем выше и отопительный коэффициент.
Так как в тепловом насосе q 1 > ац, тоj>1. Значение отопительного коэффициента в реальных тепловых насосах равно 3 - 5.
Если бы тепловой насос работал по циклу Карно, то с учетом формулы
![]() и (20.2)
и (20.2)
![]() (20.3)
(20.3)
При постоянной температуре нижнего источника теплоты Т2 эффективность теплового насоса будет зависеть от температуры, при которой рабочее тело отдает теплоту в отопительную систему. Этой температурой и необходимо руководствоваться при выборе теплоносителя.
Максимальная работа, Эксергетический метод исследования
При переходе рабочего тела из неравновесного состояния в равновесное, максимум работы будет получен тогда, когда процесс изменения состояния рабочего тела обратим. Для определения максимальной работы рассмотрим расширенную изолированную систему, состоящую из рабочего тела (источника работы) и окружающей среды. Для того чтобы рабочее тело (система) пришло в равновесие со средой, необходимо изменить внутреннюю энергию за счет отвода или подвода теплоты или же за счет совершения работы, так как по первому закону термодинамики
du = dq - dA.
Подвод или отвод теплоты внешней среде происходит при постоянной температуре, равной температуре окружающей среды Т0. Если процесс обратим, то рабочее тело получит и отдаст теплоту при той же температуре. Тогда, по второму закону термодинамики
dq = T 0ds
Определим максимальную работу, которая складывается из той работы, которую совершит замкнутая термодинамическая система, и работы р0dv, пошедшей на преодоление давления окружающей среды р0.
Элементарная максимальная работа равна
da макс = Т 0ds-du-p0dv , (20.4)
или после интегрирования
a макс= (u 1 - u 2) - p 0 (v 1 - v 2 ) - T 0 (s 02 - s 01) (20.5)
Индексы “1” и “2” характеризуют состояние рабочего тела (системы) в начале и после приведения его в состояние равновесия с окружающей средой.
В выражении (2) разность u 1 - u 2 представляет собой работу системы в адиабатном процессе изменения состояния;p 0 (v 1 - v 2 ) - работу системы над окружающей средой;T 0 ( s 02 - s 01) -теплоту, переданную от источника работы окружающей среде и пошедшую на приращение энтропии среды.
При обратимом изменении состояния расширенной системы изменение энтропии равно нулю
( s 02 - s 01) обр +( s 2 - s 1)= 0 (20.6)
и
Ds обр=( s 02 - s 01)обр =s 1- s 2 = 0 , (20.7)
где ( s 02 - s 01)- изменение энтропии окружающей среды;( s 2 - s 1)- изменение энтропии рабочего тел (системы).
Тогда величина максимальной полезной работы, произведенной изолированной системой, т.е. работоспособность равна
а макс= (u 1 - u 2) - p 0 (v 1 - v 2 ) - T 0 (s 2 - s 1) (20.8)
Из уравнения (20.8) следует, что максимальная работа, которую можно получить от рассматриваемой системы (рабочего тела), будет определяться начальным состоянием рабочего тела в процессе производства работы, но не будет зависеть от характера процесса изменения состояния рабочего тела. Следовательно, максимальная работа представляет собой функцию состояния системы.
При необратимом изменении состояния расширенной системы, когда
( s 02 - s 01) +( s 2 - s 1)>0, (20.9)
Ds необр=( s 02 - s 01)- (s 1- s 2 ) , (20.10)
где Ds необр- увеличение энтропии системы в результате протекающих в ней необратимых процессов.
Работа системы в случае необратимости протекающих в ней процессов, полезная работа, равна
а = а макс- Т0Ds необр , (20.11)
где Т 0Ds необр - потеря работоспособности системы.
Уравнение
Dа = Т0Ds необр (20.12)
называют уравнением Гюи-Стодолы
Задача определения Ds необрдолжна решаться отдельно для каждого реального процесса. Метод исследований , основанный на анализе потерь работоспособности в процессах, называютэксергетическим методом.
Потери работоспособности в циклах
Свойство увеличения энтропии системы может быть использовано для определения потерь, возникающих вследствие необратимых явлений в процессах, и в частности в процессах преобразования теплоты и работы, т.е. в циклах.
Работа в необратимом
цикле будет меньше, чем в обратимом, и
уменьшение работы, совершаемой в цикле,
так же как и увеличение энтропии, может
служить мерой необратимости процессов,
происходящих с рабочим телом цикла.
Максимальное количество работы в цикле
при данных источниках теплоты называется
работоспособностьюилиэксергиейтеплоты очевидно, максимальную работу
в цикле Карно можно получить за счет
теплоты, отводимой от горячего источника
с температурой Т, и используя окружающую
среду в качестве холодного источника
с температурой Т0.Пусть источник
выделил бесконечно малое количество
теплотыdq, при этом в
работу превратиться лишь часть теплоты![]() ,
остальная часть
,
остальная часть![]() dqбудет передана окружающей среде. Таким
образом, максимальное количество работы
от теплотыdqс температурой
Т равно
dqбудет передана окружающей среде. Таким
образом, максимальное количество работы
от теплотыdqс температурой
Т равно
da макс =![]() (20.13)
(20.13)
Следовательно, при постоянной температуре горячего источника
а макс=q![]() (20.14)
(20.14)
Таким образом, качество
теплоты, т.е. ее ценность , зависит от
температуры и определяется коэффициентом
качества теплоты, равным![]()
Коэффициент качества теплоты определяет, какая часть ее может быть превращена в работу. Эксергия (работоспособность) теплоты при температуре окружающей среды равна нулю.
В случае переменной температуры горячего источника
а
макс=q - T 0
![]() = q- Т0 Ds
, (20.15)
= q- Т0 Ds
, (20.15)
где Ds- уменьшение энтропии горячего источника; Т0 Ds- теплота не превращенная в работу.
В отличие от цикла Карно A-B-C-D (рис.20.1) будут иметь место потери:

так как температура рабочего тела больше температуры холодного источника; из-за необратимых процессов в рабочем теле, связанных с увеличением энтропии (трение в рабочем теле в процессе сжатия d-a и расширенияb-c).
Первые два вида потерь связаны с процессом теплообмена при конечной разности температур. При этом в рабочем теле не будет равновесного состояния во всей массе и цикл будет внешне необратим. (При внешне необратимых процессах состояние рабочего тела мало отличается от равновесного и характеризуется определенными значениями термодинамических параметров так же, как это имеет место в равновесных процессах).
Изменение энтропии при неравновесных процессах теплообмена вследствие подвода (отвода) теплоты к рабочему телу может быть определено по формуле (20.10). Изменение энтропии вследствие трения может быть определено по количеству теплоты, выделившейся в процессе с трением.
Приращение энтропии системы за цикл равно приращению энтропии от каждого из составляющих процессов
Ds* = SDs.
Потери работоспособности вследствие необратимости подсчитывается как произведение температуры окружающей среды на изменение энтропии системы
Da = T 0Ds* (20.16)
Полезная работа в необратимом цикле a-b-c-d равна
а = а макс-T 0Ds*, (20.17)
причем а макс =q 1 - q 2 представляет собой работу в обратимом цикле, аT 0Ds*- потерю работоспособности.
Таким образом полезная работа необратимого цикла меньше работы обратимого цикла на величину произведения абсолютной температуры теплоприемника ( т.е. окружающей среды) на приращение энтропии всей системы. Относительный эффективный КПД необратимого цикла равен
![]() (20.20)
(20.20)
Если считать, что максимальная работа в цикле Карно (А-В-С-D) равна
а
макс=q1ht
= q1
![]() ,
,
где q1 , Т1- теплота, переданная рабочему телу от горячего источника, и температура горячего источника; Т2 = Т0- температура окружающей среды.
Тогда
![]() . (20.21)
. (20.21)
При анализе потерь работы необходимо помнить, что изменение энтропии рабочего тела за цикл равно нулю.(цикл замкнут). И общая потеря равна сумме потерь работоспособности (эксергии), а не работы. Это имеет принципиальное значение для оценки совершенства действительных процессов в отдельных частях двигателя (машины).
Потери работоспособности (эксергии) потока.
Рассмотрим установившийся поток рабочего тела, источник работы, имеющий на входе в канал параметры, u1,v1,s1,T1,p1 и на выходе из канала параметрыu2,v2,s2,T2,p2.Параметры внешней среды обозначим черезu0,v0,s0,T0,p0.
Максимальная работа, которую может произвести поток при отсутствии равновесия с окружающей средой, должна увеличиться на величину, потраченную на преодоление давления окружающей среды
p 1v 1 - p 0v 1 = v 1 (p 1 - p 0)
Величина v 1 (p 1 - p 0)представляет собой работу проталкивания в окружающую среду.
Таким образом, учитывая выражение (20.8), работа единицы массы установившегося потока в результате обратимого перехода из состояния 1 в состояние
а макс= (u 1 - u 0) - p 0(v 0 - v 1) - Т 0(s 1 - s 0) + v 1(p 1 - p 0) =
= (u 1 +p 1v 1) - (u 0 + p 0v 0) - T 0(s 1 - s 0) = (i 1 - i 0) - T 0(s 1 - s 0).(20.22)
Если кинетическая
энергия потока
![]() имеет значение, которым пренебречь
нельзя, то приw 0
= 0
имеет значение, которым пренебречь
нельзя, то приw 0
= 0
а
макс = (i 1
- i 0)
+ ![]() - T 0(s
1 - s
0).
(20.23)
- T 0(s
1 - s
0).
(20.23)
Из формул (20.22), (20.23) видно, что максимальная работа представляет однозначную функцию состояния системы, зависящую от начальных параметров и параметров окружающей среды. Снижение работоспособности между состояниями 1 и 2 вдоль пути установившегося потока равно
![]() . (20.24)
. (20.24)
Величина, на которую это снижение превышает работу, производимую над окружающей средой вне потока, является мерой необратимости любого адиабатного термодинамического процесса между состояниями 1 и 2 . При этом должны быть известны величины энтальпии и энтропии для начального и конечного состояний.
Диаграмма состояния в координатах i - s позволяет наглядно представить графически величины потери эксергии потока. Пренебрегая изменением скорости, можно вычислить потери удельной эксергии потока между состояниями 1 и 2 по формуле
Dе1-2=Dа1-2 =i 1 - i 2 - T 0 (s 1 - s 2). (20.25)
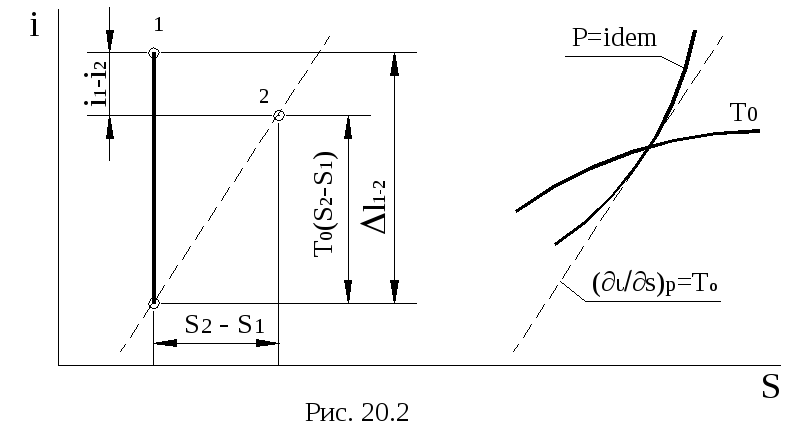
На рис. 20.2 для определения этой величины воспользуемся следующим построением. Пусть точка 1 изображает начальное состояние, точка 2 конечное. В точке пересечения изобары с изотермой Т 0проведем касательную. Наклон этой касательной к оси абсцисс пропорционален температуре окружающей среды. Через точку 2 проведем прямую, параллельную касательной до пересечения с изоэнтропой, проведенной через точку 1. Отрезок этой изоэнтропы между найденной точкой пересечения и точкой 1 представляет собой снижение эксергии рабочего тела между состояниями 1 и 2 . При вычислении удельной эксергии потока для различных рабочих тел можно воспользоватьсяe - i диаграммами для единицы массы, значение эксергии определим по формуле
e = i - i 0 - T 0 (s - s 0). (20.26)
Линии i = idemв такой диаграмме располагаются вертикально, а е =idem- горизонтально. Линииs = idemперпендикулярны осиs
На e - i диаграмму наносится сетка изобар, изотерм, а также верхняя и нижняя пограничные кривые данного процесса. Характер e - i диаграммы определяется физическими свойствами вещества, для которого она построена. Вид диаграммы, показанной на рис. 20.3 , характерен для воды, у которой Ткр>Т0.

Эксергетический метод анализа использует как первый, так и второй законы термодинамики с учетом роли окружающей среды.
Такой метод исследования теплотехнических процессов позволяет: более широко оценить термодинамическую эффективность различных процессов: количественно определить степень необратимости процессов, учитывая при этом качество теплоты; учесть влияние изменений в окружающей среде на показатели установки; наметить пути термодинамического совершенствования процессов (для уменьшения необратимости процесса горения необходимо подогревать воздух, для уменьшения потерь от необратимости теплообмена необходимо осуществлять его с минимальным перепадом температур и т.п.).
