
- •Содержание
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные понятия химии
- •1.2 Основные законы химии
- •2 Основные классы неорганических соединений
- •2.1 Простые вещества
- •2.2 Сложные вещества
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.2 Способы выражения состава растворов
- •3.1.3 Физико-химические процессы образования растворов
- •3.1.4 Экстракция
- •3.2 Растворы неэлектролитов
- •3.2.1 Законы Рауля
- •3.2.2 Осмос
- •3.3 Растворы электролитов
- •3.3.1 Электролитическая диссоциация
- •3.3.2 Сильные и слабые электролиты
- •3.4 PH водных растворов
- •4 Ионно-обменные реакции
- •4.1 Необратимые ионно-обменные реакции
- •4.2 Обратимые ионно-обменные реакции
- •5 Гидролиз солей
- •5.1 Различные случаи гидролиза
- •2) Гидролиз соли образованной сильным основанием и слабой кислотой
- •3) Гидролиз соли образованной слабым основанием и слабой кислотой
- •5.2 Константа гидролиза
- •5.3 Смещение равновесия при гидролизе
- •6. Окислительно-восстановительные реакции
- •6.1 Составление уравнений окислительно-восстановительных реакций
- •6.2 Прогнозирование окислительно-восстановительных свойств веществ по степеням окисления элементов
- •6.3 Основные типы окислительно-восстановительных реакций
- •6.4 Взаимодействие металлов с водой, кислотами и щелочами
- •7 Гальванические элементы
- •7.1 Принцип работы гальванического элемента
- •7.2 Водородный электрод сравнения. Электрохимический ряд
- •8 Электролиз
- •8.1 Электролиз расплавов
- •8.2 Электролиз водных растворов
- •8.3 Количественные расчёты в электролизе
- •8.4 Химические источники электрической энергии
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •10 Термодинамика
- •10.1 Внутренняя энергия и энтальпия. Закон Гесса
- •Или через промежуточный продукт (со) в две реакции:
- •10.2 Энтропия
- •10.3 Энергия Гиббса
- •11 Химическая кинетика Химическая кинетика – учение о скоростях и механизмах протекания химических реакций.
- •11.1 Скорость реакции
- •Основные факторы, влияющие на скорость реакции:
- •Число частиц с энергией большей, чем Еа равно заштрихованной площади.
- •12.1.2 Модель атома по Бору
- •12.2 Современные представления о строении атома
- •13 Периодический закон и периодическая таблица д.И. Менделеева
- •14 Химическая связь и строение молекул
- •14.1 Химическая связь
- •14.1.1 Квантово-механическое описание модели молекулы водорода
- •14.1.2 Основные характеристики химической связи
- •Валентный угол–это угол между двумя химическими связями.Он отражает геометрию молекулы.
- •14.1.3 Типы химических связей Ковалентная связь –это связь между двумя атомами за счет образования общей электронной пары.
- •14.2 Состав и строение молекул
- •15 Типы кристаллических решеток
- •16.1 Общая характеристика s-элементов первой и второй групп
- •16.2 Свойства воды
- •16.2.1 Строение молекулы воды
- •16.2.2 Физические свойства воды
- •16.2.3 Химические свойства воды
- •16.3 Жесткость воды
- •18 Комплексные соединения
- •18.1 Состав комплексных соединений
- •18.2 Реакции с участием комплексных соединений
- •19.8.1 Элементы триады железа
- •19.8.2 Платиновые металлы
- •20 Органические соединения
- •20.1 Углеводороды
- •20.2 Кислородсодержащие соединения
- •20.3 Амины и аминокислоты
- •21 Полимеры
- •21.1 Классификации полимеров
- •21.2 Полимеризационные полимеры
- •21.3 Поликонденсационные полимеры
- •21.4 Структура и состояние полимеров
- •22 Рабочие вещества низкотемпературной техники
- •22.2 Хладагенты органического происхождения
- •Список использованных источников
3.4 PH водных растворов
Ионное произведение воды
Запишем уравнение диссоциации воды:
H2O « H+ + OH– .
Отсюда
выражение константы равновесия (константа
диссоциации воды) имеет вид:
 .
.
Из значения константы диссоциации воды следует, что диссоциация воды
протекает незначительно и поэтому можно считать, что
[H2O]
=
 1000/(18·1)
= 55,6 моль/л.
1000/(18·1)
= 55,6 моль/л.
Тогда KH2O = [H+][OH–] = 1,8·10–16·55,6 = 1·10–14 (при 25 оС).
Произведение [H+][OH–] является постоянной величиной, которую называют ионным произведением воды.
[H+][OH–] = 10–14. (3.19)
Из ионного произведения воды следует, что концентрации ионов H+ и OH– взаимосвязаны, поэтому для характеристики среды можно использовать концентрацию только одного вида ионов. На практике используется концентрация ионов Н+.
В чистой воде [H+] = 10–7 моль/л,
в кислой среде [H+] > 10–7 моль/л,
в щелочной среде [H+] < 10–7 моль/л.
Концентрации ионов H+ и OH– могут меняться в очень широких пределах, поэтому в расчетах удобнее использовать не значения концентраций, а их логарифмы (lg). Отсюда получаем:
|
рН = –lg[H+]. |
(3.20) |
Значок «p» обозначает математическую операцию «–lg», а [H+] – молярную концентрацию ионов водорода.
рН – это отрицательный десятичный логарифм из молярной концентрации ионов водорода.
Шкала рН имеет следующий вид:
0 7 14
ا-----------------------ا--------------------------ا
кислая нейтральная щелочная среды.
Примеры расчетов рН в растворах сильных и слабых кислот и оснований
1 Рассчитать pH 0,1М раствора серной кислоты.
Решение
H2SO4 ® 2H+ + SO42–, [H+] = 2C(H2SO4) = 0,1·2 = 0,2 моль/л,
рH = –lg[H+] = –lg2 ·10–1 = –lg2 – lg10–1= –0,3 + 1 = 0,7.
2 Рассчитать pH 0,1М раствора гидроксида натрия.
Решение
NаОН ® Nа+ + ОН–, [ОH–] = C(NаОН) = 0,1 моль/л,
[H+] = KH2O / [ОH–] = 10–14/10–1 = 10–13 моль/л.
рH = –lg[H+] = –lg 10–13 = 13.
3 Рассчитать pH в 0,1М растворе Н2СО3.
Решение
Напишем уравнения диссоциации угольной кислоты:
Н2СО3 ↔ Н+ + НСО3– , Кд1 = 5·10–7;
НСО3– ↔ Н+ = СО32– Кд2 , = 5 ·10–11.
Расчет концентрации ионов водорода проведем только по первой ступени диссоциации:
[H+]
= 
 =
=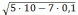
 =
2,2·10–4
моль/л.
=
2,2·10–4
моль/л.
Отсюда, рН = –lg 2,2·10–4 = –0,34 + 4 = 3,64.
Из полученных значений рН видно, что при одинаковой молярной концентрации сильные электролиты изменяют рН в значительно большей степени. При смешивании сильных и слабых кислот или оснований рН практически определяется диссоциацией сильного электролита.
Буферные растворы–это растворы, при добавлении к которым кислот или щелочей их pH меняется незначительно.
Буферными свойствами обладают:
1) растворы слабых кислот и их солей. Например:
СН3СООН + СН3СООNа – ацетатный буферный раствор;
2) растворы слабых оснований и их солей. Например:
NН4ОН + NН4Сl – аммонийный буферный раствор;
3) растворы кислых солей слабых кислот. Например, NаН2РО4.
4 Ионно-обменные реакции
Ионно-обменные реакции–это реакции обмена между ионами в результате которого образуются слабый электролит, осадок, газ или комплексное соединение.
