
- •Содержание
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные понятия химии
- •1.2 Основные законы химии
- •2 Основные классы неорганических соединений
- •2.1 Простые вещества
- •2.2 Сложные вещества
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.2 Способы выражения состава растворов
- •3.1.3 Физико-химические процессы образования растворов
- •3.1.4 Экстракция
- •3.2 Растворы неэлектролитов
- •3.2.1 Законы Рауля
- •3.2.2 Осмос
- •3.3 Растворы электролитов
- •3.3.1 Электролитическая диссоциация
- •3.3.2 Сильные и слабые электролиты
- •3.4 PH водных растворов
- •4 Ионно-обменные реакции
- •4.1 Необратимые ионно-обменные реакции
- •4.2 Обратимые ионно-обменные реакции
- •5 Гидролиз солей
- •5.1 Различные случаи гидролиза
- •2) Гидролиз соли образованной сильным основанием и слабой кислотой
- •3) Гидролиз соли образованной слабым основанием и слабой кислотой
- •5.2 Константа гидролиза
- •5.3 Смещение равновесия при гидролизе
- •6. Окислительно-восстановительные реакции
- •6.1 Составление уравнений окислительно-восстановительных реакций
- •6.2 Прогнозирование окислительно-восстановительных свойств веществ по степеням окисления элементов
- •6.3 Основные типы окислительно-восстановительных реакций
- •6.4 Взаимодействие металлов с водой, кислотами и щелочами
- •7 Гальванические элементы
- •7.1 Принцип работы гальванического элемента
- •7.2 Водородный электрод сравнения. Электрохимический ряд
- •8 Электролиз
- •8.1 Электролиз расплавов
- •8.2 Электролиз водных растворов
- •8.3 Количественные расчёты в электролизе
- •8.4 Химические источники электрической энергии
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •10 Термодинамика
- •10.1 Внутренняя энергия и энтальпия. Закон Гесса
- •Или через промежуточный продукт (со) в две реакции:
- •10.2 Энтропия
- •10.3 Энергия Гиббса
- •11 Химическая кинетика Химическая кинетика – учение о скоростях и механизмах протекания химических реакций.
- •11.1 Скорость реакции
- •Основные факторы, влияющие на скорость реакции:
- •Число частиц с энергией большей, чем Еа равно заштрихованной площади.
- •12.1.2 Модель атома по Бору
- •12.2 Современные представления о строении атома
- •13 Периодический закон и периодическая таблица д.И. Менделеева
- •14 Химическая связь и строение молекул
- •14.1 Химическая связь
- •14.1.1 Квантово-механическое описание модели молекулы водорода
- •14.1.2 Основные характеристики химической связи
- •Валентный угол–это угол между двумя химическими связями.Он отражает геометрию молекулы.
- •14.1.3 Типы химических связей Ковалентная связь –это связь между двумя атомами за счет образования общей электронной пары.
- •14.2 Состав и строение молекул
- •15 Типы кристаллических решеток
- •16.1 Общая характеристика s-элементов первой и второй групп
- •16.2 Свойства воды
- •16.2.1 Строение молекулы воды
- •16.2.2 Физические свойства воды
- •16.2.3 Химические свойства воды
- •16.3 Жесткость воды
- •18 Комплексные соединения
- •18.1 Состав комплексных соединений
- •18.2 Реакции с участием комплексных соединений
- •19.8.1 Элементы триады железа
- •19.8.2 Платиновые металлы
- •20 Органические соединения
- •20.1 Углеводороды
- •20.2 Кислородсодержащие соединения
- •20.3 Амины и аминокислоты
- •21 Полимеры
- •21.1 Классификации полимеров
- •21.2 Полимеризационные полимеры
- •21.3 Поликонденсационные полимеры
- •21.4 Структура и состояние полимеров
- •22 Рабочие вещества низкотемпературной техники
- •22.2 Хладагенты органического происхождения
- •Список использованных источников
20.2 Кислородсодержащие соединения
Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода заменены гидроксильными группами. К простейшим представителям спиртов относятся СН3–ОН – метиловый спирт (метанол), СН3–СН2–ОН – этиловый спирт (этанол) и т.д.
Производные на основе ароматических углеводородов с группой –ОН в бензольном ядре называются фенолами. Например, С6Н5–ОН – фенол.
Подобно молекулам воды молекулы низших спиртов соединяются между собой посредством водородных связей. Поэтому они имеют более высокие температуры кипения, чем соответствующие углеводороды.
Общим свойством спиртов и фенолов является способность замещения водорода гидроксильной группы на металл. Например,
2СН3–СН2–ОН + 2Nа → 2СН3–СН2–ОNа + Н2↑.
Кроме спиртов с одной гидроксильной группой известны спирты, молекулы которых содержат несколько гидроксильных групп (многоатомные спирты). Примерами таких спиртов могут служить двухатомный спирт этиленгликоль и трехатомный – глицерин:
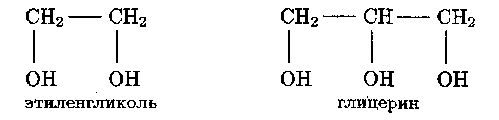
Этиленгликоль и глицерин – высококипящие жидкости, смешивающиеся с водой в любых отношениях.
![]()
В альдегидах к углероду карбонильной группы по одной связи присоединен атом водорода, а по второй – углеводородный радикал. К альдегидам также относится формальдегид (Н2С=О), у которого к углероду присоединены два атома водорода. В кетонах по двум связям к карбонильной группе присоединены углеводородные радикалы. Например,
СН3–СО –СН3 – пропанон (ацетон).
Карбоновые кислоты – это органические соединения, содержащие карбо–ксильную группу –СООН.
Примеры простейших карбоновых кислот:

Карбоновые кислоты подвергаются электролитической диссоциации:
СН3–СООН ↔ СН3–СОО– + Н+
и участвуют в реакциях нейтрализации:
СН3–СООН + NаОН ↔ СН3–СООNа + Н2О,
СН3–СООН + Nа+ + ОН– ↔ СН3–СОО– + Nа+ + Н2О,
СН3–СООН + ОН– ↔ СН3–СОО– + Н2О,
Уксусная кислота СН3–СООН – жидкость с острым раздражающим запахом (Ткип. = +118,1 °С). Другие представители летучих карбоновых кислот: бутановая (масляная), пентановая (валериановая), гексановая (капроновая) обладают неприятным запахам.
Простые эфиры – это соединения, молекулы которых состоят из двух
углеводородных радикалов, связанных посредством атома кислорода: R–О–R.
Простые эфиры образуются при межмолекулярной дегидратации спиртов. Например,
СН3–ОН + НО–СН3 → СН3–О–СН3(диметиловый эфир) + Н2О.
Сложные эфиры – это продукты взаимодействия карбоновых кислот со спиртами. Например,
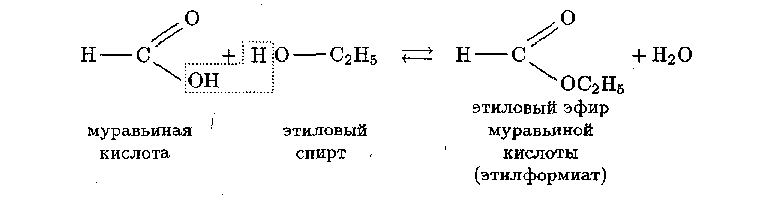
Реакцию образования сложных эфиров из кислоты и спирта называют реакцией этерификации.
Сложные эфиры подвергаются гидролизу с образованием вновь кислоты или соли и спирта. Реакция щелочного гидролиза сложных эфиров называется реакцией омыления. Например:

Многие сложные эфиры имеют приятный запах и часто встречаются в растениях, придавая аромат цветам, запах плодам и ягодам. Некоторые из сложных эфиров готовятся искусственно и под названием «фруктовых эссенций» широко применяются в кондитерском деле, в производстве прохладительных напитков, в парфюмерии.
Жиры – это сложные эфиры глицерина и карбоновых кислот. Приведем схему образования эфира при взаимодействии глицерина и стеариновой кислоты:

В состав твердых жиров входят главным образом эфиры предельных (пальмитиновой и стеариновой) кислот, а в состав жидких жиров (масел) – эфиры непредельных кислот. При присоединении водорода по двойным связям жидкие жиры превращаются в твердые. Такой процесс называют гидрированием или гидрогенизацией и применяют для получения из растительных масел пищевого маргарина.
Жиры подвергаются гидролизу (омылению). При гидролизе жира получаются глицерин и входящие в его состав кислоты.
