
- •Содержание
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные понятия химии
- •1.2 Основные законы химии
- •2 Основные классы неорганических соединений
- •2.1 Простые вещества
- •2.2 Сложные вещества
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.2 Способы выражения состава растворов
- •3.1.3 Физико-химические процессы образования растворов
- •3.1.4 Экстракция
- •3.2 Растворы неэлектролитов
- •3.2.1 Законы Рауля
- •3.2.2 Осмос
- •3.3 Растворы электролитов
- •3.3.1 Электролитическая диссоциация
- •3.3.2 Сильные и слабые электролиты
- •3.4 PH водных растворов
- •4 Ионно-обменные реакции
- •4.1 Необратимые ионно-обменные реакции
- •4.2 Обратимые ионно-обменные реакции
- •5 Гидролиз солей
- •5.1 Различные случаи гидролиза
- •2) Гидролиз соли образованной сильным основанием и слабой кислотой
- •3) Гидролиз соли образованной слабым основанием и слабой кислотой
- •5.2 Константа гидролиза
- •5.3 Смещение равновесия при гидролизе
- •6. Окислительно-восстановительные реакции
- •6.1 Составление уравнений окислительно-восстановительных реакций
- •6.2 Прогнозирование окислительно-восстановительных свойств веществ по степеням окисления элементов
- •6.3 Основные типы окислительно-восстановительных реакций
- •6.4 Взаимодействие металлов с водой, кислотами и щелочами
- •7 Гальванические элементы
- •7.1 Принцип работы гальванического элемента
- •7.2 Водородный электрод сравнения. Электрохимический ряд
- •8 Электролиз
- •8.1 Электролиз расплавов
- •8.2 Электролиз водных растворов
- •8.3 Количественные расчёты в электролизе
- •8.4 Химические источники электрической энергии
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •10 Термодинамика
- •10.1 Внутренняя энергия и энтальпия. Закон Гесса
- •Или через промежуточный продукт (со) в две реакции:
- •10.2 Энтропия
- •10.3 Энергия Гиббса
- •11 Химическая кинетика Химическая кинетика – учение о скоростях и механизмах протекания химических реакций.
- •11.1 Скорость реакции
- •Основные факторы, влияющие на скорость реакции:
- •Число частиц с энергией большей, чем Еа равно заштрихованной площади.
- •12.1.2 Модель атома по Бору
- •12.2 Современные представления о строении атома
- •13 Периодический закон и периодическая таблица д.И. Менделеева
- •14 Химическая связь и строение молекул
- •14.1 Химическая связь
- •14.1.1 Квантово-механическое описание модели молекулы водорода
- •14.1.2 Основные характеристики химической связи
- •Валентный угол–это угол между двумя химическими связями.Он отражает геометрию молекулы.
- •14.1.3 Типы химических связей Ковалентная связь –это связь между двумя атомами за счет образования общей электронной пары.
- •14.2 Состав и строение молекул
- •15 Типы кристаллических решеток
- •16.1 Общая характеристика s-элементов первой и второй групп
- •16.2 Свойства воды
- •16.2.1 Строение молекулы воды
- •16.2.2 Физические свойства воды
- •16.2.3 Химические свойства воды
- •16.3 Жесткость воды
- •18 Комплексные соединения
- •18.1 Состав комплексных соединений
- •18.2 Реакции с участием комплексных соединений
- •19.8.1 Элементы триады железа
- •19.8.2 Платиновые металлы
- •20 Органические соединения
- •20.1 Углеводороды
- •20.2 Кислородсодержащие соединения
- •20.3 Амины и аминокислоты
- •21 Полимеры
- •21.1 Классификации полимеров
- •21.2 Полимеризационные полимеры
- •21.3 Поликонденсационные полимеры
- •21.4 Структура и состояние полимеров
- •22 Рабочие вещества низкотемпературной техники
- •22.2 Хладагенты органического происхождения
- •Список использованных источников
21.3 Поликонденсационные полимеры
Поликонденсация – реакция образования полимера за счет отщепления от молекул мономеров низкомолекулярных веществ.
Фенолоформальдегидные смолы – это высокомолекулярные соединения, образующиеся в результате взаимодействия фенола (С6Н5ОН) с формальдегидом (Н2С=0). Образование фенолоформальдегидных смол происходит согласно схеме:

Полиэфирные смолы. Примером таких смол может служить полиэтилентерефталат – продукт поликонденсации двухосновной ароматической терефталевой кислоты с двухатомным спиртом этиленгликолем:
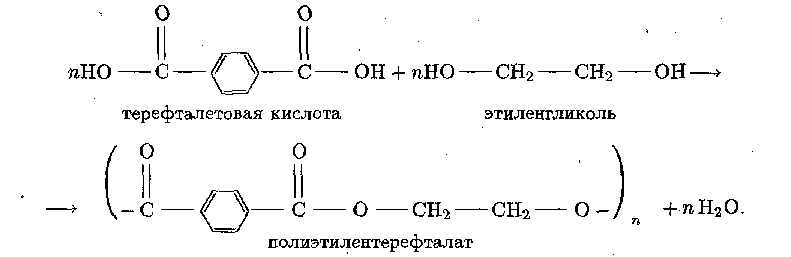
В нашей стране эту смолу выпускают под названием лавсан (за рубежом – терилен, дакрон). Из нее готовят волокно, напоминающее шерсть, но значительно более прочное, дающее несминаемые ткани. Лавсан обладает высокой термо-, влаго- и светостойкостью, устойчив к действию щелочей, кислот и окислителей.
Полиамидные смолы являются синтетическими аналогами белков. Полиамиды выдерживают нагрузки, близкие для цветных металлов. Применяются в качестве кордовых нитей автомобильных шин и для др. изделий.
21.4 Структура и состояние полимеров
Первичная структура определяется составом и последовательностью соединения элементарных звеньев, входящих в состав макромолекулы.
Вторичная структура определяется определенной конформацией в пространстве макромолекулы.
Третичная структура определяется объединением макромолекул в более сложные агрегаты.
По отношению к нагреванию полимеры делятся на термопластичные и термореактивные.
Термопластичные могут многократно при нагревании размягчаться, а при охлаждении затвердеть без существенного изменения своих свойств. К термопластичным полимерам относятся полиэтилен, полипропилен, полистирол, поливинилхлорид, фторопласт и другие полимеры линейного строения. Изделия из термопластичных полимеров можно изготовить обычным методом литья, а также сваривать нагреванием.
Термореактивные – при нагревании вначале размягчаются и реагируют с образованием пространственного полимера, который при последующем нагревании утрачивает способность размягчаться. Полимеры, у которых макромолекулы имеют пространственную сшитую структуру, не могут обратимо размягчаться и затвердевать, так как для этого требуется разрыв химических связей. Если же такой полимер нагреть до такой температуры, когда имеющиеся химические связи начнут разрываться, то сначала он приобретет некоторую подвижность, но затем начнется реакция с образованием более сложной пространственной структуры или его разложение. К ним относятся фенолформальдегидная, мочевиноформальдегидная и др. смолы.
Для полимеров такие агрегатные состояния, как кристаллическое, жидкое и газообразное, присущие низкомолекулярным веществам, не могут существовать из-за большой молекулярной массы.
При нагревании линейного термопластичного аморфного полимера до температуры разложения он будет последовательно приобретать следующие состояния:
1) стеклообразное; 2) высокоэластичное; 3) вязкотекучее.
Стеклообразное – по своей структуре подобно стеклу и в таком состоянии между макромолекулами полимера соблюдается только ближний порядок. Упругая деформация полимера в таком состоянии не превышает нескольких процентов. При снятии нагрузки полимер восстанавливается в своих размерах.
Высокоэластичное – полимер ведет себя как эластичное тело. Нагрузка вызывает деформацию полимера до 500÷800 %. При этом скрученные макромолекулы вытягиваются, но при снятии нагрузки макромолекулы полимера возвращаются в исходное состояние.
Вязкотекучее – под действием нагрузки возникает течение полимера, так как макромолекулы могут смещаться относительно друг друга. При снятии
нагрузки вязкая жидкость сохраняет полученную форму.
Переходы между различными состояниями носят плавный характер, так как полимер состоит из макромолекул с различной степенью полимеризации.
