
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Биохимия в рисунках и схемах
.pdf
мембрана
Глицерол-3-фосфат
Q
I |
Fe-S |
|
II |
||
|
||
НАДН НАД+ |
||
|
сукцинат |
|
SH2 |
матрикс |
|
изоцитрат |
митохондрии |
|
пируват |
||
|
||
малат |
|
|
глутамат |
|
|
и др. |
ацил-КоА |
|
Комплекс I – НАДН-дегидрогеназа –
флавопротеин, содержащий |
ФМН. Этот |
||
фермент окисляет |
НАДН и передает два |
||
водорода (2Н+2е-) на коэнзим |
Q. В комплекс |
||
входят также Fe-S-белки. |
|
||
Комплекс |
II – сукцинатдегидрогеназа – |
||
флавопротеин, содержащий |
ФАД. Этот |
||
фермент окисляет сукцинат и передает два |
|||
водорода (2Н+2е-) |
на коэнзим Q. В составе |
||
комплекса есть Fe-S-белки. |
|
||
В матриксе митохондрий находятся также |
|||
другие |
ФАД-зависимые дегидрогеназы, |
||
которые окисляют соответствующие субстраты (глицерол-3-фосфат, ацил-КоА) и передают далее водороды на коэнзим Q.
Потоки атомов водорода сливаются на стадии образования восстановленного КоQН2.
Коэнзим Q является последним компонентом цепи, который способен транспортировать как протоны, так и электроны ( 2Н+2е-). Далее протоны ( 2Н+) переходят с внутренней поверхности мембраны митохондрий на внешнюю, а электроны е- через цепь цитохромов переносятся на кислород.
Межмембранное
пространство
НАДНН НАД+ |
|
фумарат |
½ О2+2Н Н2О |
|
сукцинат |
|
|||
|
|
|
|
матрикс |
|
|
|
|
|
Комплекс III – убихинондегидрогеназа – ферментный комплекс, состоящий из цитохрома b, Fe-S-белка и цитохрома с1. Этот комплекс транспортирует электроны
2е- от восстановленного убихинона КоQН на цитохром |
с (небольшой по размерам |
||||||||
|
2 |
|
|
|
|
|
|
|
|
водорастворимый белок, находится на внешней стороне внутренней мембраны). |
|
||||||||
Комплекс IV – цитохром с-оксидаза – ферментный комплекс, |
|
|
|
|
|||||
состоящий из цитохромов а и а3. Эти ферменты осуществляют |
|
|
|
|
|||||
2е + ½ О |
|
|
О2- |
||||||
последнюю стадию биологического окисления |
– |
|
2 |
|
|||||
|
|
|
|
|
|||||
восстановление электронами 2е- молекулярного кислорода: |
|
|
|
|
|
||||
Восстановленный кислород О 2- взаимодействует со свободными протонами |
2Н+ |
||||||||
матрикса, в результате чего образуется вода: |
|
|
|
|
|
|
|
||
40 |
2Н+ + О2- |
|
Н О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
2 |
|
|
|
|
|
|
|
Комплекс I |
|
|
Q |
Комплекс III |
|
|
|
|
|
Комплекс IV |
|
|
|
||
ФМН FeS |
|
|
b FeS c1 |
|
|
с |
|
|
a a3 |
|
|
1/2О2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|||||
НАД+ |
|
|
|
|
Комплекс II |
2Н |
||
ФАД FeS |
|||
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Н2О |
|
SH2 |
|
SH2 |
|
|
|
||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||
Направление переноса протонов и электронов определяют окислительно- |
члены |
|||||||||
восстановительные потенциалы. Д ля обеспечения спонтанного переноса |
||||||||||
окислительно-восстановительного ряда |
должны располагаться в порядке |
|||||||||
возрастания потенциалов. |
|
|
|
|
||||||
|
|
|
|
|
|
Редокс-потенциал пары |
НАД+/НАДН = -0,32 в , что |
|||
-0,32 |
|
|
|
|
|
говорит о высокой способности отдавать электроны. |
||||
|
|
|
|
|
Редокс потенциал пары |
кислород/вода = |
+0,82 в , |
|||
|
|
|
|
|
|
что говорит о высоком сродстве к электронам. |
|
|
||
|
|
|
|
|
|
Общая разность редокс-потенциалов равна |
1,14 в , |
|||
|
|
|
|
|
|
этому соответствует изменение свободной энергии |
||||
|
|
|
|
|
|
G = -220 кДж/моль. Эта общая величина энергии |
||||
|
|
|
|
|
|
реакции разбивается на небольшие и более |
|
|
||
|
|
|
|
|
|
удобные |
«пакеты», величина которых |
|
|
|
|
|
|
|
|
|
определяется разностью окислительно- |
|
|
||
|
|
|
|
|
|
восстановительных потенциалов соответствующих |
||||
|
|
|
|
|
|
промежуточных продуктов. Предполагается, что |
||||
+0,82 |
|
|
|
|
|
это разделение на пакеты обеспечивает |
|
|
||
дыхательной цепи удивительно высокий выход энергии, составляющий примерно 60%.
О2 
 Дыхательная цепь митохондрий
Дыхательная цепь митохондрий 
 Н2О
Н2О
тепло |
энергия |
АДФ + Ф |
АТФ |
|
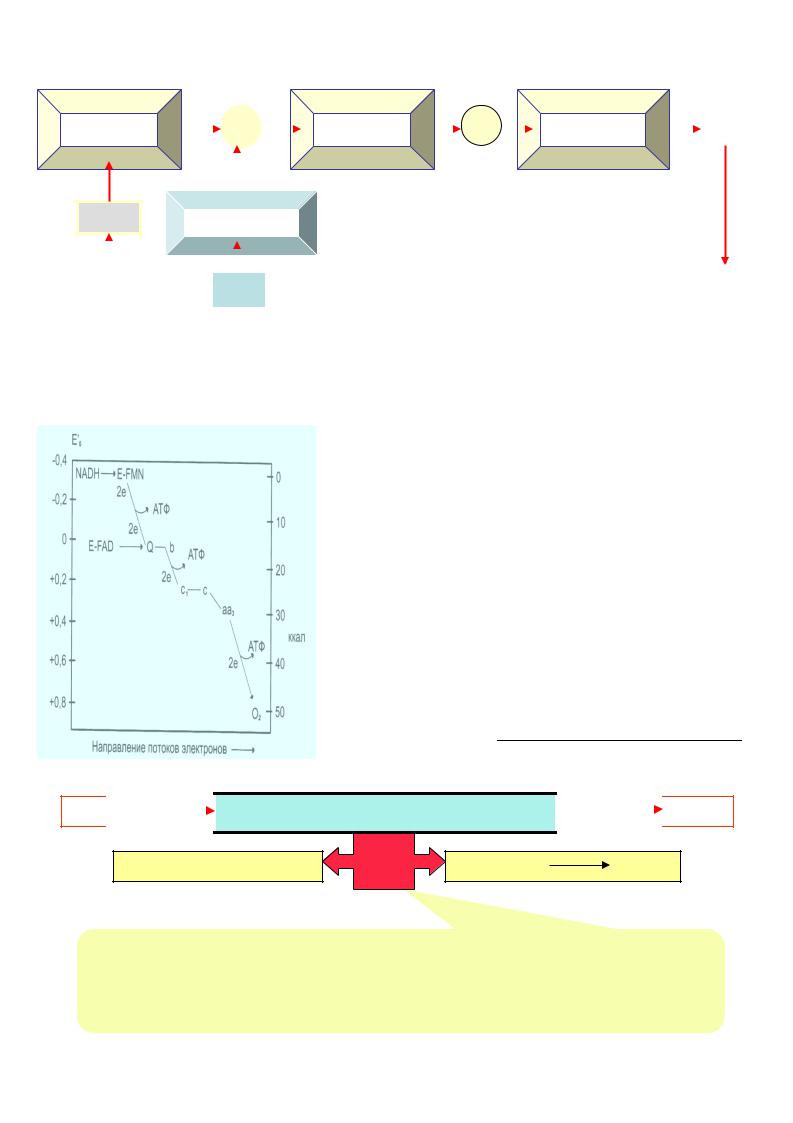
При прохождении по ЦПЭ пары электронов выделяется |
энергия, большая |
часть которой (60%) рассеивается в виде тепла, а остальная аккумулируется |
|
в макроэргических связях АТФ, т.е. поглощается в ходе |
реакции синтеза |
АТФ, т.е. окислительного фосфорилирования. |
41 |

Это фосфорилирование называется окислительным, т.к. энергия для образования макроэргической связи генерируется в процессе окисления, т.е. движения протонов и электронов по ЦПЭ.
VI. Механизм окислительного фосфорилирования
|
Н+ |
Н+ |
|
Н+ |
цит.с |
||
|
|||
|
|
межмембранное
пространство
|
|
|
|
фумарат |
|
½ О2+2Н+ |
Н2О |
|
|
||||||
|
|
сукцинат |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||
НАДНН НАД+ |
|
|
|
|
АДФ+Ф |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
||
|
матрикс |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
синтез АТФ |
|
|
|
|
|
Н+ |
||||
химический |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
потенциал рН |
|
|
электрохимический |
|
|
|
|
|
|
|
|||||
|
|
|
|
потенциал ΔµН+ |
|
|
|
|
АТФ-синтаза |
|
|||||
Основные переносчики электронов – комплексы I, III, |
IV – используя энергию |
||||||||||||||
электронов, обеспечивают перенос протонов |
Н+ из матрикса в межмембранное |
||||||||||||||
пространство. В результате понижается значение |
|
|
рН и возникает протонный |
||||||||||||
электрохимический потенциал ΔµН+ (хемиосмотическая теория П.Митчелла ).
Именно этот потенциал является движущей силой |
синтеза АТФ из АДФ и Ф. |
|
Синтез АТФ сопряжен с обратным потоком протонов |
Н+ из межмембранного |
|
пространства в матрикс. Внутренняя мембрана митохондрий для этого потока |
||
непроницаема. Осуществляется обратный поток протонов благодаря специальной |
||
ферментной системе, называемой протонная |
АТФ-аза или АТФ-синтаза (комплекс |
|
V). При достижении определенного значения |
ΔµН+ активируется АТФ-аза, в ней |
|
открывается канал, через который протоны возвращаются в матрикс из |
||
межмембранного пространства, а энергия |
ΔµН+ |
используется для синтеза АТФ. |
42 |
|
|
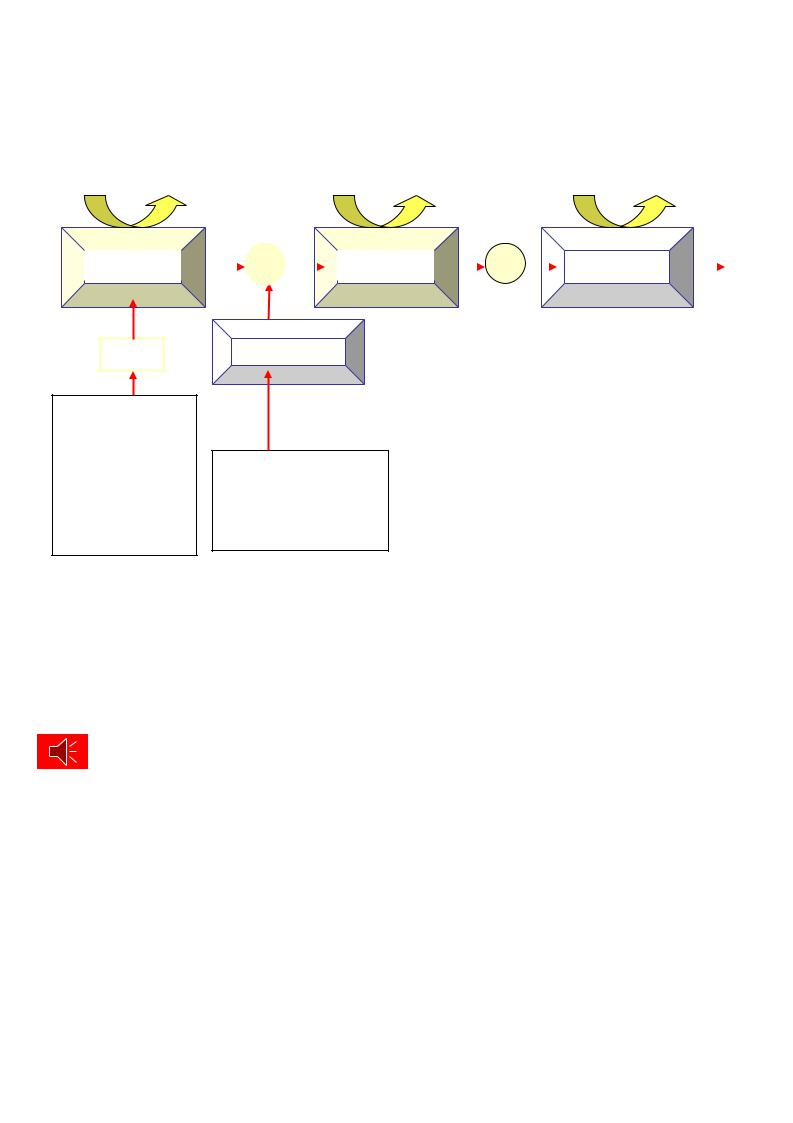
Каждый из трех комплексов ( |
|
I, III, |
IV) обеспечивает протонный градиент, |
|||||||||||||||||||||||
необходимый для активации АТФ-синтазы и синтеза 1 молекулы АТФ. |
|
|
|
|
||||||||||||||||||||||
|
|
|
|
АТ |
|
|
|
|
|
|
АТ |
|
|
|
|
|
АТ |
|||||||||
АДФ + Ф |
|
Ф |
|
|
АДФ + Ф |
|
Ф |
|
АДФ + Ф |
|
Ф |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
Комплекс I |
|
|
|
|
Q |
|
|
Комплекс III |
|
|
|
Комплекс IV |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
ФМН FeS |
|
|
|
|
|
b FeS |
c1 |
|
|
|
с |
|
|
a a3 |
|
|
|
О2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
Комплекс II |
Коэффициент окислительного |
|
|||
|
НАД+ |
ФАД |
FeS |
|
|||
|
|
|
|
фосфорилирования |
P/O – отношение |
||
SH2 |
(P/O = 3) |
|
|
количества фосфорной кислоты |
(Р), |
||
|
|
использованной на фосфорилирование, |
|||||
пируват |
|
|
к поглощенному кислороду (О). |
|
|||
α-кетоглутарат |
|
|
|
||||
SH2 |
(P/O=2) |
P/O зависит от точки вхождения |
|
||||
изоцитрат |
H2 |
||||||
|
малат |
сукцинат |
восстановительных эквивалентов |
||||
глутамат |
ацил-КоА |
от субстратов |
SH2 |
в цепь транспорта |
|||
|
лактат |
глицерол-3-фосфат |
электронов. |
|
|
|
|
Субстраты SH2, окисляемые НАД-зависимыми дегидрогеназами (пируват,
α-кетоглутарат, изоцитрат, малат, глутамат, лактат) являются более энергетически ценными, т.к. при их окислении образуется 3 АТФ ( P/O = 3), чем субстраты, окисляемые ФАД-зависимыми дегидрогеназами (сукцинат, ацил-КоА, глицерол-3- фосфат), при окислении которых образуется 2 моля АТФ (P/O=2).
Все описанные процессы переноса протонов и электронов и синтеза АТФ (тканевого дыхания и окислительного фосфорилирования) тесно сопряжены: они происходят только одновременно и скорость их меняется одновременно.
Процессы усвоения пищи и образования АТФ должны приспосабливаться к энергетическим потребностям клетки, т.е. производство и потребление АТФ должно быть согласовано.
При увеличении в клетке расходования АТФ повышается скорость поступления АДФ в митохондрии, а значит, растет скорость синтеза АТФ. Поэтому увеличивается скорость переноса протонов, т.е. возрастает скорость дыхания. Такая корреляция, т.е. ускорение окислительного фосфорилирования и дыхания при повышении концентрации АДФ называется дыхательным контролем. Другими словами, дыхательный контроль – это соотношение АТФ/АДФ : при его понижении интенсивность дыхания
увеличивается. |
43 |

В некоторых случаях сопряжение фосфорилирования и дыхания нарушается,
т.е. происходит |
«неконтролируемое» |
|
дыхание митохондрий. Это может |
|
|
происходить при |
повреждении мембраны |
|
митохондрий, а также при действии |
||
веществ, функционально разделяющих |
||
окисление и фосфорилирование |
– |
|
разобщающих агентов . Эти липофильные вещества (2,4-динитрофенол, жирные кислоты ) могут переносить протоны через мембрану митохондрий, минуя АТФазу, т.е. уничтожая протонный градиент. Природный разобщающий агент – белок термогенин, который является протонным каналом в митохондриях бурого жира.
При этом Р/О снижается, энергия
рассеивается в виде тепла.
1.Повреждение мембраны
2.Подвижные переносчики
норадреналин
жир ЖК
3.Управляемый протонный канал
термогенин
Ингибиторы электронного транспорта и окислительного фосфорилирования
1. Ингибиторы, блокирующие дыхательную цепь за счет связывания с определенными ферментами или коферментами на разных участках цепи. При этом Р/О снижается до нуля в зависимости от места действия ингибитора:
а) ротенон (инсектицид), барбитураты (снотворные), антибиотик пиерицидин А.
в) антимицин (антибиотик).
с) CN-, CO, H2S.
Ротенон, барбитураты а)
НАДН КоQ цит.b цит.с1 цит.с цит.аа3 О2
в)
антимицин
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НАДН |
|
КоQ |
|
цит.b |
|
|
|
цит.с1 |
|
цит.с |
|
цит.аа3 |
|
О2 |
|
|
|
|
|
|
|
|
с)
СN- или СО
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НАДН |
|
КоQ |
|
цит.b |
|
цит.с1 |
|
цит.с |
|
цит.аа3 |
|
|
О2 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||||
2. Ингибиторы окислительного фосфорилирования:
а) олигомицин – антибиотик, ингибирует функцию АТФ-синтазы (не действует на тканевое дыхание).
44

VII. Общие пути катаболизма
Окислительное декарбоксилирование пирувата
Этот процесс отщепления СО2 от пировиноградной кислоты и переноса ацетильного остатка на коэнзим А с образованием ацетил-КоА осуществляется с помощью
мультиферментного пируватдегидрогеназного комплекса (ПДГ).
В состав комплекса входят три фермента (Е1 , Е2 , Е3 ) и пять кофакторов:
|
тиаминпирофосфат |
(ТПФ) |
простетические группы - |
|
|||
|
липоевая кислота |
( ЛК) |
прочно связаны с |
|
|||
|
ФАД |
НАД |
апоферментами |
|
|
|
|
|
|
|
|
|
|
+ |
|
коэнзим А |
||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
(HS-КоА) |
|
коферменты – легко диссоциируют |
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
от апоферментов |
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
+НАД+ + НSКоА |
|
СО2+ацетил-SКоА+НАДН Н+ |
||
|
|
|
|
|
|
Пируват |
|||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О
Е1 –ТПФ катализирует отщепление СО2 от пирувата и перенос гидроксиэтильного остатка на ТПФ.
Е2 –ЛК переносит гидроксиэтильный остаток от ТПФ на простетическую группу – ЛК, при этом дисульфидная связь разрывается, а ацетильный остаток и водород
присоединяются к ЛК. Затем ацетильный остаток переносится с ЛК на |
НSКоА с |
образованием ацетил-SКоА, а ЛК восстанавливается до дигидро-ЛК. |
|
Е3-ФАД катализирует дегидрирование дигидро-ЛК, которая переходит в исходную окисленную форму, а водороды восстанавливают ФАД. На последней стадии
водороды переносятся на НАД+ с образованием НАДН Н+. |
45 |

VIII. Цикл трикарбоновых кислот
Цикл трикарбоновых кислот (цикл Кребса, цитратный цикл ) – это циклическая последовательность ферментативных реакций, в результате которых ацетил-SКоА (СН3СО SКоА) - продукт катаболизма белков, жиров и углеводов, окисляется до углекислого газа СО2 с образованием атомов водорода ( Н), которые используются для восстановления первичных акцепторов цепи переноса электронов: НАД+ и ФАД.
(С2)
(С6)
(С4) |
(С6) |
|
|
||
|
СО2 |
|
(С4) |
α- |
|
(С5) |
||
|
||
|
СО2 |
|
(С4) |
|
|
|
(С4) |
|
|
(С4) |
Метаболиты и ферменты ЦТК локализованы в матриксе и внутренней мембране митохондрий. Они функционально сопряжены с митохондриальными цепями переноса электронов. Поэтому восстановительные эквиваленты (4 пары водородов Н), образующиеся при окислении метаболитов цикла Кребса, через первичные акцепторы
НАДН Н + |
и |
ФАДН2 передаются в дыхательную цепь для восстановления атомов |
|||
кислорода |
О2 с образованием молекул |
Н2О. |
При этом образуется АТФ |
в ходе |
|
окислительного фосфорилирования. |
|
|
|
||
Ацетил-КоА |
– «активная уксусная кислота» |
(содержит 2 атома углерода |
С2), |
||
образуется при окислительном декарбоксилировании пирувата. В первой реакции она конденсируется с четырехуглеродным оксалоацетатом ( С4), при этом образуется шестиуглеродный цитрат ( С6). Затем от цитрата последовательно отщепляются два углерода в виде двух молекул СО2, в результате чего вновь регенерируется оксалоацетат (С4). Таким образом, суммарное уравнение ЦТК:
46 |
СН3СООН + 2Н2О |
|
2СО2 + 8Н |
|

1
SКоА конденсация
НSКоА
цитратсинтаза
8
дегидрирование
оксалоацетат |
|
цитрат |
|
|
|
2 |
а |
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|
|
|
||
|
дегидратация |
||||||
малат- |
ЦТК |
аконитаза |
|
|
|
|
|
дегидрогеназа |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
7
гидратация
малат |
|
|
|
фумараза |
|
цис-аконитат |
|
НАДНН+ |
аконитаза |
2в |
|
|
|
гидратация |
|
|
|
|
|
|
|
|
|
ФАДН2
фумарат |
|
|
|
|
изоцитрат-изоцитрат |
|
|||||||||||
|
|
|
|
сукцинат- |
|
|
|
|
3 |
||||||||
6 |
|
|
|
|
|
|
|
дегидрогеназа |
|
|
|||||||
|
|
|
дегидрогеназа |
|
|
|
|
|
декарбокси- |
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
дегидрирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лирование |
|
|
|
|
|
|
|
|
сукцинил- |
|
α-кето- |
СО2 |
|||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
глутарат- |
|
|
|
||||||
|
|
|
|
|
|
|
тиокиназа |
|
дегидрогеназа |
|
|
|
|||||
|
|
|
|
сукцинат |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
НSКоА |
|
SКоА |
|
НSКоА α-кетоглутарат |
|||||||||
|
|
|
|
|
ГТ |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
ГДФ+Ф |
|
СО2 |
|
|
|
|||||||
|
|
|
|
|
|
Ф |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
сукцинил SКоА |
|
|
|
|||||
|
|
5 |
|
|
|
|
|
|
|
|
4 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
субсратное |
|
|
|
|
|
|
|
|
окислительное |
47 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
фосфорилирование |
|
|
|
|
|
декарбоксилирование- е |
|||||||||

Энергетический баланс ЦТК
В ЦТК при окислении одной молекулы «активного ацетата» образуются восстановленные коферменты: 3 молекулы НАДН Н + и 1 молекула ФАДН 2. Они далее окисляются в дыхательной цепи, при этом за счет окислительного фосфорилирования образуется по 3АТФ на каждую НАДН Н + и по 2АТФ на ФАДН 2. Таким образом, за счет окислительного фосфорилирования образуется (3х3 + 2х1 = 11) АТФ.
Кроме того, в цикле Кребса имеется реакция субстратного фосфорилирования , в которой за счет расщепления макроэргической связи субстрата (сукцинил SКоА) образуется новое макроэргическое соединение - ГТФ. Далее ГТФ отдает свой фосфат на АДФ с образованием 1 молекулы АТФ . Таким образом, всего при окислении 1 моля ацетилКоА образуется (11 + 1 = 12) АТФ.
|
Регуляция ЦТК |
||||
пируват |
АТФ, ацетилКоА, НАДН, |
||||
|
|||||
пируват |
жирные кислоты |
|
|
|
|
дегидрогеназный |
АМФ, НSКоА, НАД+, Са2+ |
||||
комплекс |
|||||
ацетил-КоА |
|
|
|
||
|
АТФ, НАДН, сукцинил-КоА |
||||
|
АДФ |
|
|
|
|
цитрат |
цитрат |
|
Самым важным фактором |
|
|
синтаза |
|
регуляции цикла является |
|
||
|
|
|
соотношение НАДН/НАД+. |
|
|
оксалоацетат |
|
|
|
||
изоцитрат |
|||||
ЦТК |
|
АТФ |
|||
малат |
изоцитрат |
||||
|
|
|
|||
дегидрогеназа |
дегидрогеназа |
АДФ, Са2+ |
|||
НАДН |
|
|
|
|
|
малат |
α-кетоα-кетоглутарат |
||||
ФАДН2 |
глутарат- |
НАДН, сукцинил-КоА |
|||
|
дегидрогеназа |
Са2+ |
|||
|
|
||||
сукцинат |
сукцинил SКоА |
||||
дегидрогеназа |
|
|
|
|
|
|
ингибирование |
ГТФ |
активация |
|
|
48 |
|
Задания для самопроверки и самокоррекции
Задача 1.
Нарушение последовательности ферментов при реконструкции цепи тканевого
дыхания в эксперименте полностью блокирует его активность. Каким свойством компонентов необходимо руководствоваться в построении активной цепи переноса электронов?
А, Молекулярной массой В. Редокс-потенциалом С. Структурой кофакторов
D.Электрофоретической подвижностью.
Задача 2. Сопряжение тканевого дыхания с фосфорилированием требует
наличия градиента концентрации Н+ между двумя сторонами внутренней митохондриальной мембраны. Какую роль он играет в синтезе АТФ?
А. Катализирует реакцию синтеза АТФ
В. Активирует АТФ-синтетазу С. Участвует в образовании промежуточных высокоэнергетических соединений
Д. Способствует выделению энергии в дыхательной цепи
Е. Переводит компоненты дыхательной цепи в высокоэнергетическую форму
путем изменения их конформации.
Задача 3. Животные содержались на рационе, лишенном некоторых витаминов.
Отсутствие какого витамина приведет к нарушению активности дегидрогеназ тканевого дыхания?
А. РР В. Пиридоксина
С. Фолиевой кислоты D. Кобаламина
Е.. Рутина
Задача 4.Студенты в лабораторной работе in vitro исследовали действие малоната на ряд ферментов аэробного окисления глюкозы. Накопление, какого метаболита ЦТК они обнаружили?
А. Малата В. Цитрата
С. Лактата
D. Изоцитрата Е. Сукцината
Правильность решения проверьте, сопоставив их с эталонами ответов.
1-B, 3-A, 5-C.
49
