
Тройные диаграммы
.pdf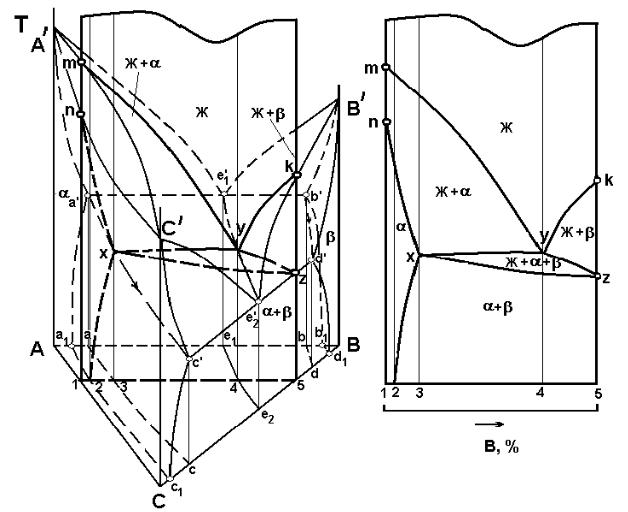
Рисунок 3.15 – Построение политермического (вертикального) разреза диаграммы состояния
Разрез имеет пять характерных сплавов, которые обозначены цифрами от 1 до 5. На рисунке 3.15 через эти точки проведены вертикальные линии. Ликвидус разреза состоит из двух кривых my и ky, отвечающих температу рам начала кристаллизации α и βрастворов соответственно. Точки m и k принадлежат ликвидусам соответствующих двойных систем АС и ВС. Со лидус разреза включает две кривые, одна из которых nx отвечает темпера турам конца кристаллизации αраствора, а вторая xz температурам конца кристаллизации эвтектики α+β. Видно, что вертикальная плоскость не пере секает поверхность солидуса тройного βраствора. Кривые xy и yz – это сле ды от сечения линейчатых поверхностей начала кристаллизации эвтектики α+β. Кривая x2 является следом от сечения вертикальной плоскостью по верхности сольвуса a1a′c′c1a1.
Аналогичным образом можно построить другие политермические раз резы диаграммы состояния. На практике используют разрезы построенные по экспериментальным и расчетным точкам.
60

Рассмотрим фазовые превращения в тройных сплавах системы. Сплав М расположен на эвтектической кривой е1е2 (см. рисунок 3.16,б). Он имеет две критические точки, которые обозначены на рисунке 3.16,а цифрами 1 и 2.
а |
б |
Рисунок 3.16 Кристаллизация сплава М: положение конодных треугольников и конод в пространстве (а) и в проекциях на плоскости концентрационного треугольника (б)
Первая точка принадлежит поверхности начала кристаллизации эвтек тики α+β, а вторая – поверхности конца кристаллизации этой эвтектики, ко торая одновременно является поверхностью солидуса. Таким образом, при охлаждении сплава М с температуры точки 0 первичные кристаллы α или β не выделяются. Кристаллизация этого сплава начинается с выделения эвтек тики α+β. При температуре Т1, соответствующей точке 1, жидкость состава y1′ становится насыщенной относительно кристаллов α и β. Состав первых эвтектических αкристаллов определяется точкой x1′, а βкристаллов – точ кой z1′. Эти две точки принадлежат кривым максимальной растворимости a′c′ и b′d′ соответственно.
Равновесие трех фаз в этот момент кристаллизации изображается ко нодным треугольником y1′x1′z1′. На рисунке 3.16,б изображена проекция это го треугольника y1x1z1. Кристаллизация эвтектики происходит в интервале температур от Т1 до Т2, так как вариантность системы равна с=33+1=1.
61

В процессе кристаллизации двойной эвтектики происходит перемеще ние конодного треугольника таким образом, что одна его вершин скользит по кривой двойной эвтектики, а две другие вершины по кривым предельной растворимости. Таким образом, состав жидкой фазы изменяется от точки y1′ до y2′, состав αраствора от точки x1′ до x2′, а состав βраствора от z1′ до z2′. Процесс кристаллизации двойной эвтектики α+β заканчивается, когда конода x2′z2′, соединяющая два твердых раствора, пересечет фигуративную линию 0М сплава М. Этому моменту соответствует положение конодного треуголь ника y2′x2′z2′, что подтверждает правило центра тяжести.
При понижении температуры от Т2 до Тком. изза уменьшения взаимной растворимости компонентов в твердом состоянии составы α и βфаз изме няются по кривым x2′x3 и z2′z3, принадлежащим поверхностям сольвуса a1a′c′c1a1 иb1b′d′d1b1 соответственно.
На рисунке 3.16,б показаны положения конод, конодных треугольни ков, кривых изменения составов фаз, соответствующих кристаллизации сплава М, в проекциях на плоскость концентрационного треугольника.
Сплав М имеет две фазы (α и β) и одну структурную составляющую – двойную эвтектику (α+β). Количество каждой фазы можно определить по правилу рычага
m = |
Mz3 |
× m ; m = |
Mx3 |
× m . |
|||
x z |
x z |
||||||
α |
сплава β |
сплава |
|||||
|
3 |
3 |
|
3 |
3 |
|
|
Кривая охлаждения сплава М и схема его микроструктуры при комнат ной температуре изображены на рисунке 3.17.
Рисунок 3.17 Кривая охлаждения сплава М и схема микроструктуры
62

Сплав 1 (рисунок 3.18), находящийся в области ae1e2ca, имеет три кри тические точки. Первая точка принадлежит поверхности ликвидус α раствора, вторая точка – поверхности начала кристаллизации двойной эвтек тики α+β, а третья точка – поверхности конца кристаллизации двойной эв тектики, одновременно являющейся поверхностью солидуса. В структуре сплава 1 можно обнаружить две фазы (α и β) и три структурные составляю щие: первичные αкристаллы, эвтектику α+β и вторичные βкристаллы.
Рисунок 3.18 Положение фигуративных точек сплавов и кривые охлаждения сплавов
Тройные сплавы, фигуративная точка которых принадлежит области e1bde2e1 (на рисунке 3.18 сплав 2), также имеют три критические точки. Структура этих сплавов состоит из первичных βкристаллов, двойной эвтек тики α+β и вторичных αкристаллов.
Сплавы областей Аa1c1CA(например, сплав 3) и b1Bd1b1 кристаллизу ются как α и βрастворы, при охлаждении в твердом состоянии не претерпе вают фазовых превращений и на кривых охлаждения имеют по две критиче ские точки.
Сплавы соседних областей a1acc1a1 (например, сплав 4) и bb1d1db также заканчивают кристаллизацию как α и βрастворы, но при охлаждении в твердом состоянии в результате вторичной кристаллизации становятся двух фазными. Они имеют по три критические точки. Под микроскопом в струк туре сплава 4 можно увидеть две структурные составляющие: первичные α и выделившиеся из них вторичные βкристаллы.
Примером диаграммы состояния рассмотренного типа служит диа грамма состояния системы золото – кремний – серебро (рисунок 3.19).
63

Рисунок 3.19 Диаграмма распределения фазовых областей в системе AuSiAg (данные экспериментальных исследований Куприной В.В.)
Основную часть диаграммы состояния занимает двухфазная область. Линия двойной эвтектики проходит приблизительно при 5% Si. Область тройного твердого раствора прилегает узкой полосой к стороне системы зо лото серебро.
Контрольные вопросы к подразделу 3.1.2
1.Нарисуйте в проекциях диаграмму состояния тройной системы АВС с моновариантным эвтектическим равновесием Жα+β, когда эвтектиче ский разрыв возникает в двух двойных системах АВ и ВС, а в третьей двойной системе АС компоненты образуют непрерывный ряд твердых рас творов.
2.Какие би и моновариантные фазовые равновесия характерны для рассматриваемой системы?
3.Перечислите все поверхности этой диаграммы состояния.
4.Что собой представляет поверхность ликвидуса этой тройной систе
мы?
5.Укажите проекции поверхностей ликвидусов α и βрастворов на плоскости концентрационного треугольника.
6.Какую кривую называют эвтектическим тальвегом?
7.Что представляет собой поверхность солидуса рассматриваемой тройной системы АВС? Укажите проекции солидусов α и βрастворов на плоскости концентрационного треугольника.
64
8. Какие линейчатые поверхности имеет диаграмма состояния системы АВС? Покажите проекции этих поверхностей на плоскости концентраци онного треугольника.
9.Объясните, как образуются поверхности начала кристаллизации двойной эвтектики α+β?
10.Как образуется поверхность конца кристаллизации двойной эвтек тики α+β?
11.Что представляют собой поверхности сольвуса в системе АВС? Укажите их проекции на плоскости концентрационного треугольника.
12.Перечислите рекомендуемые этапы построения изотермических разрезов диаграмм состояния тройных систем.
13.Какую информацию можно получить из изотермического разреза диаграммы состояния?
14.Перечислите рекомендуемые этапы построения политермических разрезов диаграмм состояния тройных систем.
15. Какую информацию можно получить из политермического разреза диаграммы состояния?
16.Рассмотрите кристаллизацию сплавов, фигуративная точка которых находится в различных областях концентрационного треугольника диаграм мы состояния рассматриваемой тройной системы. Сколько критических то чек имеет каждый сплав? Нарисуйте кривые охлаждения сплавов. Укажите фазовый состав сплавов и их структуру при комнатной температуре.
17.Какая реальная металлическая система относится к подобному типу диаграмм состояния?
Лекция 10
План лекции
Изображение диаграммы состояния в пространстве и проекциях. Анализ изотермических сечений диаграммы состояния.
3.2 Диаграмма состояния системы с моновариантным перитектическим равновесием
Рассмотрим случай равновесия, когда перитектический разрыв раство римости возникает в двух двойных системах, в то время как в третьей компо
65
ненты смешиваются во всех соотношениях как в жидком, так и в твердом со стоянии. Подобная ситуация имеет место в тройных системах NiPdRe, Ni PdRu, PtPdRu и др.
Диаграмма состояния тройной системы такого типа приведена на ри сунке 3.20.
Тройная система АВС с моновариантным перитектическим равнове сием Ж+β α несколько отличается от предыдущей системы с эвтектиче ским равновесием Ж α+β (см. лекции 8 и 9). Она ограничена двумя двой ными системами АВ и ВС перитектического типа и системой АС с непре рывными рядами жидких и твердых αрастворов. Стрелки показывают на правление понижения температуры. Граничный раствор на основе компонен та В обозначен β.
Область трехкомпонентного αтвердого (рисунок 3.20,а) ограничена поверхностями АА′sС′СА, АА′а′а1А, а1а′с′с1а1, СС′с′с1С и А′а′с′С′sА′, а об ласть βраствора – поверхностями b1b′B′Bb1, d1d′B′Bd1, b′B′d′b′ и b1b′d′d1b1.
Ликвидус системы состоит из двух поверхностей: поверхности начала кристаллизации αраствора A′p1′p2′C′ιA′ и поверхности начала кристаллиза ции βраствора p1′B′p2′p1′. Эти две поверхности пересекаются по перитекти ческой кривой p1′p2′. На диаграмме состояния, представленной в проекциях (рисунок 3.20,б), им соответствуют области Аp1p2CA, p1Bp2p1 и кривая p1p2.
Солидус системы имеет три поверхности. Поверхность А′a′c′C′A′ отве чает температурам конца кристаллизации αраствора (рисунок 3.20,а), по верхность b′В′d′b′– температурам конца кристаллизации βраствора (области AacCA и bBdb соответственно на рисунке 3.20,б). Для тройных сплавов, фи гуративная точка которых находится в области abdc (рисунок 3.20,б), соли дусом является линейчатая поверхность конца кристаллизации по перитекти ческой реакции. Образование этой поверхности будет рассмотрено ниже.
Перитектическая кривая p1′p2′ и кривые a′c′ и b′d′ изображают составы жидкости и граничных α и βрастворов, участвующих в перитектическом равновесии Ж+β α.
Между поверхностями ликвидуса β и солидуса αраствора расположе ны три промежуточные линейчатые поверхности.
Поверхность, отвечающая температурам начала перитектической реак ции Ж+β→α, образуется путем перемещения горизонтали p1′a′b′ двойной системы АВ в сторону понижения температуры (y1′z1′, y2′z2′, y3′z3′, рисунок 3.21,а). При этом один конец коноды «скользит» по перитектической кривой (точки y1′, y2′, y3′), а другой ее конец – по кривой b′d′ (точки z1′ ,z2′ z3′). Поло жение коноды всегда остается параллельным плоскости концентрационного треугольника.
Две линейчатые поверхности, отвечающие температурам конца пери тектической реакции Ж+β→α, можно получить путем перемещения частей p1′a′ и a′b′ горизонтали p1′a′b′двойной системы АВ в сторону более низких
66

температур. Для одной из этих поверхностей положения коноды соответст вуют прямым y1′x1′, y2′x2′, y3′x3′, а для другой прямым x1′z1′, x2′ z2′, x3′ z3′.
Все перечисленные прямые параллельны плоскости концентрационного тре угольника.
а |
б |
Рисунок 3.20 – Диаграмма состояния тройной системы с моновариантным перитектическим равновесием в пространстве (а) и проекция диаграммы состояния на плоскость концентрационного треугольника (б)
Врезультате образуется серия конодных треугольников (y1′x1′z1′, y2′x2′z2′, y3′x3′z3′), каждый из которых соответствует своей температуре (Tp1′>T> Tp2′). На рисунке 3.21,б изображены проекции этих конодных тре угольников.
Проекции рассмотренных линейчатых поверхностей на плоскость кон центрационного треугольника занимают области p1bdc p2p1, p1acp2p1 и abdca соответственно (рисунки 3.20,б и 3.21,б).
Впространственной диаграмме состояния (рисунок 3.20,а) через кри вые a′c′ и a1c1, b′d′и b1d1 проходят две поверхности сольвуса. Поверхность a1a′c′c1a1 характеризует переменную растворимость компонента В в компо нентах А и С, а поверхность b1b′d′d1b1 компонентов А и С в компоненте В. Эти поверхность проектируются на плоскость концентрационного треуголь ника в области a1ac c1a1 и b1bdd1b1 (рисунок 3.20,б).
67

а |
б |
Рисунок 3.21 – Образование линейчатых поверхностей в тройной системе АВС с моновариантным перитектическим равновесием
Рассмотрим изотермические сечения диаграммы состояния системы А В С, представленной на рисунке 3.20. Рекомендуемые этапы построения та ких разрезов рассмотрены выше (см. лекцию 8).
Построение изотермического разреза при температуре TB>Т1>Tp1′ пока зано на рисунке 3.22. Кривая 12 – это след от пересечения горизонтальной плоскостью поверхности ликвидуса βраствора, кривая 34 – изотерма соли дуса βраствора.
Аналогичным образом можно построить изотермические сечения и при других температурах (рисунок 3.23).
При температуре, соответствующей перитектической точке p1′ в двой ной системе АВ, на разрезе (рисунок 3.23,б) появляется трехфазная область Ж+α+β, которую представляет перитектическая горизонталь p1ab на стороне АВ треугольника. При температурах ниже точки p1′ трехфазная область представлена конодным треугольником (рисунки 3.23,в,г), к сторонам кото рого примыкают три двухфазные области Ж+α, Ж+β и α+β. Между областя ми Ж+α и α+β находится область αтвердого раствора. По мере понижения
68

температуры трехфазная область непрерывно смещается к стороне ВС, об ласть Ж+β сужается, а области Ж+α и α+β расширяются.
Рисунок 3.22 – Построение изотермического разреза
При температурах ниже Tp2′, но выше точки плавления компонента С, двухфазная область Ж+α отходит от области α+β и смещается к вершине С треугольника (рисунок 3.23,д).
Рисунок 3.23 – Изотермические разрезы диаграммы состояния, представленной на рисунке 3.20
69
