
- •Часть I. Введение в предмет 9
- •2.1. Организация хирургической помощи
- •Часть I I
- •Глава 3. Общий уход
- •4.6. Отделение реанимации и интенсивной терапии
- •Глава 5. Асептика
- •5.1. Виды и распространенность хирургической инфекции
- •Глава 6. Антисептика
- •Глава 7. Боль и обезболивание
- •I. Оценка общего состояния больных
- •II. Оценка объема и характера операции
- •III. Оценка характера анестезии
- •Глава 8. Переливание крови и ее компонентов
- •0(1)Ар а(н)в в(ш)а ab(IV)0
- •8.4. Трансфузионные средства
- •I. Прямое (непосредственное) переливание крови
- •II. Непрямое (опосредованное) переливание крови
- •III. Обратное переливание (реинфузия) крови
- •Глава 9. Водно-электролитные нарушения
- •9.1. Основные причины нарушений водно-электролитного баланса
- •Глава 10. Нарушения свертывания крови у хирургических больных и методы их коррекции
- •10.1. Коагуляционная система
- •Глава 11. Кровотечение
- •II. Вид кровоточащего сосуда:
- •III. Клинические проявления:
- •Глава 12. Питание хирургических больных
- •12.4.1.1. Зондовое питание
- •Глава 13. Эндогенная интоксикация в хирургии и принципы ее коррекции
- •13.1. Основные виды эндотоксикоза у хирургических больных
- •Глава 14. Неоперативная хирургическая техника
- •14.1. Десмургия
- •14.1.1. Основные перевязочные материалы
- •14.13, Б).
- •14.3.2.6. Пункция плевральной полости
- •Глава 15. Обследование хирургических больных
- •Глава 16. Критические нарушения жизнедеятельности у хирургических больных
- •Глава 17. Основы гнойно-септической хирургии
- •17.2.1. Фурункул
- •17.2.4. Рожа
- •17.4.2. Паротит
- •18.4. Травма груди
- •Повреждения живота
- •18.10.3. Электротравма
- •19.2.2. Лечение и профилактика тромбоэмболии венозных сосудов
- •19.4. Некроз
- •20.1. Общая характеристика опухолей
- •20.4. Клиническая диагностика опухолей
- •20.5. Лечение онкологических больных
- •22.1. Эхинококкоз
- •22.3. Аскаридоз
- •23.1. Пороки развития костей черепа
- •23.2. Пороки развития головного мозга
- •23.3. Пороки развития лица
- •26.1. Предоперационный период
17.2.4. Рожа
Рожа (erysipelas) — инфекционное заболевание, характеризующееся четко отграниченным острым воспалением всех слоев собственно кожи (реже — слизистой оболочки), лихорадкой, явлениями общей интоксикации.
Источником инфекции является человек, больной каким-либо стрептококковым заболеванием (ангиной, скарлатиной, рожей, стрептококковым фарингитом), а также здоровый носитель стрептококка. Контагиозность больных рожей невелика. Инфекция может передаваться через руки, перевязочный материал, инструментарий. В доасептический период развития хирургии рожа была одним из основных осложнений раневого процесса.
Внедрение возбудителя в кожу происходит из экзогенных или эндогенных источников. Входными воротами при экзогенном инфицировании являются различные микротравмы (ссадины, царапины, потертости), тогда говорят о первичной роже. Экзогенное инфицирование через рану, распространение стрептококка в кожу, непосредственно прилегающую к какому-либо гнойному очагу (фурункулу, карбункулу), приводит к развитию вторичной рожи, являющейся осложнением основного заболевания.
Из эндогенного источника (очага скрытой инфекции) стрептококк может быть занесен в кожу гематогенным путем. В развитии болезни играет
420
роль предрасположенность организма: аллергическое состояние, сенсибилизация к стрептококку. Патогенез развития первичной рожи как эндогенной инфекции предполагает следующие звенья: сенсибилизация к стрептококку вследствие латентной инфекции (носительства); нарушение гистоге-матического барьера под воздействием какого-либо фактора, снижающего неспецифическую резистентность организма (переохлаждение, интеркур-рентная инфекция) с транзиторной бактериемией; гематогенное внедрение стрептококка в кожу, при этом локализация очага воспаления определяется микротравмой или другими причинами, приводящими к нарушению трофики (ушиб, лимфостаз, хроническая венозная недостаточность, болезни кожи).
Вторичная рожа иногда также может развиваться гематогенным путем, локализуясь в областях, отдаленных от первичного гнойного очага. Чаще развитие вторичной рожи в отдалении от первичного гнойного очага обусловлено лимфогенным распространением инфекции.
Клиническая картина. С началом болезни в зоне инвазии инфекта развивается серозное воспаление ретикулярного слоя кожи, склонное к распространению по ходу лимфатических сосудов до подкожной клетчатки. Серозный экссудат содержит в основном нейтрофилы. В тканях, капиллярах и особенно в лимфатических сосудах содержится большое количество стрептококков. По мере распространения воспаление охватывает все слои кожи, сопровождаясь десквамацией и паракератозом эпидермиса. Описанные изменения характерны для эритематозной рожи.
При более тяжелом течении воспаления большое количество экссудата отслаивает эпидермис с образованием пузырей (булл), содержащих прозрачный, желтоватый экссудат, являющийся по сути чистой культурой стрептококка (буллезная рожа). В редких случаях экссудат приобретает геморрагический характер вследствие повышенной ломкости капилляров, пропотевания эритроцитов. По мере стихания воспаления количество экссудата постепенно уменьшается, отслоившийся эпидермис отторгается, и кожный покров восстанавливается за счет регенерации сосочкового слоя. При неблагоприятном течении рожи экссудат пузырей приобретает гнойный характер вследствие увеличения количества нейтрофилов либо присоединения вторичной инфекции при спонтанном вскрытии булл. Восстановление эпидермиса в этом случае задерживается, вследствие лизиса росткового слоя эпидермиса возможно формирование длительно незаживающих язв. Распространение гнойного экссудата на подкожную клетчатку означает развитие подкожной флегмоны. Такое течение болезни называется многими авторами флегмонозной рожей, однако правильнее считать его не отдельной формой рожи, а ее осложнением, ибо речь идет о поражении не только собственно кожи.
У ослабленных, истощенных больных, при наличии тяжелых нейротро-фических нарушений экссудат и токсины высоковирулентных стрептококков нарушают кровообращение кожи, что приводит к обширным некрозам (гангренозная, или некротическая, рожа).
Разрешение рожи нередко сопровождается остаточными явлениями: нарушением крово- и лимфообращения вследствие склероза лимфатических сосудов, нарушениями трофики кожи. Иммунитета после рожи не возникает, более того, у больных сохраняется или усиливается сенсибилизация к стрептококку. Рецидивная рожа возникает в период от нескольких дней до 2 лет после предыдущего заболевания, как правило, без предшествующей травмы, при воздействии разнообразных факторов общего и местного (например, переохлаждение) характера, снижающих уровень неспецифической
421

Рис. 17.4. Рожа, эритематозная форма.
а — кожа ушной раковины резко отечна и гиперемирована; б — отек, локальная гиперемия и инфильтрация кожи дистальной части голени.
резистентности организма. При возникновении рожи более чем через 2 года после предыдущего заболевания говорят о повторной роже, которая нередко имеет другую локализацию.
Инкубационный период длится в среднем 3—4 сут (от 12 ч до 5 сут). Продромальные явления (недомогание, слабость, головная боль) наблюдаются редко.
Заболевание в большинстве случаев начинается остро, с резко выраженных симптомов эндогенной интоксикации: быстрого повышения температуры тела до 39—41 °С с потрясающим ознобом, слабости, сильной головной боли, мышечных болей, тошноты, иногда рвоты. Исчезает аппетит, появляется бессонница; в тяжелых случаях возможны бред, судороги, менин-геальные симптомы. Отмечаются тахикардия, тахипноэ. У большинства больных определяется гепатолиенальный синдром. Температурная кривая в большинстве случаев постоянного типа, реже — ремиттирующего. При исследовании крови отмечаются умеренная нормохромная анемия, нейтро-фильный лейкоцитоз, эозинопения. Снижается суточный диурез, в моче определяется белок, при тяжелой интоксикации — гиалиновые и зернистые цилиндры, лейкоциты, эритроциты.
Спустя 12—24 ч от начала болезни появляются местные признаки: вначале жгучая боль, ощущение жара и напряжения, а затем эритема (пятно гиперемии) и отек пораженной области, быстро увеличивающиеся в размере. Эритема обычно равномерная, с четкими зазубренными в виде языков границами («географическая карта»), приподнимается над уровнем непораженной кожи. На участках, где кожа малоподвижна, плотно соединена с подлежащими тканями, гиперемия выражена слабо. Болезненность более интенсивна по периферии пятна. Местная температура повышена. По мере распространения процесса интенсивность гиперемии в центре поражения постепенно уменьшается. Перечисленные симптомы характерны для эрите-матозной формы рожи (рис. 17.4).
При эритематозно-буллезной роже на фоне описанной выше эритемы видны пузыри различной величины, заполненные серозным, геморрагическим или гнойным экссудатом (рис. 17.5).
Пузыри нередко вскрываются спонтанно, и пораженная поверхность кожи покрывается подсыхающим экссудатом, струпом. Буллезная рожа обыч-
422
..
\
а
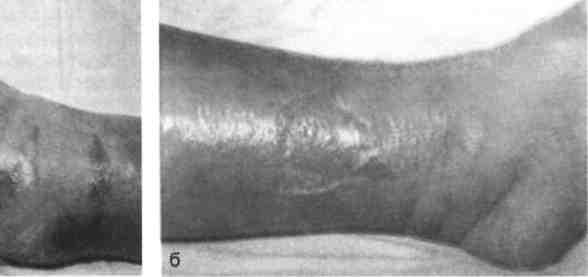
Рис. 17.5. Рожа, эритематозно-буллезная форма.
а — стопа и дистальная часть голени отечны, эпидермис на большом протяжении отслоен, под ним видны участки некротизированной дермы; б — кожа дистального отдела голени и части стопы гиперемирована, отечна, со вскрывшимися буллезными элементами и отслоенным эпидермисом.
но длится до 2 нед. По выздоровлении отечность и краснота кожи исчезают, возможно обильное шелушение. К остаточным явлениям относят пигментацию и пастозность кожи, поредение волос.
Эритематозно-геморрагическая форма рожи характеризуется появлением геморрагии на фоне эритемы, фибринозно-геморрагического выпота и пузыря. Наличие пузырей характерно для буллезно-геморрагической формы рожи {рис. 17.6).
Для некротической формы рожи характерно появление на площади эритемы багрово-синих либо черных участков различной формы, соответствующих очагам омертвения кожи и подкожной клетчатки (рис. 17.7).

Последующее отторжение погибшего эпидермиса обусловливает появление геморрагического экссудата, вследствие присоединения вторичной инфекции развивается флегмона подлежащих тканей с тяжелой интоксикацией и высоким риском генерализации инфекционного процесса.
Некоторые особенности клинических проявлений рожи связаны с локализацией очага воспаления. Рожистое воспаление на лице сопровождается значительным отеком, особенно век. При роже волосистой части головы гиперемия выражена слабо или может отсутствовать, выявляются лишь припухлость кожи, ее болезненность и симптомы интоксика-
Рис. 17.6. Рожа, буллезно-геморрагиче-ская форма: многочисленные буллезные элементы на коже лица, содержащие геморрагический экссудат.
J

Рис. 17.7. Рожа, некротическая форма.
ции. Локализуясь на туловище, рожа носит особо распространенный характер и протекает с тяжелой интоксикацией, нередко бывает ползучей либо мигрирующей. Под ползучей рожей понимают постепенное распространение («расползание») ее по поверхности кожи. Мигрирующей (блуждающей) рожей называют последовательное поражение различных участков кожи, отстоящих друг от друга на каком-либо расстоянии. Процесс «блуждания» рожи может продолжаться несколько недель и весьма истощает больных. При локализации на конечностях отмечаются преимущественно эритематозная и буллезная формы рожи с выраженными общими явлениями; с первых часов болезни появляются боли по ходу вен и лимфатических сосудов, что может привести к ошибочному диагнозу острого тромбофлебита. Рожистое воспаление мошонки и полового члена сопровождается выраженным отеком тканей, нередко — нарушением кровообращения и обширным некрозом кожи.
Рожистое воспаление слизистых оболочек (губ, зева, глотки) в настоящее время встречается редко. Местные симптомы рожи слизистых оболочек такие же, как и при поражении кожи: яркая отграниченная эритема, отечность, болезненность, возможно развитие пузырей.
Рецидивная рожа обычно протекает легче первичного заболевания: менее выражены симптомы интоксикации, эритема неяркая, крайне редко наблюдается гангренозная форма.
Осложнения рожи обусловлены дальнейшим развитием аутоиммунного процесса (общие для всех стрептококкозов — ревматизм, миокардит, гломе-рулонефрит) либо диссеминацией инфекции (флегмона подлежащей клетчатки, бурсит, тендовагинит, артрит, тромбофлебит, лимфангит и лимфаденит, сепсис). Следует помнить об опасности вторичного менингита при роже лица и волосистой части головы.
Диагностика рожи в типичных случаях нетрудна и основывается на характерных клинических признаках. Диагностика затруднена у резко ослабленных больных (отсутствие гиперемии), при роже волосистой части головы (эритема маскируется волосяным покровом), при «закрашивании» эритемы мазями (ихтиол) в процессе самолечения. В этих случаях диагностировать рожу позволяет обнаружение по периферии поражения кожи приподнятого резко болезненного воспалительного валика, наличие тяжелой интоксикации.
Дифференциальный диагноз рожи проводят с инфекционными эритемами, дерматитами, флегмоной, лимфангитом, эризипелоидом, в отдельных случаях — с сибирской язвой, обычным солнечным ожогом. Рожа отличается от эритем и дерматитов внезапным появлением общих симптомов с последующим развитием характерного пятна («географическая карта»), имеющего четко различаемый валик на границе со здоровой кожей. Кроме того, при роже отмечаются выраженная болезненность по периферии поражен-
424
ной кожи и тенденция к распространению очага, не свойственные эритемам и дерматитам. Дифференциация рожи с флегмоной также основывается на клинических признаках: при флегмоне болезненность, отек и краснота максимальны в центре очага поражения, воспалительный инфильтрат расположен глубже (в подкожной или межмышечной клетчатке) и плотнее рожистого инфильтрата, краснота неравномерна и не имеет четких границ. Выявление воспалительного инфильтрата в подкожной клетчатке, особенно с неравномерным размягчением его, при наличии четко отграниченной эритемы кожи позволяют диагностировать эритематозную рожу, осложнившуюся флегмоной. Лимфангиты отличаются от рожи гиперемией в виде полос или сетки соответственно характеру поражаемых лимфатических сосудов.
Лечение. При роже показана срочная госпитализация в хирургический стационар. Необходимы постельный либо палатный режим, иммобилизация пораженной конечности, высококалорийная мол очно-растительная диета с большим содержанием витаминов. Основой лечения является антибактериальная терапия.
Чаще всего рожу вызывают S. pyogenes, но встречаются и стрептококки групп В, С и D. Исследования последних лет показали возможность длительного персистирования стрептококков в стенках склерозированных лимфатических капилляров на месте очага воспаления. Эти факторы обусловливают высокую склонность болезни к рецидивированию.
При инфекции средней тяжести взрослым и детям старше 10 лет назначают фе-ноксиметилпенициллин, при тяжелом течении — бензилпенициллин, при аллергии на пен и циллины — эритромицин. Продолжительность лечения не менее 14 сут. В острых случаях быстрый эффект дает бензилпенициллин; спустя 36—48 ч его заменяют пероральными препаратами. При частых рецидивах рожи профилактически вводят бензатин бензилпенициллина по 2,4 млн ЕД 1 раз в 3—4 нед.
При часто рецидивирующей роже, остаточных явлениях после первого курса антибиотиков в течение 10 сут рекомендуют введение продигиозана (3 инъекции по 50—100 мкг с интервалом 3 дня) либо тималина, тимогена (по 10 мг через день) с целью иммуномодуляции и активации L-форм стрептококка. Затем проводят повторный курс антибактериальной терапии (6—7 сут), отдавая предпочтение тетра-циклинам либо макролидам. Такая схема имеет целью снижение частоты рецидивов рожи. Часто рецидивирующая рожа является показанием к проведению гормонотерапии (преднизолон по 30 мг в сутки, до 420 мг на курс) на фоне проводимой анти-биотикотерапии. Местное лечение проводят в соответствии с формой рожи.
При эритематозной роже применяют УФО зоны поражения в эритем-ной дозе (3—4 биодозы), обычно 4—5 сеансов; повязки не накладывают. При буллезной роже необходимо вскрыть пузыри, удалить отслоившийся эпидермис, после чего наложить влажно-высыхающую повязку с раствором антисептика; УФО в субэритемной дозе применяют при отсутствии гнойного экссудата. При некротической роже УФО не показано; требуется оперативное вмешательство, обычно в объеме некрэктомии; последующее местное лечение проводят в соответствии с принципами лечения гнойных ран.
При всех формах рожи противопоказаны повязки, тем более компрессы, с мазями на жировой основе. При выраженных симптомах интоксикации назначают инфузионную терапию, направленную на детоксикацию, коррекцию водно-электролитных и белковых нарушений, поддержание функций жизненно важных органов. Развитие осложнений рожи требует соответствующей коррекции лечебной программы. Исход рожи зависит от тяжести процесса, состояния больного, сопутствующих заболеваний, своевременно-
425
сти и правильности лечения. Летальность обычно связана с декомпенсацией имевшихся у больного нарушений функции жизненно важных систем (сердечно-сосудистая, печеночно-почечная). Прогноз значительно хуже при гангренозной роже и развитии осложнений.
Рецидивы рожи отмечаются у каждого 4-го больного. Каждый рецидив, усугубляя лимфостаз, может привести к образованию стойких отеков и даже к слоновости. Профилактика первичной рожи заключается в предупреждении и своевременной обработке микротравм, потертостей и строгом соблюдении правил личной гигиены. В предупреждении внутригоспитальной инфекции ведущая роль принадлежит строгому соблюдению правил асептики.
Профилактика рецидивов рожи, кроме указанных выше схем антибиоти-котерапии, предусматривает санацию очагов инфекции, повышение неспецифической резистентности организма.
17.2.5. Эризипелоид
Эризипелоид (рожа свиней, ползучая эритема) — острое медленно развивающееся инфекционное поражение кожи, вызываемое грамположитель-ной палочкой свиной рожи, обитающей в почве и разрушенном органическом субстрате. Относится к профессиональным заболеваниям и обычно возникает в результате проникающего ранения при ручной обработке продуктов животного происхождения — как съедобных (мясо, птица, рыба, устрицы), так и несъедобных (продукты переработки, кости, раковины моллюсков). После попадания на кожу в слое дермы развивается интенсивное воспаление. Микроорганизмы сосредоточиваются в глубоких слоях вокруг капилляров. На пальцах обычно появляется фиолетово-красное равномерное повреждение с неровными контурами. Отмечаются зуд и местное повышение температуры, но без лимфангита и лимфаденита. Может осложняться эндокардитом, артритом.
Основным возбудителем эризипелоида является Е. rhusiopathiae (повсеместно распространенная грамположительная сапрофитная палочка). Для подтверждения диагноза эризипелотриксозного артрита или эндокардита нужно выделить культуру из синовиальной жидкости или крови. Назначают бензилпенициллин или имипенем.
17.2.6. Абсцесс
Абсцесс (лат. abscessus — нарыв; син.: гнойник, апостема) — отграниченное скопление гноя в тканях или органах. Абсцессы локализуются чаще в подкожной клетчатке, реже — в клетчаточных пространствах. Образование абсцессов отмечается при гнойно-деструктивных поражениях легких, печени, головного мозга, предстательной железы и других паренхиматозных органов. Следует отметить, что гнойный процесс в стенке полого органа (желудка, кишки, бронха) протекает, как правило, по типу флегмонозного, и образование абсцесса в этих случаях нехарактерно.
Причиной подавляющего большинства абсцессов является внедрение микроорганизмов. Возбудители проникают в ткани вследствие повреждения кожи (микротравма, ранение, инъекция), инвазии в окружающие ткани из первичного очага — фурункула, лимфаденита, гидраденита. В этих случаях абсцесс развивается в области первичного инфицирования, и наи-
426
более частыми возбудителями являются стафилококки и стрептококки. Возникновение абсцесса на определенном удалении от первичного очага обусловлено гематогенным или лимфогенным метастазированием инфекции, и возбудитель абсцесса, как правило, идентичен микрофлоре первичного гнойного процесса. В развитии абсцессов некоторых паренхиматозных органов имеет значение нарушение дренажной функции их протоковой системы, и задерживающийся секрет играет роль питательной среды для микроорганизмов, проникающих в эту область гематогенным путем либо из сообщающихся с протоковой системой мест естественного обитания. В последнем случае абсцесс вызывается, как правило, эндогенной микрофлорой и является полимикробным заболеванием.
В редких случаях абсцесс возникает вследствие попадания в ткани веществ, вызывающих их некроз (например, керосина, скипидара), и является вначале «асептическим» процессом. Однако чаще наблюдается присоединение вторичной инфекции.
Возникновению абсцесса способствуют различные местные (ушиб, гематома) и общие факторы (гиповитаминоз, переохлаждение, кровопотеря), снижающие уровень неспецифической резистентности и в конечном итоге — уровень обсемененности тканей, достаточный для развития инфекционного процесса.
Клиническая картина. В начальной стадии воспаления происходит инфильтрация тканей серозным экссудатом и лейкоцитами. Затем под влиянием лейкоцитных и микробных ферментов ткани расплавляются, и образуется полость, заполненная гнойным экссудатом, т. е. абсцесс. Стенками абсцесса являются некротизированные ткани, фибрин, «лейкоцитарный вал». По мере развития демаркационных процессов вокруг гнойной полости формируется грануляционная ткань, являющаяся основой пиогенной мембраны. Последующее течение болезни обусловлено взаимоотношениями инвазивности и патогенности микрофлоры с уровнем резистентности организма. При достаточной степени защитной реакции организма пиогенная мембрана обеспечивает долговременное отграничение гнойной полости, и в результате созревания грануляционной ткани образуется второй, наружный, слой пиогенной мембраны, представленный зрелой соединительной тканью; абсцесс приобретает хроническое течение. Хронический абсцесс может подвергнуться инкапсуляции, т. е. вокруг него формируется плотная рубцовая капсула. Это сравнительно редкий вариант благоприятного течения. Чаще пиогенная мембрана формируется не полностью, имеет дефекты, и гнойный процесс распространяется на окружающие ткани, а микроорганизмы и их токсины в большом количестве поступают в лимфатическое или кровеносное русло. В этих случаях абсцесс осложняется флегмонозным поражением окружающих тканей, лимфаденитом, тромбофлебитом, артритом либо развивается генерализованная форма инфекции — сепсис.
Гнойное расплавление окружающих тканей может привести к спонтанному опорожнению абсцесса на поверхность тела, в просвет близлежащего полого органа или полости. Если образующийся путь оттока гнойного экссудата (свищ) обеспечивает хорошее дренирование абсцесса, а пиогенная мембрана еще не имеет соединительнотканного слоя, то вследствие очищения и рубцевания полости может наступить выздоровление. Однако чаще дренирования через образовавшийся узкий свищ недостаточно, сохраняются гнойное воспаление и расплавление тканей и рассчитывать на заживление не приходится.
Клиническая картина абсцесса складывается из местных и общих проявлений инфекционного воспаления. Местные признаки зависят от глубины
427
расположения гнойной полости от поверхности тела. При подкожной локализации абсцесса имеются типичные симптомы воспаления: покраснение кожи, припухлость, болезненность при пальпации, местное повышение температуры; в той или иной степени нарушается функция (ограничиваются движения). Характерным симптомом абсцесса является флюктуация, или зыбление: при толчкообразной пальпации колебания, передаваемые через жидкость (гной), ощущаются на противоположной поверхности. Чем глубже от кожи расположен абсцесс, тем менее выражены местные признаки воспаления. При подфасциальном, межмышечном, поднадкостничном абсцессе может совершенно отсутствовать гиперемия, припухлость незначительна и имеет разлитой характер. Флюктуация, как правило, не определяется, так как колебания жидкости не ощутимы через слой мышц. Для абсцессов внутренних органов указанные местные признаки воспаления совершенно нехарактерны; их эквивалентом в клинической картине являются симптомы сдавления и нарушения функции соответствующих органов, систем.
Общие проявления инфекционного процесса при абсцессах составляют синдром эндогенной интоксикации. Больные жалуются на общую слабость, снижение аппетита, нарушение сна, головную боль. Выявляются тахикардия, повышение температуры тела, нередко со значительными колебаниями в течение суток (более 1,5 °С) и ознобом. Выраженность симптомов интоксикации прямо зависит от величины абсцесса и вирулентности микрофлоры. При глубоком расположении гнойной полости общие симптомы воспаления нередко выходят на первый план.
Диагноз абсцесса основывается в первую очередь на клинических данных. Обнаружение флюктуации на фоне местных и общих симптомов воспаления является исчерпывающим для диагностики поверхностных, подкожных абсцессов. При глубокой локализации гнойного очага, когда симптом флюктуации, как правило, отсутствует, необходимы рентгенологические, ультразвуковые исследования с целью выявления отграниченного скопления жидкости (гноя). Значение диагностической пункции невелико, так как, во-первых, при поверхностных абсцессах она не требуется, во-вторых, пункция глубоких абсцессов «вслепую» может дать ложноотрицатель-ный результат (игла не проникает в гнойную полость). Кроме того, диагностическая пункция, как инвазивный метод исследования, может привести к осложнениям (инфицирование тканей, повреждение сосуда, нерва, париетальной серозной оболочки, внутреннего органа).
Лечение. Диагноз абсцесса независимо от его локализации означает необходимость срочного оперативного вмешательства. Целями операции являются эвакуация гнойного экссудата, санация и дренирование гнойной полости. Поверхностный (подкожный) абсцесс вскрывают линейным разрезом, длина которого соответствует диаметру гнойной полости. После удаления гноя рану исследуют с целью выявления гнойных затеков. Обнаруженные в полости абсцесса тканевые перемычки разделяют; для опорожнения гнойных затеков бывает необходим дополнительный разрез. Удаляют тканевые секвестры, иссекают некротизированные ткани, рану промывают раствором антисептика. Операция завершается, как правило, наложением повязки с водорастворимой мазью либо раствором антисептика. Такое вмешательство — вскрытие и хирургическая обработка абсцесса — может быть выполнено под инфильтрационной анестезией. При выраженном перифокальном отеке и гиперемии тканей, развитии регионарного лимфангита, лимфаденита предпочтительна проводниковая анестезия или общее обезболивание (внутривенный наркоз). Глубоко расположенные абсцессы вскрывают не-
428
большим разрезом, по возможности в проекции нижнего полюса гнойной полости, через который эвакуируют гной и пальцем исследуют гнойную полость, разделяют тканевые перемычки. При большом размере гнойной полости или обнаружении гнойных затеков расширяют разрез либо выполняют другой в проекции затека или противоположного полюса абсцесса. По возможности производят некрэктомию, после чего рану дренируют одним или несколькими перфорированными трубками, через которые налаживают приточно-отсасывающее дренирование.
При хронических абсцессах санация гнойной полости включает также иссечение стенки абсцесса, представленной Рубцовыми тканями. В некоторых случаях абсцесс иссекают единым блоком с окружающими тканями (резекция пораженного органа) без вскрытия гнойной полости; такая операция заканчивается наложением швов на рану с обязательным приточно-отсасывающим дренированием. В послеоперационном периоде проводят лечение с учетом фазности раневого процесса. Общее лечение включает применение антибиотиков, дезинтоксикационную и иммунотерапию.
17.2.7. Флегмона
Флегмона (греч. phlegmone — жар, воспаление) — разлитое гнойное воспаление клетчатки и клетчаточного пространства. В зависимости от локализации воспаления различают флегмоны поверхностные (подкожные, или эпифасциальные) и глубокие; среди последних выделяют межмышечные (субфасциальные) и флегмоны клетчаточных пространств. Флегмоны некоторых локализаций имеют свои названия, например воспаление околопочечной клетчатки — паранефрит, околокишечной клетчатки — параколит, околопрямокишечной клетчатки — парапроктит, клетчатки средостения — медиастинит. По характеру экссудата выделяют серозную, гнойную, гнилостную флегмоны; в случаях преобладания некротических процессов говорят о некротической флегмоне. Чаще флегмона локализуется в подкожной клетчатке, что связано с большой частотой травмы (в том числе микротравмы) и возможностью инфицирования.
Флегмона может быть самостоятельным заболеванием — первичная флегмона, или осложнением имеющейся хирургической инфекции — панариция, карбункула, абсцесса, лимфаденита, гнойного артрита, остеомиелита — вторичная флегмона.
Микробы проникают в клетчатку при повреждении (в том числе микротравме) кожи, слизистых оболочек. Глубокие (субфасциальные) флегмоны чаще развиваются вследствие ранений, инъекций. Воспаление клетчаточных пространств обусловлено обычно нарушением целости слизистых оболочек близлежащих органов в результате травм, воспалительно-дегенеративных или опухолевых заболеваний. Реже встречается гематогенное инфицирование клетчатки.
Наиболее частыми возбудителями первичных поверхностных флегмон являются гноеродные микроорганизмы — стафилококки, стрептококки.
Этиология флегмон, развивающихся вследствие повреждения слизистых оболочек, во многом обусловлена микрофлорой близлежащих полых органов. Так, например, из гнойных очагов, локализующихся в околопрямокишечной клетчатке, постоянно высеваются ассоциации грамотрицательных колиформных бактерий и анаэробов. При флегмонах шеи и средостения часто обнаруживают неклостридиальные анаэробы, для которых полость рта является местом их естественного обитания.
429
Флегмонозное воспаление может развиваться при случайном, а иногда преднамеренном введении в клетчатку некоторых лекарственных (хлорид кальция) и химических (скипидар, бензин) веществ, вызывающих некроз тканей. Инфекционный процесс в этих случаях развивается вторично.
Воспалительный процесс в клетчатке не имеет выраженной тенденции к отграничению и характеризуется наклонностью к дальнейшему распространению по протяжению рыхлой клетчатки с образованием гнойных затеков. Это связано с относительно малым количеством кровеносных сосудов и соединительнотканных элементов в клетчатке, что обусловливает ее слабую сопротивляемость инфекции.
Клиническая картина. На первом этапе развития флегмоны воспалительный экссудат распространяется в пределах фасциального футляра, клетча-точного пространства. Серозная инфильтрация тканей сопровождается повышением внутритканевого давления, которое, сдавливая сосуды, ухудшает перфузию клетчатки. Ишемия усугубляется вследствие тромбоза мелких кровеносных сосудов, развивающегося под воздействием некоторых бактериальных токсинов. Флегмонозное воспаление распространяется как по ходу подкожной клетчатки, так и вглубь, проникая в другие фасциальные футляры по паравазальной клетчатке, что ведет к возникновению вторичной, подфасциальной флегмоны. В ишемизированных тканях микроорганизмы находят благоприятные условия для своего развития, и ко 2—4-му дню заболевания экссудат приобретает гнойный, а иногда гнилостный характер, что усугубляет степень поражения тканей. Обычно наблюдается гнойное пропитывание клетчатки. Абсцедирование флегмоны (образование гнойной полости) может происходить при гноеродной микрофлоре и нехарактерно для гнилостных, некротических и анаэробных форм флегмоноз-ного воспаления. Микробные токсины и продукты распада тканей в большом количестве попадают в кровеносное русло и обусловливают развитие синдрома эндогенной интоксикации.
Клиническая картина флегмоны вариабельна и зависит от локализации воспалительного очага, вида микрофлоры, характера экссудата. Кроме того, выраженность клинических симптомов обусловлена стадией воспаления. В клинической картине флегмонозного воспаления принято различать местные симптомы воспаления и синдром эндогенной интоксикации. Подкожные (эпифасциальные) флегмоны, вызванные возбудителями гноеродной инфекции, проявляются типичными местными признаками воспаления. Заболевание начинается остро: появляются боль, припухлость в зоне поражения, гиперемия кожи над инфильтратом, не имеющая четких границ, местное повышение температуры. Боль усиливается при движениях, поэтому при локализации флегмоны на конечности наступает сгибание в суставах. Из общих симптомов инфекционного процесса типичны недомогание, слабость, головная боль, повышение температуры тела до 40 °С с ознобом. При исследовании крови обнаруживают нарастающий лейкоцитоз, нейтро-филез, увеличение СОЭ. С развитием гнойно-некротической стадии флегмонозного воспаления местные признаки претерпевают типичные изменения: воспалительный инфильтрат, плотноэластичный в начальной стадии, размягчается, в ряде случаев появляется флюктуация; гиперемия кожи над очагами размягчения и флюктуации сменяется синюшной окраской; боль приобретает тупой постоянный характер, но сила ее может уменьшиться. Нередко выявляются сопутствующие флегмоне регионарный лимфаденит, лимфангит, тромбофлебит. Нарастают общие проявления инфекционно-воспалительного процесса: появляются суточные колебания температуры, превышающие 1,5 °С и сопровождающиеся ознобами; усиливаются одыш-
430
ка, тахикардия; нередко отмечается тенденция к артериальной гипотензии. В крови нарастает лейкоцитоз, обнаруживается выраженный сдвиг лейкоцитарной формулы влево, появляются юные и незрелые формы нейтрофи-лов. Клиническое течение флегмоны редко бывает благоприятным; часто встречаются злокачественные формы, когда процесс быстро прогрессирует, захватывая обширные участки подкожной, межмышечной клетчатки, и сопровождается тяжелой интоксикацией.
Осложнения флегмон являются следствием диссеминации инфекционного процесса (лимфангит, лимфаденит, тромбофлебит, рожа, вторичные гнойные затеки, сепсис) или гнойно-некротического расплавления окружающих тканей (гнойный артрит, тендовагиниты). Особенно опасным осложнением является гнойный артериит с последующим разъеданием сосудистой стенки и возникновением вторичного аррозивного артериального кровотечения. Некоторые осложнения свойственны особым локализациям флегмоны. Так, флегмона лица, глазницы может осложниться гнойным менингитом, флегмона шеи — отеком голосовой щели и удушьем или распространением процесса в средостение с возникновением вторичного гнойного медиастинита.
Диагноз флегмон основывается в первую очередь на оценке местных признаков воспаления. Диагностика поверхностных флегмон не вызывает особых затруднений. Диагностика гнойно-некротической стадии воспаления (определение показаний к оперативному вмешательству) в большинстве случаев основана на выявлении размягчения инфильтрата и флюктуации, которым сопутствуют изменения лейкоцитарной формулы крови. С учетом давности и динамики заболевания этих критериев обычно бывает достаточно для постановки правильного диагноза. В тех случаях, когда подкожная флегмона возникает вторично (лимфаденит, остеомиелит, гнойный артрит и др.), при постановке диагноза следует выявлять и основное заболевание. Распознавание глубоких флегмон нередко затруднительно даже для опытного хирурга. Резкая и разлитая болезненность, наличие плотного воспалительного инфильтрата в глубине тканей, нарушение функции, высокая температура и другие симптомы интоксикации заставляют заподозрить развитие глубокой флегмоны и являются показанием к госпитализации больного в хирургический стационар. Глубокие флегмоны следует дифференцировать с глубоким тромбофлебитом, гематогенным остеомиелитом, артериальным тромбозом. От сосудистых поражений их отличает значительно большая болезненность при глубокой пальпации тканей в пределах фасциальных границ определенной мышечной группы; на проекции сосудистого пучка особой болезненности не отмечается, сохранена пульсация магистральных артерий. Кроме того, для артериального тромбоза, тромбофлебита нехарактерны высокая лихорадка и выраженные изменения картины крови. Наибольшие трудности возникают при дифференцировании с гематогенным остеомиелитом. Умеренный отек конечности, ограничение движений и болезненность при пальпации тканей, лейкоцитоз и изменения формулы крови встречаются при обоих заболеваниях. Рентгенологические признаки поражения кости при остеомиелите часто отсутствуют в первые 2—3 нед, а болезненная нагрузка по оси конечности выявляется не всегда. В сомнительных случаях рекомендуются диагностическая пункция мягких тканей, пункция костномозгового канала, ультразвуковое исследование с целью обнаружения скопления гноя; допустим разрез для прямой ревизии тканей.
Лечение больных с флегмонами осуществляют только в условиях стационара; амбулаторное лечение недопустимо. Лишь в начальной стадии флег-
431
моны (стадия серозного воспаления) допустимо консервативное лечение. Оно включает постельный режим, иммобилизацию конечности. Основу консервативной терапии составляет применение антибиотиков. Назначают 1—2 препарата широкого спектра действия в максимальных дозах, используя внутривенное, внутримышечное либо регионарное введение. Показано введение протеолитических ферментов (трипсин или химотрипсин по 5— 10 мл 2 раза в сутки внутримышечно). Местно применяют «сухое тепло» (УВЧ, соллюкс). Одновременно назначают противовоспалительные, сердечные средства, а при явлениях интоксикации — обильное питье, дезинтокси-кационную терапию. Отсутствие положительной динамики болезни в течение 1—2 сут консервативного лечения является показанием к оперативному вмешательству.
На стадии гнойно-некротического воспаления показано неотложное оперативное вмешательство; отсрочка его недопустима. Операцию выполняют под общим обезболиванием (местное обезболивание возможно как исключение при хирургическом лечении ограниченных подкожных флегмон). Производят вскрытие и хирургическую обработку флегмоны. Анатомически обоснованный разрез должен обеспечивать полноценную ревизию тканей в очаге воспаления и проведение адекватной хирургической обработки раны. При обширных флегмонах нередко требуется несколько параллельных разрезов. Хирургическая обработка включает эвакуацию гнойного экссудата, иссечение некротизированных и пропитанных гноем участков клетчатки и фасций, вскрытие и санацию гнойных затеков, дополнительную санацию раны с применением ультразвука, вакуумирования, пульсирующей струи антисептика или с обильным промыванием раствором антисептика. Операция завершается дренированием раны и наложением повязки с мазью на водорастворимой основе, либо с сорбентом, либо с протеолитическим ферментом или раствором антисептика. После адекватной по объему операции обычно быстро снижается температура, улучшается общее состояние, стихают местные симптомы воспаления, что позволяет использовать ранний вторичный шов. В специализированных лечебных учреждениях после вскрытия и хирургической обработки флегмон, вызванных гноеродной микрофлорой, допускается проведение проточно-аспирационного дренирования с наложением первичного шва на операционную рану. Однако при сложной конфигурации гнойной полости, нерадикальной хирургической обработке раны, а также при анаэробной этиологии флегмоны наложение первичного шва категорически запрещается.
Особенностью оперативного вмешательства при флегмоне новорожденных является нанесение множественных разрезов (насечек) не только в зоне поражения, но и обязательно на границе со здоровыми участками, а также захватывая 1,5—2 см здоровой поверхности. Это позволяет уменьшить отек в пограничной зоне и отграничить распространение процесса. Спустя 6—8 ч после операции выполняют перевязку, во время которой оценивают динамику процесса. Если отмечается дальнейшее распространение очага, немедленно вновь наносят множественные мелкие разрезы, также захватывая здоровые участки кожи.
При тяжелой форме прогрессирующей флегмоны, безуспешности оперативного и общего лечения в связи с угрозой для жизни больного показана ампутация конечности.
В послеоперационном периоде обязательно применяют антибиотики; их выбор и сочетание зависят от предполагаемого возбудителя или его точной идентификации. Коррекцию антибиотикотерапии проводят после получения результатов бактериологического исследования. При выраженных яв-
432
лениях интоксикации назначают инфузионную терапию, проводят детокси-кацию с использованием форсированного диуреза, гемосорбции, плазмафе-реза; по показаниям переливают кровь, ее компоненты, проводят иммунотерапию. Первые после операции перевязки нередко требуют общей анестезии. Во время перевязки необходимо тщательно осмотреть рану, выявить и санировать все гнойные затеки, повторно обработать раневую поверхность ультразвуком, струей антисептика. После полного очищения раны накладывают вторичный шов, а при обширных дефектах кожи выполняют аутодермопластику.
Прогноз зависит от своевременности лечения и степени развития септических явлений. При ограниченной форме подкожной флегмоны прогноз обычно благоприятный. При прогрессирующей флегмоне, тяжелых осложнениях ее и при локализации флегмоны на лице прогноз серьезен.
17.3. Гнойные заболевания клетчаточных пространств 17,3.1. Флегмона шеи
Флегмона шеи нередко развивается в связи с наличием очагов инфекции в кариозных зубах, при ангине, фарингите, ларингите, тиреоидите, гнойных заболеваниях слюнных желез, кожи лица и волосистой части головы, детских инфекционных болезнях, а также при ранении пищевода, глотки, гортани.
Флегмона шеи может локализоваться в любом клетчаточном пространстве ее. Обычно протекает остро, за исключением так называемой деревянистой флегмоны Реклю. Особенности анатомического строения шеи способствуют быстрому распространению гнойного процесса с одного клетча-точного пространства на другие и даже на средостение, в полость черепа, подмышечную ямку, подключичную ямку, на переднюю грудную стенку. Так, гнойный процесс, локализующийся между поверхностной и собственной фасциями, может спуститься ретромамиллярно; процесс, развившийся между висцеральным и париетальным листками внутришейной фасции, — распространиться в загрудинное пространство и средостение, а процесс, локализующийся между висцеральным листком внутришейной фасции и предпозвоночной фасцией, — в заднее средостение. При поражении клетчатки сосудисто-нервного пучка гной распространяется в средостение, а также в подключичную и подмышечную области.
Клиническая картина. Особенности клинического течения флегмон шеи зависят от локализации процесса и определяют выбор метода оперативного вмешательства.
Поверхностная (подкожная) флегмона шеи проявляется гиперемией, болезненностью и отечностью кожи. Повышаются местная температура и температура тела. Гнойный очаг локализуется, как правило, под подкожной мышцей шеи, плотно соединяющейся с кожей. Поверхностную флегмону шеи вскрывают поперечным или продольным разрезом, проведенным до собственной фасции шеи, и дренируют. С целью профилактики воздушной эмболии следует щадить наружную яремную вену, лежащую под кодкожной мышцей.
Флегмона ложа грудино-ключично-сосцевидной мышцы часто возникает вследствие мастоидита. Она проявляется выраженным болевым синдромом и припухлостью (колбасовидным набуханием) в области мышцы. Голова
433
больного сначала наклонена в сторону поражения, а в дальнейшем при расплавлении мышцы принимает нормальное положение (симптом Войно-Ясенецкого). Фасция, окружающая мышцу, долго препятствует распространению гноя. При разрушении переднего листка фасции гной распространяется под подкожную мышцу шеи, при разрушении заднего листка — в сосудистое и предвисцеральное клетчаточные пространства и далее в средостение. Гнойный очаг вскрывают продольным разрезом над пораженной мышцей, щадя наружную яремную вену.
Флегмона надгрудинного клетчаточного пространства возникает вследствие лимфаденита или остеомиелита рукоятки грудины. Проявляется болезненной припухлостью и сглаженностью контуров в области яремной вырезки грудины, наличием так называемого воспалительного воротника. При разрушении передней стенки надгрудинного клетчаточного пространства гной проникает в подкожную клетчатку. Большую опасность представляет разрушение задней фасциальной стенки, при котором гнойный процесс может проникнуть за грудину и далее в средостение. Гной распространяется также по ходу передних яремных вен под нижние отделы грудино-ключично-сосцевидных мышц и далее в средостение, в надключичную и подмышечную области. Поэтому ранняя операция при такой флегмоне служит профилактикой тяжелейших гнойных осложнений.
Подчелюстная и подбородочная флегмоны проявляются припухлостью и резкой болезненностью в соответствующей области, усиливающейся при открывании рта и жевании, наличием гнилостного запаха изо рта. При флегмоне подчелюстной области процесс может локализоваться в подкожной клетчатке или толще подчелюстной железы и сопровождаться ознобом, резкой интоксикацией, гектической лихорадкой.
Флегмона клетчаточного пространства сосудисто-нервного пучка шеи возникает чаще при ангине. Она проявляется резкой болезненностью по ходу грудино-ключично-сосцевидной мышцы, в области которой определяется плотная припухлость, положительным симптомом Войно-Ясенецкого. Гной скапливается в фасциальном влагалище сосудисто-нервного пучка, откуда он может непосредственно перейти в средостение, а при разрушении фасциальной стенки влагалища — в предвисцеральное и позадивисце-ральное пространства. Разрушая фасциальное влагалище по заднему краю грудино-ключично-сосцевидной мышцы, гной распространяется в надключичную область. Опасными осложнениями этой флегмоны являются аррозия крупных сосудов с профузным кровотечением и тромбоз внутренней яремной вены. Вследствие давления воспалительного инфильтрата на гортань, глотку и пищевод нередко наблюдаются расстройства дыхания и глотания.
При флегмоне предвисцерального пространства гнойный процесс локализуется между трахеей и гортанью сзади грудиноподъязычных и спереди грудинощитовидных мышц. На передней поверхности шеи развивается болезненная припухлость, голова больного несколько запрокинута назад, движения резко болезненны; часто наблюдаются расстройства дыхания и глотания, цианоз лица.
Флегмона позадивисцерального пространства чаще развивается при ранении и закрытых повреждениях пищевода (инструментальные исследования, инородные тела). Возникнув в параэзофагеальной клетчатке, гнойно-некротический процесс в связи с высокой вирулентностью микрофлоры (часто это неклостридиальные анаэробы) быстро распространяется в средостение, нередко осложняясь аррозивным кровотечением из сонной артерии и остеомиелитом позвонков.
434
Рис. 17.8. Разрезы, применяемые для 1

вскрытия флегмон шеи [Гостищев В. К.,
1996].
1 — подбородочная флегмона; 2 — подниж-нечелюстная флегмона; 3 — окологлоточный абсцесс; 4, 5 — флегмона сосудистого влагалища в нижнем (4) и верхнем (5) отделах; 6 — разрез по Кютнеру; 7 — разрез по де Кервену; 8 — флегмона бокового треугольника шеи; 9 — предтрахеальная флегмона и гнойный струмит; 10 — надгрудинная меж-апоневротическая флегмона.
Хроническая неспецифическая флегмона шеи (деревянистая флегмона Реклю) наблюдается обычно у ослабленных больных и бывает вызвана слабовирулентной микрофлорой. Клинически она проявляется плотным, деревянистым инфильтратом, иногда занимающим всю шею, который покрыт отечной, синюшной кожей. Наряду с подкожной клетчаткой поражаются и глубокие клетчаточные пространства, что может обусловливать расстройства дыхания и глотания.
Лечение. Хирургическое вмешательство при флегмонах шеи сводится к вскрытию и дренированию гнойников {рис. 17.8).
Вскрытие флегмоны надгрудинного клетчаточного пространства осуществляют продольным разрезом от яремной вырезки грудины до щитовидного хряща. Можно использовать и поперечный доступ между передними краями грудино-ключично-сосцевидных мышц на 2 см выше грудины.
При вскрытии гнойника предвисцерального пространства разрез проводят от щитовидного хряща до яремной вырезки рукоятки грудины. Гнойный процесс из этого клетчаточного пространства легко может проникнуть в средостение, поэтому разрез ведут книзу до здоровых тканей и обеспечивают отток гноя из самой низкой точки гнойника. При флегмонах, обусловленных ранением гортани и трахеи, показана трахеостомия.
При анаэробной флегмоне подкожной клетчатки (анаэробный целлюлит) обычно не наблюдается сплошного поражения клетчатки; периферические гнойные очаги в виде гнезд локализуются на различном удалении от основного очага и могут быть окружены неизмененной клетчаткой. Поэтому при лечении подкожной флегмоны используют множественные разрезы, обеспечивающие вскрытие всех очагов или предупреждающие дальнейшее распространение гнойного процесса. При анаэробной флегмоне более глубоких отделов шеи процесс может распространяться на все клетчаточные пространства шеи. В этом случае наиболее радикальной является операция Дьяконова. Разрез начинают под нижней челюстью на стороне поражения, отступя от нее на 2 см, и ведут по переднему краю грудино-ключично-сосцевидной мышцы; не доходя 2 см до ключицы, разрез поворачивают кзади и проводят параллельно ключице до трапециевидной мышцы. В нижнем отделе доступа пересекают грудино-ключично-сосцевидную мышцу, достигая в конечном итоге широкого вскрытия всех клетчаточных пространств шеи.
Гнойный очаг подчелюстной и подбородочной областей вскрывают разрезом, параллельным нижнему краю нижней челюсти, отступя от него на 2 см книзу и не доходя до переднего края жевательной мышцы, где проходят
435
лицевые артерия и вена. При подбородочной флегмоне разрез проводят между подбородком и подъязычной костью.
Разрез для вскрытия флегмоны клетчаточного пространства сосудисто-нервного пучка проводят по внутреннему краю грудино-ключично-сосце-видной мышцы от угла нижней челюсти до яремной вырезки рукоятки грудины. В тех случаях, когда гной прорывается в область заднего края груди-но-ключично-сосцевидной мышцы, разрез осуществляют по этому краю мышцы от ключицы до границы верхней и средней трети мышцы, щадя выходящий здесь из-под мышцы добавочный нерв (при повреждении этого нерва отмечается наклон головы больного в здоровую сторону и некоторый поворот в сторону поражения). В сосудистое ложе нередко прорывается гной при гнойном паротите; такой затек должен быть вскрыт.
Вскрытие флегмоны позадивисцерального пространства осуществляют по Разумовскому — разрезом по переднему краю грудино-ключично-сосцевид-ной мышцы.
При оперативном вмешательстве деревянистой флегмоны Реклю производят множественные разрезы с целью вскрытия всех клетчаточных пространств шеи.
17.3.2. Субпекторальная флегмона
Субпекторальная флегмона локализуется под грудными мышцами — большой и малой, где расположены два пространства — субпекторальные поверхностное и глубокое. Нагноительный процесс может развиться как первичное заболевание в случаях ранений и открытых травм, но обычно является следствием распространения инфекции из очагов первичного гнойного поражения; иногда развивается по механизму аденофлегмоны или гнойного затека из подмышечной впадины.
Для клинической картины характерны припухлость в зоне большой грудной мышцы, пальпация которой резко болезненна, сглаженность подключичной ямки, ограничение движений в плечевом суставе. Симптомы флюктуации не определяются по причине значительной толщины мышцы. По той же причине отсутствуют другие признаки инфекционного воспаления — краснота, местное повышение температуры. Больной на стороне поражения приводит плечо к грудной клетке; попытка отведения плеча резко усиливает боль. Даже при сравнительно небольших местных проявлениях наблюдаются высокая температура тела с ознобами, изменение формулы крови, другие явления тяжелой интоксикации организма. При длительно существующих гнойных процессах флегмона мигрирует под лопатку.
Тщательный осмотр, пальпация необходимы для определения места наибольшего скопления гноя и места проведения оперативного разреза. В комплексном лечении флегмоны основным является раннее широкое вскрытие гнойника разрезом по наружному краю большой грудной мышцы, при необходимости с наложением контрапертур и адекватное его дренирование (рис. 17.9).
17.3.3. Флегмона конечности
При глубоких флегмонах конечностей процесс гнойного воспаления распространяется по клетчаточным пространствам, рыхлой жировой клетчатке, расположенной под фасцией и между мышцами. Глубокие флегмоны встре-
436
Рис. 17.9. Субпекторальная флегмона 1

(вскрытие и дренирование).
I — скопление гноя под грудными мышцами (заштриховано); 2 — разрез по нижнему краю большой грудной мышцы, через который в полость гнойника проведен оконча-тый дренаж (3). Через два дополнительных разреза у верхнего полюса гнойника (контрапертуру) с помощью корнцанга (4) проведена вторая дренажная трубка.
чаются значительно реже подкожных и по своей этиологии могут быть первичными и вторичными, экзогенными и эндогенными. Глубокие первичные экзогенные флегмоны развиваются при попадании возбудителей через те или иные повреждения кожи, а также при воздействии внешних агентов (ранения, ожоги, инъекции). Эндогенные глубокие флегмоны вторичного происхождения являются следствием проникновения возбудителей через кровеносные и лимфатические сосуды, затеков гнойного отделяемого, а также прорывов гнойников, сопутствующих остеомиелитам, пандактилитам, тендовагинитам.
На плече глубокая флегмона распространяется по влагалищам сосудисто-нервного пучка, по ложам сгибательных и разгибательных мышц. В верхней части плеча флегмона может локализоваться под дельтовидной мышцей, в нижней части — в ложе плечелучевой мышцы с распространением на латеральную часть предплечья. Флегмона может распространяться и по фасциальным пространствам плеча по ходу лучевого, локтевого нервов и попадать в ложе разгибателей. При расположении в ложе сгибателей плеча флегмону вскрывают через параллельные разрезы по краям двуглавой мышцы. К ложу разгибателей доступ обеспечивается двумя параллельными разрезами по задней поверхности плеча; мышцы раздвигают тупым путем. При глубокой флегмоне, развившейся в фасциальном влагалище сосудисто-нервного пучка, разрез рекомендуется производить над двуглавой мышцей кнаружи и кпереди от проекции артерии; мышцу разделяют пальцем или тупым инструментом. Если глубокие флегмоны плеча контуриру-ются, возможен прямой доступ к гнойной полости.
В пределах предплечья имеются три фасциальных ложа — сгибательных мышц, разгибательных мышц, наружное ложе. Соотношение этих анатомических пространств изменяется в зависимости от уровня предплечья. Наружное ложе, содержащее сухожилия, отделено плотной фасциальной пластинкой, которая не дает возможности гнойному экссудату распространяться на окружающие ткани. По ложу сгибателей, разгибателей флегмона распространяется на другие пространства. Глубокий отдел ложа сгибателей делится межкостной мембраной на передний и задний отделы. В заднем отделе нижней трети предплечья содержатся сухожилия. Между квадратным пронатором и поверхностными сухожилиями сгибателей расположено пространство Пирогова—Парона. В нем может локализоваться глубокая флегмона, сообщающаяся со срединным клетчаточным пространством кисти. Оперативный доступ обеспечивается из разрезов, параллельных проекции сосудов как по передней, так и по задней поверхности предплечья. Кожу и фасцию рассекают острым путем, а мышцы, сухожилия расслаивают тупо.
437
На бедре имеются три основных фасциальных пространства — ложе сгибателей, ложе разгибателей, ложе приводящих мышц. Важную роль в распространении глубоких флегмон на бедре играет бедренный треугольник, расположенный под пупартовой связкой. Здесь поверхностные флегмоны имеют возможность распространяться вглубь по межмышечным пространствам. По ложу приводящих мышц бедра гнойные процессы, мочевые затеки могут мигрировать из области таза; по задней поверхности бедра — из ягодичной области, параректальной клетчатки. Глубокие флегмоны, сопутствующие остеомиелиту бедренной кости, возникают на любом уровне в зависимости от места прорыва гнойного очага кости. При гнойных артритах тазобедренного, коленного суставов глубокие абсцессы и флегмоны чаще локализуются между головками m. quadriceps femoris в зоне их сухожильного прикрепления. При локализации глубокой флегмоны бедра в ложе его сгибателей продольные разрезы наносятся до переднелатеральной поверхности; межмышечные промежутки рассекают до кости. Когда флегмона локализуется в ложе приводящих мышц, разрезы производят до пе-реднемедиальной либо по внутренней поверхности бедра; приводящие мышцы расслаивают тупым путем. При локализации флегмоны в заднем ложе и клетчатке по ходу п. ischiadicus прибегают к длинным разрезам по средней линии задней поверхности бедра.
На голени различают три фасциальных ложа — переднее, заднее, наружное.
По ходу клетчатки, окружающей основной сосудисто-нервный пучок голени, глубокие межмышечные пространства бедра соединяются со стопой. При развитии глубоких флегмон в переднем, наружном клетчаточных пространствах создается опасность сдавления сосудов и нарушения кровообращения вплоть до некроза отдельных мышечных групп.
При глубокой флегмоне в наружном ложе голени разрез производят по передненаружной поверхности голени. К заднему ложу голени оперативные доступы осуществляют по краям трехглавой мышцы и пяточного сухожилия. Глубокую флегмону переднего ложа голени вскрывают разрезом, который проходит параллельно переднему краю болыпеберцовой кости на расстоянии около 2 см от последнего.
17.3.4. Медиастинит
Медиастинит (mediastinitis; лат. mediastinum — средостение -itis) — воспаление клетчатки средостения.
Выделяют первичный (встречается реже) и вторичный медиастинит. Первичный медиастинит обусловлен проникновением возбудителей в клетчатку средостения различными путями. Вторичный медиастинит — превалирующая форма; чаще всего развивается в результате проникновения инфекции в клетчатку средостения при химических ожогах и повреждениях пищевода, трахеи, бронхов (инородными телами, при ранениях их, в том числе во время эндоскопических исследований), после операций на органах средостения, на легких. Меньшее значение имеет распространение инфекции из очагов в прилежащих органах и полостях (из клетчатки шеи, трахеобронхиаль-ных лимфатических узлов, позвоночника, ребер, грудины, плевральной полости). Еще реже встречается метастатический медиастинит в результате ге-могенно-лимфогенного распространения инфекции (одонтогенный).
Среди острых медиастинитов по клиническому течению выделяют молниеносные, острые и подострые формы.
438
По распространенности процесса различают: острые лимфадениты с вовлечением клетчатки средостения; острые гнойные медиастиниты (абсцессы); разлитые гнойные медиастиниты (флегмоны).
В соответствии с анатомическими особенностями средостения различают передний и задний медиастинит, каждый из которых в свою очередь может быть верхним, средним и нижним, а также тотальным с распространением воспалительного процесса на клетчатку всего средостения.
Принято выделять 3 фазы развития медиастинита: реактивную, токсическую и терминальную. Это дает возможность прогнозировать течение заболевания, планировать патогенетически обоснованное комплексное лечение и осуществлять контроль за ним.
Острый медиастинит характеризуется бурным развитием общих и местных симптомов. В течении медиастинита может найти проявление один из признаков существующей триады синдромов, каждый из которых имеет определенную симптоматику. В триаде синдромов два признака являются постоянными и хорошо выраженными: боль и токсикоз. Они создают фон заболевания, обусловливающий клиническую картину. Третий синдром, связанный со сдавлением сосудисто-нервного пучка шеи, может иметь различную степень выраженности симптомов.
Клиническая картина. Постоянный и ранний признак медиастинита — боль, которая имеет разную локализацию и интенсивность. Боль чаще всего локализуется за грудиной, иногда резко выражена. Давление на грудину при пальпации значительно усиливает боль.
Заболевание начинается внезапно с повышения температуры тела до 39—40 °С, лихорадки гектического характера с ознобами, профузным потом, рано появляются одышка, цианоз, тахикардия, наблюдаются снижение АД, нервно-психические нарушения, т. е. имеются признаки тяжелой интоксикации.
Синдром верхней полой вены проявляется отеком верхней половины туловища, шеи и лица, расширением подкожных вен.
Местная симптоматика зависит как от локализации и характера медиастинита, так и от степени вовлечения в воспалительный процесс органов средостения — пищевода, трахеи, блуждающего, возвратного, диафрагмаль-ного нервов, симпатического ствола, сердца. В связи с этим она разнообразна: возможны дисфагия, удушье, упорный кашель, осиплость голоса, изменение ритма сердечных сокращений при вовлечении в процесс симпатического ствола — синдром Бернара—Горнера, икота (в результате раздражения диафрагмальных нервов), иногда весьма упорная и мучительная, парез желудочно-кишечного тракта.
Диагностика. При объективном исследовании можно обнаружить зоны притупления в области грудины (при переднем медиастините) или в пара-вертебральной зоне (задний медиастинит). В редких случаях (при анаэробной инфекции) пальпаторно можно выявить газ в подкожной клетчатке.
Помогает в топической диагностике сравнительная клиническая характеристика передних и задних медиастинитов по А. Я. Иванову.
Из рентгенологических методик наибольшее значение имеет полипозиционная рентгеноскопия. На рентгенограммах органов грудной клетки в прямой и боковой проекциях отмечается расширение тени переднего средостения в верхних отделах с полициклическими контурами, иногда определяются округлые выпуклые тени, выступающие в правую или левую плевральную полость.
При переднем медиастините на рентгенограмме отмечаются смещение, а иногда и сдавление трахеи, наличие теней в переднем отделе средостения; можно обнаружить газовые пузыри. При заднем медиастините — сдавление пищевода, наличие
439
теней в заднем отделе средостения. При подозрении на повреждение пищевода выполняют эхофагографию с водорастворимым контрастным веществом в горизонтальном положении больного, которая помогает выявить затекание контрастного вещества за контур стенки пищевода, эмфизему средостения.
Заметно расширяются диагностические возможности при компьютерной томографии. На MP-томограммах органов шеи и грудной клетки в аксиальной, фронтальной и сагиттальной проекциях обнаруживают увеличение объема клетчатки в верхнем отделе как переднего, так и заднего средостения. Выявляют полости, локализовавшиеся загрудинно и превертебрально, неправильной формы, распространявшиеся до уровня правого желудочка и до VI грудного позвонка. Интенсивность сигналов от стенок полостей повышена по сравнению с окружающей клетчаткой, что свидетельствует об активности воспалительного процесса.
Лечение медиастинита должно быть энергичным и комплексным. Только операция в предельно ранние сроки может обеспечить успех, поэтому общее тяжелое состояние больного не должно служить противопоказанием к неотложному вмешательству по жизненным показаниям.
Выбор способа дренирования зависит от локализации и распространенности инфекционно-воспалительного процесса.
При верхнем медиастините выполняют трансцервикальную медиастино-томию по В. И. Разумовскому с введением в переднее и заднее средостение двухпросветных дренажных трубок для подведения лекарственных препаратов и вакуумной аспирации. Шейный доступ к средостению удобен и малотравматичен, позволяет осуществить адекватное раскрытие флегмон глубоких клетчаточных пространств шеи, прежде всего заглоточного пространства.
При передненижней локализации процесса возможно применение пара-стернального либо чрезгрудинного (продольного, поперечного) доступов. Однако эти доступы сложны и сопряжены с опасностью инфицирования раны, развития остеомиелита грудины. Дренирование абсцесса в нижнем отделе переднего средостения возможно и через небольшой разрез у основания мечевидного отростка. Дренирование небольших абсцессов целесообразно проводить под рентгенотелевизионным контролем. Для дренирования заднего средостения используют один из вариантов паравертебральной медиастинотомии по И. Т. Насилову, а также используют методику введения двухпросветной трубки через троакар интеркостально без резекции ребер или торакоскопическую медиастинотомию.
В послеоперационном периоде проводят непрерывный либо фракционный лаваж гнойной полости с постоянной активной аспирацией при разрежении 50—100 см вод. ст. За сутки используют 1,5—2 л антисептического раствора. Через 2—3 дня состояние больных заметно улучшается, температура и другие признаки эндотоксикоза уменьшаются.
По ходу операции медиастинотомии часто возникает необходимость в наложении трахеостомы, которая может выполнять двойственную роль: дополнительное раскрытие фасциальных пространств шеи и обеспечение функции внешнего дыхания. В случаях повреждения пищевода, дополнительно выполняют гастростомию.
17.3.5. Паранефрит
Паранефрит (paranephritis; греч. para — около + nephros почка + -itis) — воспаление околопочечной жировой клетчатки. Выделяют первичную и вторичную формы паранефрита. Первичный паранефрит возникает при отсутствии почечного заболевания. Инфекция проникает в паранефральную
440
клетчатку из отдаленного гнойного очага любой локализации гематогенным путем. Вторичный паранефрит обычно является осложнением гнойного воспалительного процесса в почке (карбункул почки, пионефроз, гнойный перинефрит), при котором инфекция непосредственно распространяется на паранефральную клетчатку. Вторичный паранефрит может быть также следствием распространения инфекции по лимфатическим анастомозам, связывающим лимфатическую систему правого паранеф-рального пространства, червеобразного отростка, слепой и восходящей кишки.
Острый воспалительный процесс в паранефральной клетчатке начинается с инфильтрации ее с последующим гнойным расплавлением и образованием гнойной полости, окруженной инфильтратом. Этому способствуют плотные фасциальные перемычки, радиально разделяющие околопочечную клетчатку. При прогрессировании заболевания фасциальные перемычки разрушаются, образуется паранефральная флегмона.
По локализации воспалительного процесса в паранефральной клетчатке различают передний, задний, верхний, нижний и тотальный паранефрит. Передний паранефрит наблюдается редко. Задний паранефрит встречается наиболее часто. В запущенных случаях образовавшийся гнойник может самостоятельно прорваться под кожу в области поясничного четырехугольника Лесгафта—Гринфельта или поясничного треугольника (треугольник Пти). При верхнем паранефрите возможен реактивный выпот в плевральной полости, а иногда гнойник вскрывается в плевральную полость и бронх. При нижнем паранефрите гнойник нередко распространяется вниз по подвздошно-поясничной мышце в клетчатку малого таза или под паховую связку, а в далеко зашедших случаях он может вскрыться в мочевой пузырь.
Паранефрит может возникнуть внезапно на фоне полного здоровья или присоединиться как осложнение другого гнойного процесса. Заболевание начинается с озноба, высокой температуры и боли в поясничной и подреберной областях. Иногда характер боли напоминает приступ почечной колики. Появляется общая слабость, наблюдаются потеря аппетита, метеоризм, запор. Через 3—4 дня температура становится гектической и субфеб-рильной. Состояние больного тяжелое, нарастает интоксикация. Все формы паранефрита характеризуются жалобами на боль в поясничной и подреберной областях при глубоком вдохе. При осмотре иногда удается обнаружить искривление позвоночника в здоровую сторону. Пальпаторно в области почки может быть выявлено плотное бугристое образование, напоминающее опухоль.
При верхнем паранефрите почка иногда оттеснена книзу и доступна пальпации. Часто в воспаление вовлекается поддиафрагмальная клетчатка, ограничивается подвижность купола диафрагмы, не раскрывается диафраг-мальный синус. При прогрессировании заболевания наблюдаются реактивный выпот в плевральной полости, а затем вскрытие гнойника в плевральную полость с образованием эмпиемы плевры. Нижний паранефрит конту-рируется в виде неподвижной воспалительной опухоли в области пояснич-но-подвздошной мышцы. При заднем и нижнем паранефрите может наблюдаться мышечная контрактура в тазобедренном суставе (псоас-сим-птом). Пальпация области почки обычно болезненна, характерны резко положительные симптомы Израэля (болезненность при надавливании в области поясничного треугольника) и Пастернацкого. При заднем паранефрите имеют место припухлость в поясничной области, местное повышение кожной температуры.
441
Важную роль в диагностике паранефрита играет рентгенологическое исследование. На обзорном снимке можно обнаружить нечеткость контуров поясничной мышцы, искривление позвоночника в сторону поражения. Тени почки размыты или не видны. Экскреторная урография выявляет отклонение мочеточника в медиальную или латеральную сторону; слабо дифференцируется прилоханочный отдел мочеточника. Подвижность почки при дыхании на больной стороне резко ограничена. При отграниченном инфильтрате в поясничной области допустима диагностическая пункция, однако лучше ею пользоваться во время операции.
Лечение. В ранней стадии острого паранефрита, когда еще не произошло нагноения воспалительного инфильтрата, проводят консервативное лечение с применением антибактериальных средств. При образовании пара-нефрального абсцесса показано оперативное вмешательство: люмботомия, широкое вскрытие и дренирование гнойной полости.
При заднем паранефрите гнойник иногда вскрывают и дренируют через межмышечный доступ, не прибегая к люмботомии.
17.3.6. Парапроктит
Парапроктит (paraproctitis; греч. para — около + проктит) — гнойный очаг в околопрямокишечной клетчатке, связанный с наличием инфекции в стенке прямой кишки.
Среди ограниченных параректальных нагноений по их глубине локализации различают 5 основных форм абсцессов (рис. 17.10): подкожные околопрямокишечные, ишиоректальные, подслизистые, тазово-прямокишеч-ные и ретроректальные.
Выделяют также боковой и подковообразный абсцесс, при которых процесс локализуется позади и по бокам прямой кишки, охватывая большую
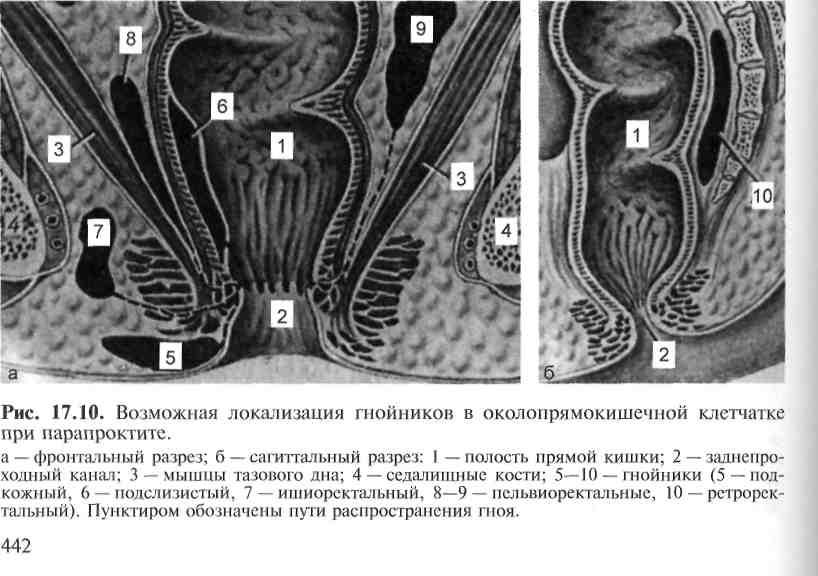
часть ее окружности. Передние парапроктиты, почти исключительно подкожные, редки.
Гнойный экссудат в большинстве случаев содержит смешанную флору, в состав которой входят кишечная палочка, анаэробы, золотистый и белый стафилококк, стрептококк, энтерококк. Абсолютно доминирующими являются ассоциации кишечной палочки со стафилококком или стрептококком.
Входными воротами инфекции в подавляющем большинстве случаев являются воспаленные кишечные (морганиевы) крипты, куда открываются устья анальных желез. Отсюда воспалительный процесс (в конечном итоге гнойного характера) переходит на околопрямокишечную клетчатку, распространяясь по имеющимся здесь клетчаточным пространствам. Однако возбудители инфекции могут проникать в клетчатку и при других заболеваниях дистального отдела прямой кишки — проктите, геморрое, анальных трещинах, реже при микротравмах слизистой оболочки прямой кишки. Воспалительные процессы околопрямокишечной клетчатки могут возникнуть в связи с заболеванием других органов — предстательной железы, уретры, бульбоуретральных (куперовских) желез, органов женской половой сферы, распадающейся раковой опухоли, неспецифическом язвенном колите, остеомиелите костей, позвоночника.
Клиническая картина. Острый неспецифический паракроктит в типичных случаях проявляется весьма характерными клиническими признаками. Больной отмечает боль в прямой кишке, тазу и промежности, чувство дискомфорта во время акта дефекации (тенезмы, задержка стула), дизуриче-ские расстройства, повышение температура тела.
Местные признаки параректальных абсцессов обусловлены их локализацией. Подкожные абсцессы, располагающиеся около анального отверстия, проявляются резкими болями в области ануса, особенно сильными при дефекации. В промежности отчетливо определяется воспалительная припухлость (инфильтрат) на стороне поражения с гиперемированной, отечной лоснящейся кожей. Ее пальпация резко болезненна. Флюктуация проявляется поздно и не во всех случаях.
При более глубоком, ишиоректалъном, абсцессе общие расстройства выражены гораздо резче. Инфекционно-воспалительный процесс захватывает глубокие слои клетчатки и распространяется позади прямой кишки на другую сторону вплоть до предстательной железы и тазовой клетчатки. В первые дни обычно превалируют общие симптомы. Больного беспокоят тяжесть в тазу и тупые боли в прямой кишке, которые по мере формирования гнойника приобретают пульсирующий характер; могут наблюдаться ди-зурические расстройства. Внешне местные признаки ишиоректального абсцесса, как правило, проявляются к исходу первой недели в виде нерезко выраженной отечности и гиперемии кожи, что свидетельствует о переходе воспаления на подкожную жировую клетчатку. Местные изменения раньше всего удается обнаружить, исследуя прямую кишку пальцем.
Для пельвиоректального абсцесса характерна картина тяжелого общего заболевания. Такой абсцесс располагается выше тазового дна, но может локализоваться и низко, либо спереди, либо сзади, либо по бокам прямой кишки. При данной локализации парапроктит не имеет наружных признаков в области заднего прохода, ишиоректальных впадин; поверхностная боль отсутствует. Больного беспокоят недомогание, лихорадка, озноб, тяжесть и боли в нижней половине живота, области таза. Возможны дизури-ческие расстройства, а также иррадиация боли в крестец, надлобковую область. В этот период ошибочно диагностируют колит, цистит, сальпингит и пр. В дальнейшем инфекционно-воспалительный процесс «спускается»
443
вниз — в клетчатку седалищно-прямокишечной впадины с формированием здесь гнойника, сопровождающегося характерными клиническими признаками.
Подслизистые абсцессы локализуются выше морганьевых крипт или ано-ректальной линии. При пальцевом исследовании прямой кишки определяется округлое эластичное образование, располагающееся под слизистой оболочкой, а при распространении воспаления на межмышечное пространство — уплощение стенки кишки с нечетким инфильтратом. В отличие от подкожных абсцессов при подслизистой форме парапроктита боль бывает менее интенсивной. Гнойник обычно вскрывается в просвет кишки в течение недели, и заболевание заканчивается выздоровлением. В ряде наблюдений гнойно-воспалительный процесс распространяется книзу в подкожную клетчатку или кверху в вышележащую под слизистую ткань прямой кишки; такой абсцесс называется подкожно-слизистым.
Ретроректальные абсцессы проявляются сильной болью в прямой кишке с иррациацией в крестец. Местные признаки заболевания проявляются при распространении воспалительного процесса на ишиоректальную, подкожную клетчатку. При пальцевом исследовании определяется болезненное выбухание задней стенки прямой кишки; давление на копчик усиливает боль.
Весьма тяжело протекает парапроктит, вызванный анаэробной флорой. Характерными признаками анаэробного парапроктита являются быстрое распространение процесса, выраженная инфильтрация тканей, не всегда имеющая четко определяемый центральный очаг воспаления. У больных наблюдаются снижение АД, резкая тахикардия при умеренном повышении температуры тела. При преобладании в микробной флоре Вас. perfringens отмечается крепитация. В этой группе выделяют гангренозно-гнилостный парапроктит и форму, протекающую с восходящим анаэробным лимфангитом. Гангренозно-гнилостный парапроктит характеризуется распадом седалищно-прямокишечной и тазово-прямокишечной клетчатки с распространением процесса на подкожную жировую клетчатку, мышцы ягодичной области. Парапроктит с восходящим анаэробным лимфангитом носит более распространенный характер, поражает лимфатические сосуды передней стенки живота вплоть до реберной дуги и мышцы брюшной стенки, иногда брюшину.
Диагностика острого парапроктита основывается на данных клинического исследования, осторожном пальцевом исследовании прямой кишки и лабораторных данных. К инструментальным методам исследования (ано-скопия, ректороманоскопия) по причине резкой болезненности прибегать не следует. При подкожном парапроктите обнаруживают болезненный инфильтрат, расположенный не выше гребешковой линии; стенки прямой кишки выше анального канала остаются эластичными. При ишиоректаль-ном абсцессе болезненный инфильтрат в силу глубокого расположения удается выявить при бимануальном исследовании прямой кишки: палец одной руки вводят в прямую кишку, а другой рукой снаружи выявляют уплотнение параректальной клетчатки. При этом характерно усиление болезненности при толчкообразной глубокой пальпации промежности. На поздней стадии определяется инфильтрация стенки анального канала, нижне-ампулярного отдела прямой кишки: флюктуация выявляется редко. Подслизистые гнойники при пальцевом исследовании распознаются без труда. Тазово-прямокишечные абсцессы распознают чаще в поздней стадии, когда жалобы больного позволяют заподозрить локализацию и связь патологического процесса с прямой кишкой. Пальцевое и бимануальное исследо-
444
вание прямой кишки обнаруживает инфильтрат, верхнюю границу которого достичь не удается; этот признак отличает ишиоректальные абсцессы от тазово-прямокишечных. При отсутствии сильной боли возможна ректоро-маноскопия, в ходе которой обнаруживают гиперемированную легко кровоточащую слизистую, выбухающую над инфильтратом. В сомнительных случаях рекомендуется диагностическая пункция. Ретроректальные абсцессы диагностируют по клиническим данным.
Дифференциальный диагноз с кистозными и опухолевыми образованиями основывается на обнаружении гнойного разрушения задней стенки прямой кишки, данных рентгенологического исследования и результатах пункции, биопсии.
Острый парапроктит может иметь три исхода: выздоровление (если вскрытие гнойника сопровождается рубцеванием отверстия в стенке кишки, послужившего входными воротами инфекции), развитие хронически рецидивирующего парапроктита, возникновение хронического парапрокти-та с формированием свища прямой кишки.
Лечение. В ранней стадии острого парапроктита, когда отсутствуют признаки гнойного расплавления тканей, проводят противовоспалительную терапию (антибиотики, микроклизмы с раствором колларгола, ромазуланом, настойкой ромашки, теплые сидячие ванны, физиотерапевтические процедуры), назначают щадящую диету с исключением раздражающих пищеварительный тракт продуктов, лекарственные средства, регулирующие стул и облегчающие дефекацию.
При наличии гнойника показано оперативное вмешательство, которое предпринимают после очистки толстой кишки с помощью клизмы. Операции, выполняемые в ранние сроки, способствуют снижению частоты осложнений (параректальные свищи), а также рецидивов заболевания. Операцию выполняют под общей анестезией. Местная анестезия мучительна для больного, не позволяет выполнить растяжение ануса и явно недостаточна для вскрытия глубоких гнойников.
Перед тем как произвести разрез кожи, прямую кишку исследуют пальцем и осматривают ее стенки с помощью ректального зеркала. Затем осуществляют чрескожную пункцию гнойника. Извлеченный гной направляют на микробиологическое исследование. В полость гнойника вводят 0,5 % раствор метиленового синего пополам с 4 % раствором перекиси водорода — полость гнойника окрашивается, а поступление красящего вещества в просвет кишки помогает установить локализацию дефекта в стенке кишки.
Применяют радиальный, полулунный, крестообразный разрезы; оптимальным является полулунный (дугообразный) (рис. 17.11).
Такой разрез наносят по окружности анального кольца, отступя от него не менее чем на 2 см. Вскрыв гнойник, необходимо обследовать полость его пальцем, разрушить перемычки, промыть раствором антисептика. Радикальная хирургическая обработка чаще не представляется возможной, поэтому во время операции применяют ультразвук, лазер и пульсирующую струю антисептика. Рану оставляют открытой, вводят дренажи и рыхло выполняют марлей с мазью на водорастворимой основе либо применяют ферменты, раствор антисептика. На следующий день после операции делают перевязку, нередко под общей анестезией. Местное лечение раны проводят по общепринятым правилам. Необходим тщательный туалет перианальной области, а после дефекации — теплые ванны с раствором перманганата калия.
Выполняют и более радикальную операцию, при которой одновременно с опорожнением гнойника иссекают пораженную крипту, а следовательно, ликвидируют источник инфекции. При поверхностном парапроктите про-
445

Рис. 17.11. Разрезы, применяемые при остром парапроктите.
а: 1 — перианальный абсцесс; 2 — позадипрямокишечный; 3 — ишиоректальный; б — хирургические доступы (б), применяемые при ишиоректальном (1) и пельвиоректальном (2) абсцессах [Гостищев В. К., 2002].
изводят радиальный разрез, а при глубоком — дугообразный и дополнительный радиальный в сторону источника инфекции.
При локализации входных ворот инфекции на задней стенке анального канала после вскрытия гнойника (дугообразным разрезом) проводят лигатуру через свищевой ход с выводом ее в анус и последующим затягиванием лигатуры (медленное прорезывание сфинктера лигатурой сопровождается постепенным образованием рубца). Метод позволяет радикально излечить больного при высоких парапроктитах, предупреждая развитие недостаточности анального сфинктера.
Низко расположенные подслизистые гнойники вскрывают через стенку прямой кишки, но только в том случае, если гнойники расположены недалеко от стенки прямой кишки. Гнойники, распложенные глубже, опорожняют через ткани промежности.
В послеоперационном периоде больным назначают бесшлаковую диету (бульон, творог, сливочное масло, кисели, яйца), с 3—4-го дня разрешают отварную рыбу, протертое отварное мясо. В течение 4—5 дней назначают простую настойку опия по 5—6 капель 3 раза в день. В дальнейшем рацион расширяют вплоть до перевода больного на общий стол.
17.3.7. Ректальные свищи
Ректальные свищи — следствие острого парапроктита, ранения или других причин (болезнь Крона, опухоли, специфические инфекции). У женщин ректовагинальные свищи чаще всего являются результатом разрыва влагалища и промежности во время родов или осложнением лучевой терапии опухолей.
446
Консервативная терапия чаще всего неэффективна и может быть оправдана лишь при наличии абсолютных противопоказаний к операции или как этап подготовки к ней.
Операцию производят только в стационарных, в том числе специализированных, условиях с адекватным обезболиванием.
При поверхностном (низком) параанальном свище производят его рассечение над зондом или иссечение по зонду; иссекают нависающие края раны и пораженную крипту и накладывают на дно раны отдельные подкож-но-подслизистые швы.
Транссфинктерные свищи иссекают в просвет кишки с последующим наложением отдельных кетгутовых швов на сфинктер, не захватывая кожу и слизистую оболочку. Гнойные затеки вскрывают с последующей раздельной тампонадой.
Экстрасфинктерные (огибающие снаружи) свищи иссекают со стороны промежности до стенки прямой кишки; пораженную крипту иссекают со стороны просвета кишки, на образовавшийся дефект слизистой накладывают два-три кетгутовых шва. Таким же образом накладывают швы на стенку кишки в глубине промежностной раны, которую не ушивают, а тампонируют. Во всех случаях остающийся участок свища выскабливают острой ложечкой и обрабатывают антисептиками.
При рубцовых изменениях в области пораженной крипты и экстрасфинк-терном пространстве свищевой ход иссекают со стороны промежности до стенки кишки и пересекают, его остатки выскабливают и обрабатывают антисептиками; на оставшуюся часть свищевого хода накладывают лигатуру.
Лигатурный метод оправдан и при свищах сложной конфигурации.
При наличии гнойных затеков, подковообразных или высоких свищей требуется раздельная тампонада просвета кишки и экстрасфинктерного пространства со швами или без, как при остром парапроктите. Внутреннее отверстие свища может быть закрыто с помощью пластики местными тканями с неполным или полным иссечением свищевого хода.
Ректовагинальные свищи, как правило, сопровождаются недостаточностью анального жома. Характер оперативного пособия определяется в каждом случае индивидуально. Иссекают рубцы промежности, задней стенки влагалища и передней стенки прямой кишки, захватывая свищ. Проводят гемостаз, сфинктеролеваторопластику, накладывают наводящие кетгутовые подслизистые швы на стенку влагалища, шелковые швы на переднюю промежность дополняют двумя-тремя поддерживающими швами на промежность. Назначают строгий постельный режим в течение 10—12 сут в физиологическом положении на функциональной кровати; ежедневные перевязки и тщательный туалет обеспечивают первичное заживление раны.
В зависимости от топографоанатомических особенностей свища могут быть использованы и другие доступы.
17.4. Гнойные заболевания железистых органов 17.4.1. Мастит
Мастит (mastitis; греч. mastos — грудь + itis; син. грудница) — воспаление паренхимы и интерстиция молочной железы. В большинстве случаев развивается воспаление одной железы.
447

Рис. 17.12. Типичная локализация гнойных очагов в молочной железе.
1 — субареолярный мастит; 2 — интрамам-марный мастит; 3 — глубокий интрамаммар-ный мастит и ретромаммарная флегмона.
В зависимости от поражения воспалительным процессом различных структур молочной железы выделяют паренхиматозный и интер-стициалъный мастит. Клиническое течение этих форм однотипно. Выделяют также галактофорит (воспа-3 ление млечных протоков) и ареолит (воспаление околососкового кружка).
По отношению к функции железы, в которой развилось воспаление, различают лактационный и нелактационный мастит. Лактационный мастит развивается у кормящих женщин и составляет до 85 % всех случаев острого мастита. К нелактационным относят маститы некор-мящих и беременных.
По клиническому течению различают острый и хронический мастит. Острый мастит в процессе развития проходит стадию серозно-инфильтра-тивного воспаления, которому соответствуют две клинические формы (серозный и острый инфильтративный мастит), и стадию гнойно-некротического расплавления тканей, клинически проявляющуюся одной из форм — абсцедирующей, флегмонозной или гангренозной. В группе хронических маститов выделяют гнойную и негнойную формы. Хронический гнойный мастит обычно является исходом острого мастита при его неправильном лечении; крайне редко встречается первично-хронический гнойный мастит. К негнойной форме относится также плазмоклеточный перидуктальный мастит.
По локализации воспалительного процесса различают поверхностные (премаммарные и субареолярные), интрамаммарные и тотальные (рис. 17.12).
Большинство маститов имеют стафилококковую этиологию 60—90 %; стрептококки встречаются в 10 раз реже; в 30 % всех случаев идентифицируют микробные ассоциации с участием грамотрицательных палочек. Крайне редкими являются специфические инфекции молочной железы (туберкулезный, сифилитический мастит).
Основным источником инфекции являются носители патогенных микроорганизмов (в первую очередь стафилококков) среди медицинского персонала родильных домов, других окружающих лиц; реже возбудители заносятся с кожи и сосков матери, из ротовой полости ребенка; иными словами, решающее значение принадлежит внутрибольничному инфицированию.
Выделяют 3 пути проникновения возбудителей инфекции в ткань молочной железы: галактогенный, лимфогенный, гематогенный (редкий). Входными воротами инфекции чаще являются трещины соска, откуда вне-
448
дрившиеся бактерии распространяются в ткань молочной железы по лимфатическим путям. Внедрение возбудителей через молочные ходы наблюдается реже. Вследствие галактофорита — воспаления млечного выводного протока — происходит отек эпителия молочных ходов, что способствует застою молока, распространению инфекции на интерстиций железы. Важнейшую роль пускового механизма в развитии мастита играет нередко развивающийся у первородящих застой молока (лактостаз), чему способствуют нарушение режима кормления и неправильное положение молочной железы (сдавление одеждой, перегиб).
Гнойный процесс в молочной железе развивается со всеми особенностями, характерными для воспаления железистых органов. В фазе серозного воспаления ткань железы пропитывается серозным экссудатом, развивается лейкоцитарная инфильтрация вокруг сосудов. При переходе воспаления в гнойно-некротическую стадию возникает диффузная гнойная инфекция паренхимы железы с мелкими очагами гнойного расплавления; при их последующем слиянии формируются абсцессы. Наиболее часто очаги гнойного воспаления локализуются интрамаммарно, субареолярно. Междольковые перегородки, слабовыраженные в молочной железе, плохо противостоят лизирующему действию гноя. В связи с этим инфекция может распространиться за пределы железы, формируются подкожные или ретромаммарная флегмоны. В некоторых случаях наступает множественный тромбоз кровеносных сосудов и как следствие развивается гангренозная форма мастита; некроз значительных участков железы может быть также следствием апо-стематозного мастита (гнойная инфильтрация паренхимы железы). Гангренозный мастит обычно протекает с общей септической реакцией; летальность при нем заметно выше, чем при других формах воспалительного поражения молочной железы.
Клиническая картина острого мастита слагается из синдрома местных воспалительных изменений и синдрома эндогенной интоксикации. В стадии серозного воспаления больные отмечают чувство нагрубания железы, колющие боли, недомогание; возможно повышение температуры тела. Форма железы практически не изменена или наблюдается незначительное увеличение ее. При сравнительной пальпации удается определить умеренно болезненное уплотнение с нечеткими границами в толще либо на поверхности железы. Сцеживание молока болезненно и не приносит облегчения; это отличает серозную стадию мастита от лактостаза. Возможно повышение СОЭ и числа лейкоцитов в периферической крови. Общее состояние больной остается удовлетворительным.
Острый инфильтративный мастит характеризуется более выраженными признаками воспаления: подъем температуры достигает 39 °С, появляются гиперемия кожи, отек и болезненность всей железы. В толще железы определяется резко болезненный инфильтрат с нечеткими границами без признаков размягчения и флюктуации. Эти симптомы при условии активного консервативного лечения обычно стихают в ближайшие 2—3 дня, но болезненность, пастозность железы, субфебрилитет могут сохраняться до 2 нед.
Переход инфекционного воспаления в стадию гнойно-некротического расплавления тканей клинически проявляется усилением боли в железе, приобретающей постоянный ноющий характер, и заметным ухудшением общего самочувствия (слабость, утрата аппетита, нарушение сна, головная боль, ознобы). При осмотре обнаруживают увеличение пораженной железы, гиперемию кожи, расширение подкожных вен, увеличенные болезненные подмышечные лимфатические узлы. Лихорадка приобретает гектиче-ский характер, сопровождается тахикардией, изменениями на ЭКГ, одыш-
449
кой. В периферической крови выраженный лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение СОЭ; нередко снижаются содержание эритроцитов и концентрация гемоглобина. Степень выраженности гнойно-резорбтивной лихорадки зависит от вирулентности возбудителя и объема поражения молочной железы и в меньшей степени — от формы гнойного мастита, которую дифференцируют по местным признакам.
При абсцедирующей форме в ткани железы пальпируется отграниченный болезненный инфильтрат с размягчением или флюктуацией в центре. Рет-ромаммарная флегмона характеризуется увеличением в объеме всей железы, которая приобретает полушаровидную форму и как бы приподнимается прямо вперед; над верхним краем железы определяется флюктуирующий инфильтрат. Для флегмонозного мастита характерны гиперемия и отек кожи, резкая болезненность при пальпации, обширное распространение инфильтрата при отсутствии четких границ с непораженной железой. Могут определяться флюктуирующие участки, но чаще они отсутствуют. Сосок обычно втянут. Общее состояние тяжелое (септическое). Гангренозный мастит сопровождается признаками некроза ткани железы: багрово-красная либо синевато-черная окраска кожи, резкий отек и пастозность тканей, возможны эпидермальные пузыри с геморрагической или мутной жидкостью. В ходе дифференциальной диагностики необходимо помнить о специфических формах (туберкулез, сифилис) и злокачественных новообразованиях молочной железы.
Лечение мастита на стадии серозного воспаления консервативное. На пораженную железу накладывают поддерживающую (не сдавливающую) повязку; при этом сосок оставляют открытым для систематического опорожнения железы (отсасывание молока). Сцеживания руками избегают, так как эта грубая процедура может способствовать прогрессированию воспаления. Назначают антибиотики широкого спектра действия, противовоспалительные средства. Эффективны УВЧ, УФО (в эритемных дозах). Все процедуры проводят после опорожнения железы.
В гнойно-некротической стадии основой лечения мастита является операция. Ее выполняют в неотложном порядке, как только диагностирована любая из форм гнойного мастита, под общим обезболиванием. Для вскрытия поверхностных, а также интрамаммарных гнойных очагов рекомендуют радиальные разрезы, не доходящие до соска на 2—3 см (опасность повреждения молочных протоков). После эвакуации гноя проводят тщательное обследование полости. Достаточная глубина разреза должна обеспечивать вскрытие всех затеков, иссечение некротических и пропитанных гноем тканей; следует разъединить тяжи и перемычки. Слабое отграничение гнойно-воспалительного процесса повышает требования к радикализму оперативного вмешательства. При больших размерах гнойной полости или формировании несколько абсцессов может потребоваться второй радиарный разрез. В случаях глубоких интрамаммарных, ретромаммарных маститов доступ к гнойному очагу осуществляют дугообразным разрезом по переходной складке под молочной железой. В ретромаммарное пространство проникают путем отслаивания железы от большой грудной мышцы; из этого доступа могут быть вскрыты интрамаммарные очаги нижних квадрантов. После хирургической обработки проводят дополнительную физическую санацию раны пульсирующей струей антисептика, вакуумированием, ультразвуком и др., обильно промывают ее антисептиком. При небольших размерах очага, радикальной операции и невыраженной перифокальной инфильтрации возможно наложение на рану первичного шва с обязательным приточно-аспирационным дренированием, при этом достигается оптимальный косметический резуль-
450
тат. В большинстве случаев рану ведут под повязкой до момента полного очищения; после этого решают вопрос о необходимости и методе закрытия раны. Как правило, применяют отсроченный первичный, реже вторичный швы; необходимость в кожной пластике возникает после обширных некрэктомий.
При тотальном гангренозном, иногда флегмонозном мастите, осложненном сепсисом, показана мастэктомия. Эта достаточно травматичная операция в условиях септического состояния пациентки требует предварительной кратковременной подготовки: коррекции электролитных нарушений, восполнении ОЦК, введении кардиотоников, антибиотиков.
Вскрывать и дренировать гнойные очаги через ограниченные разрезы при маститах не следует, так как воспалительные процессы в молочной железе редко бывают отграниченными, и при отсутствии полноценного обследования остаются недренированными гнойные затеки.
В послеоперационном периоде продолжают антибиотикотерапию; после получения результатов бактериологического исследования проводят ее коррекцию. Одновременно назначают инфузионно-трансфузионную, иммунокор-ригирующую терапию, продолжают обязательно опорожнять молочную железу. Если поступление в рану железы молока затрудняет ее заживление, то принимают меры для подавления лактации. Необходимость в искусственном сокращении лактации возникает также при торпидном течении мастита.
Консервативное лечение хронических форм мастита, как правило, бесперспективно, поэтому показано оперативное вмешательство в объеме радикального иссечения патологического очага с последующим гистологическим исследованием.
Профилактика мастита включает подготовку сосков, предупреждение патологии родов, профилактику инфицирования молочных желез в послеродовом периоде, строгое соблюдение правил личной гигиены. В послеродовом периоде необходимо ежедневно производить смену белья, соблюдать гигиену кормления. Особое значение имеет регулярное кормление до полного опорожнения железы, а когда ребенок не полностью высасывает молоко, следует пользоваться молокоотсосом. Возникающие трещины соска требуют внимания и своевременного лечения с применением всех правил асептики.
