
Ошурков П.А. - Объемные образования головного мозга - 2019
.pdfпривязку, качественную и быструю трансмиссионную корректировку изображений. Клинические данные свидетельствуют, что ПЭТ-КТ имеет преимущества перед ПЭТ и КТ, проведенными отдельно. Однако же следует отметить ограниченность применения ПЭТ при диагностике опухолей центральной нервной системы в силу высокого уровня метаболизма C6H12O6 в ткани мозга.
Шкалы Карновского и ECOG-ВОЗ
Когда идет речь об онкологическом заболевании и выборе тактики ведения пациента, целесообразно проводить оценку тяжести его состояния. В отношении нейроонкологии эта оценка применима, в первую очередь, для пациентов с вторичным поражением центральной нервной системы, однако может быть использована и в других случаях. Во всем мире приняты и широко используются две простые в использовании классификации, способные привести в некие категории различных по основному процессу пациентов. Преимущественно используются шкалы Карновского
(Karnofsky) и ECOG-ВОЗ.
Шкала Карновского. КРS (Karnofsky Performance Status Scale
|
|
|
|
|
|
|
|
|
|
Активность |
|
|
|
|
% |
|
Сохранена |
нормальная |
|
Практически здоров: жалоб нет; признаков |
|
100 |
|||||||||||
ежедневная |
активность; |
|
заболевания нет |
|
|
|
|
|
|
|
||||||
медицинская помощь |
не |
|
Сохранена нормальная ежедневная активность; |
|
90 |
|||||||||||
требуется |
|
|
|
|
|
незначительная |
степень |
выраженности |
проявлений |
|
|
|||||
|
|
|
|
|
|
|
заболевания |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нормальная ежедневная активность поддерживается с |
|
80 |
|||||||
|
|
|
|
|
|
|
усилием; |
умеренная |
степень |
выраженности |
|
|
||||
|
|
|
|
|
|
|
проявлений заболевания |
|
|
|
|
|
|
|||
Утрата |
трудоспособности, |
|
Способен себя обслужить; не способен поддерживать |
|
70 |
|||||||||||
возможно |
|
проживание |
в |
|
нормальную ежедневную активность или выполнять |
|
|
|||||||||
домашних условиях; |
большей |
|
активную работу |
|
|
|
|
|
|
|
||||||
частью |
|
способен |
|
себя |
|
Большей частью способен себя обслужить, однако в |
|
60 |
||||||||
обслужить; требуется уход в |
|
отдельных случаях нуждается в уходе |
|
|
|
|
|
|||||||||
различном объеме |
|
|
|
Частично способен себя обслужить, частично |
|
50 |
||||||||||
|
|
|
|
|
|
|
нуждается в уходе, часто требуется медицинская |
|
|
|||||||
|
|
|
|
|
|
|
помощь |
|
|
|
|
|
|
|
|
|
Не способен себя обслужить, |
|
Не |
способен |
себя |
обслуживать, |
требуются |
|
40 |
||||||||
требуется |
|
госпитальная |
|
специальный уход и медицинская помощь |
|
|
|
|||||||||
помощь; |
возможна |
быстрая |
|
Не |
способен |
себя |
обслуживать, |
показана |
|
30 |
||||||
прогрессия заболевания |
|
|
госпитализация, хотя непосредственная угроза для |
|
|
|||||||||||
|
|
|
|
|
|
|
жизни отсутствует |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
Тяжелое заболевание: необходима госпитализация, |
|
20 |
|||||||
|
|
|
|
|
|
|
необходима активная поддерживающая терапия |
|
|
|
||||||
|
|
|
|
|
|
|
Терминальный период: быстро прогрессирующий |
|
10 |
|||||||
|
|
|
|
|
|
|
фатальный процесс |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
Смерть |
|
|
|
|
|
|
|
0 |
|
|
Шкала ECOG-ВОЗ |
|
|
|
|
|
|
|
|
|
|
|
|
|||
0 |
Больной полностью активен, способен выполнять все, как и до заболевания (90-100% по |
|||||||||||||||
шкале Карновского) |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Больной неспособен выполнять тяжелую, но может выполнять легкую или |
сидячую |
||||||||||||||
1 |
работу |
(например, легкую |
домашнюю |
или |
канцелярскую работу, |
70-80% |
по |
шкале |
||||||||
|
Карновского) |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2 |
Больной лечится амбулаторно, способен к самообслуживанию, но не может выполнять |
|||||||||||||||
работу. |
Более 50% |
времени |
бодрствования проводит активно |
|
– в вертикальном |
|||||||||||
|
|
|||||||||||||||
40

положении (50-60% по шкале Карновского)
3Больной способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30-40% по шкале Карновского)
4Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10-20% по шкале Карновского)
6. Лечение опухолей головного мозга
Прежде чем начинать разговор о способах лечения опухолей головного мозга, следует сказать о том, что не все опухоли требует активной хирургической и иной тактики. При должном сборе анамнеза, отсутствии признаков инвазии и роста некоторые опухоли допустимо наблюдать. Также существует категория инкурабельных пациентов, активная хирургическая и иная тактика для которых невозможна в силу высоких рисков формирования грубого неврологического дефицита, а также высокой степени генерализации процесса с низкой предполагаемой продолжительностью жизни. В таких ситуациях порой следует предпочесть выбор в пользу сохранения качества жизни.
6.1. Этиопатогенетическое лечение
Лечение большинства патологий с точки зрения медицинской науки подразделяется на этиотропное, патогенетическое и симптоматическое. Однако этиопатогенетический подход к терапии какого-либо заболевания возможен лишь при условии установленных этиологии и патогенеза заболевания. Для онкологии не существует единой и общепринятой теории возникновения и прогрессирования процесса, а следовательно в определенном смысле невозможно и осуществление этиотропных алгоритмов терапии. Однако в ряде ситуаций патогенетический механизм все же может быть реализован. Речь идет, в первую очередь, о гормонпродуцирующих опухолях. Так, при подборе адекватной терапии гормональноактивной пролактиномы гипофиза с использованием препарата достинекс можно достичь не только стабилизации опухоли, но и регресса ее размеров. Подобные схемы лечения могут быть реализованы и для ряда иных гормон-продуцирующих опухолей центральной нервной системы. В случае верификации выраженного перифокального отека как элемент патогенетического лечения возможно применение диуретиков и гормонов для уменьшения компрессии окружяющих нервных структур и уменьшения ВЧД. В амбулаторных и стационарных условиях пациенту могут быть назначены диакарб под «прикрытием» аспаркама, а также дексаметазон внутримышечно по 4 мг * 3 раза в день с возможностью увеличения кратности и дозировки инъекций.
6.2. Симптоматическая терапия
При опухолях центральной нервной системы может применяться симптоматическое лечение. Так, пациенту нужно обеспечить адекватное обезболивание при наличии болевого синдрома, целесообразен контроль артериального давления. При наличии эписиндрома или топическом расположении опухоли, сопряженном с высоким риском его возникновения могут быть назначены антиконвульсанты (депакин, карбамаземин, вальпроаты и др).
41
6.3. Нейрохирургическое лечение
Нейрохирургическая наука идет в ногу со временем и активно развивается и совершенствуется. Нейрохирургическое вмешательство на современном этапе не мыслится без использования современных методов гемостаза, искусственных материалов, высокотехнологичных конструкций, операционного микроскопа с качественной оптикой, микрохирургического инструментария, ультразвукового деструктора, методов нейромониторинга, интраоперационной нейровизуализации, силового оборудования. Сегодня слово «трепанация» уже не подразумевает инвалидизирующее оперативное вмешательство, сопряженное с выскими показателями интраоперационной кровопотери и летальности. Нейрохирургия все больше становится похожей на искусство, приобретает черты прецизионности.
Развитие нейрохирургии значительно расширило возможности хирургического лечения опухолей центральной нервной системы. Оперативное лечение опухолей, которые еще некоторое количество времени назад считались иноперабельными, сегодня в умелых руках начинают превращаться в «потоковые» вмешательства с низкими интра- и периоперационными рисками. Безусловно, не все опухоли нервной системы удалимы тотально, равно как и не все опухоли нервной системы следует удалять, однако хирургическое лечение однозначно выходит на первый план при разговоре о нейроонкологии.
Хирургическое лечение в нейроонкологии следует разделить на следующие виды вмешательств:
•Тотальное удаление опухоли. Подразумевает удаление всей массы опухоли и инфильтрированных окружающих тканей. В первую очередь может быть выполнено при метастатическом поражении центральной нервной системы, внемозговых опухолях, внутримозговых опухолях отдельных локализаций при условии возможности резекции части здоровой ткани мозга.
•Субтотальное удаление опухоли. Наиболее частый вариант хирургического лечения при наличии инвазии опухолевой массы в жизненно-важные или функционально-значимые зоны головного мозга. В таких ситуациях удаляется до 90-99% объема опухоли, сохраняется незначительная часть ее во избежание развития грубого очагового неврологического дефицита. В таких случаях чаще всего пациенту предстоит этап последующей лучевой терапии. Также о субтотальном удалении может идти речь при хирургии опухолей, имеющих инвазивный характер роста. Так, при условии удаления всей видимой части опухоли хирург может предполагать наличие отдельных клеток опухоли в пределах здоровой ткани мозга, удаление которой будет сопряжено с формированием неврологического дефицита.
•Биопсия опухоли. Оперативное лечение, направленное на получение фрагмента опухолевой ткани для возможности гистологической верификации без удаления основного объема патологической ткани. Актуально в тех случаях, когда гистологический вариант объемного образования будет влиять на тактику ведения пациента. Также возможен в случае необходимости подбора варианта химиотерапии и лучевой терапии при невозможности или нецелесообразности масштабного оперативного лечения.
•Циторедуктивное или паллиативное удаление опухоли. По сути своей представляет собой вариант биопсии с парциальным удалением опухоли.
42
Целесообразно при отсутствии возможности тотального удаления опухоли для последующего лечения у химиотерапевтов и лучевых терапевтом. Парциальное удаление позволяем уменьшить масс-эффект, а также уменьшает количество патологической ткани, на борьбу с которой будут направлены последующие этапы лечения.
Принципы хирургического лечения опухолей головного мозга не укладываются в подходы и представления общей онкологии. Этому способствует ряд особенностей этой патологии. Первым делом следует обратить внимание на невозможность «блокрезекции» опухоли и необходимость удаления ее кускованием. Так, общеонкологические принципы предполагают удаление опухоли без ее фрагментирования, при возможности единым блоком для снижения рисков диссеминации патологических клеток. Однако же нейрохирургический доступ предполагает в большинстве случаев работу в узком пространстве с использованием микрохирургической техники и операционного микроскопа. Современный нейрохирург минимизирует тракцию ткани головного мозга, минимально применяет шпатели, а также использует на благо операции силу тяжести и возможности релаксации вещества головного мозга за счет эвакуации ликвора. Эти факторы обуславливают высокое значение грамотному предоперационному планированию, а также выбору положения головы пациента на операционном столе. В этой же связи, а также в силу близости анатомически-важных структур, невозможности смещения опухолевого узла при его выделении (во избежание компрессии им окружающей здоровой ткани мозга), возникает необходимость фрагментирования опухолевого узла и удаления опухоли кускованием.
Еще одним важным принципом нейроонкологии при разговоре об опухолях центральной нервной системы является невозможность удаления опухоли «с запасом», т.е. с иссечением здоровой ткани, окружающей опухолевый узел. Пожалуй, в этой фразе имеется некоторая неточность. Нейрохирург может удалить все, что угодно. Вопрос в том, каким окажется качество жизни пациента по окончании нейрохирургического этапа, экстубации и выхода на ясное сознание, и будут ли вообще они возможны. Да, именно близость анатомически и функционально важных нервных структур обуславливает необходимость осуществления выбора в пользу субтотального удаления опухолевого узла взамен сохранения нормальной функции. Так, удаление «с запасом» возможно лишь при ряде локализаций опухоли, где есть части головного мозга, имеющие меньшую функциональную нагрузку. В остальных случаях опухоль удаляется в пределах здоровой ткани, а также субтотально или парциально.
Микрохирургическая операция на головном мозге предполагает жесткую фиксацию головы пациента к операционному столу для исключения возможности дополнительно люфта и смещения анатомических структур в момент выполнения хирургической манипуляции. Для фиксации головы пациента в большинстве случаев используется скоба Mayfield. Ее применение предполагает чрескожную установку специальных шипов, фиксирующихся в костях черепа с последующей блокировкой подвижных частей скобы в максимально выгодном для нейрохирурга и анестезиолога положении головы пациента.
Отдельное внимание следует уделить положению пациента на операционном столе. Так, необходимость выполнения доступов к анатомически сложным областям головного мозга без дополнительной тракции окружающих структур предполагает несколько вариантов положения пациента на столе во время выполнения операции. Так, наиболее частыми вариантами являются варианты положения на спине, с валиком
43
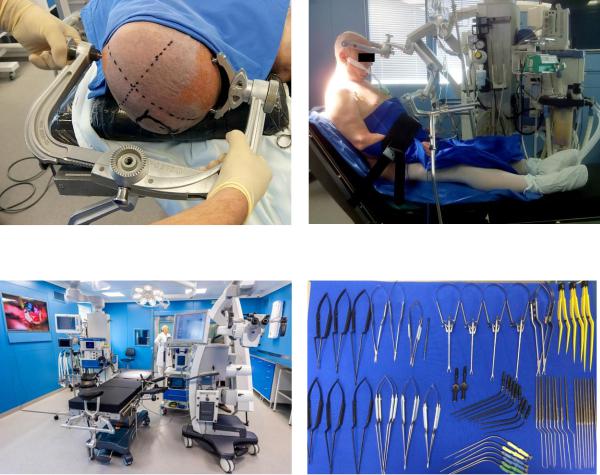
под плечом, положение на боку, на животе, а также сидя на операционном столе. Разумеется, изменения положения пациента в подавляющем большинстве случаев происходит уже после интубации пациента совместными усилиями всей операционной бригады. Каждое положение пациента на операционном столе имеет свои достоинства и недостатки. В рамках настоящего издания мы не будем останавливаться на них. Некоторым вариантам расположения в настоящее время отдается предпочтения, другие уходят в прошлое.
Рис 20. Фиксация головы пациента скобой |
Рис. 21. Положение пациента «сидя» на |
Mayfield и кожная разметка |
операционном столе |
Рис 22. Внешний вид стандартной |
Рис 23. Вариант используемого |
современной нейрохирургической |
микрохирургического инструментария |
операционной |
при нейрохирургической операции |
Наконец, нейрохирургическая операционная отличается от большинства прочих особым изобилием инструментария, а также технического оснащения, которые продолжают совершенствоваться. Многофункциональные операционные столы, масса микрохирургического инструментария и силового оборудования, ультразвуковые деструкторы, электроножи и петли, аспираторы, системы для аутогемотрансфузии, дозаторы, эндоскопы, интраоперационная навигация, метаболическая навигация, операционные микроскопы, транскраниальный допплер, интраоперационное УЗИ, интраоперационное КТ и МРТ, - это лишь часть того оснащения, которое может быть использовано в ходе современной нейрохирургической операции. Отдельное внимание уделяется современным средствам гемостаза, а также материалам, используемым для аллопластики тканей. Хирургические гематомы в мягких тканях в ряде случаев проходят асимптомно («тугое ушивание раны – лучший гемостаз»), неадекватный же
44
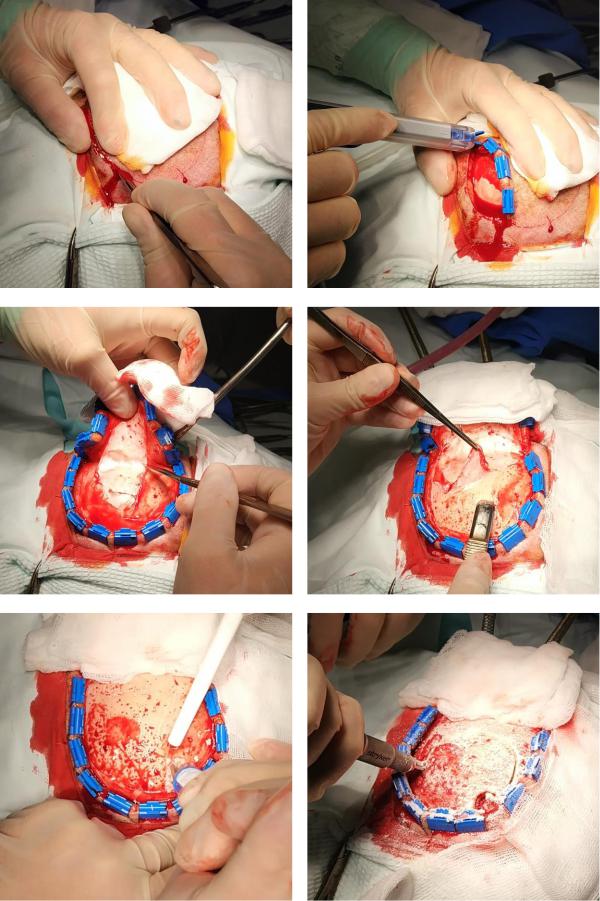
Рис. 24. Разрез кожи |
Рис. 25. Наложение кожных клипс |
Рис. 26. Поднятие кожного лоскута |
Рис. 27. Выделение лоскута надкостницы |
Рис. 28. Наложение трефины |
Рис. 29 Краниотомия |
45
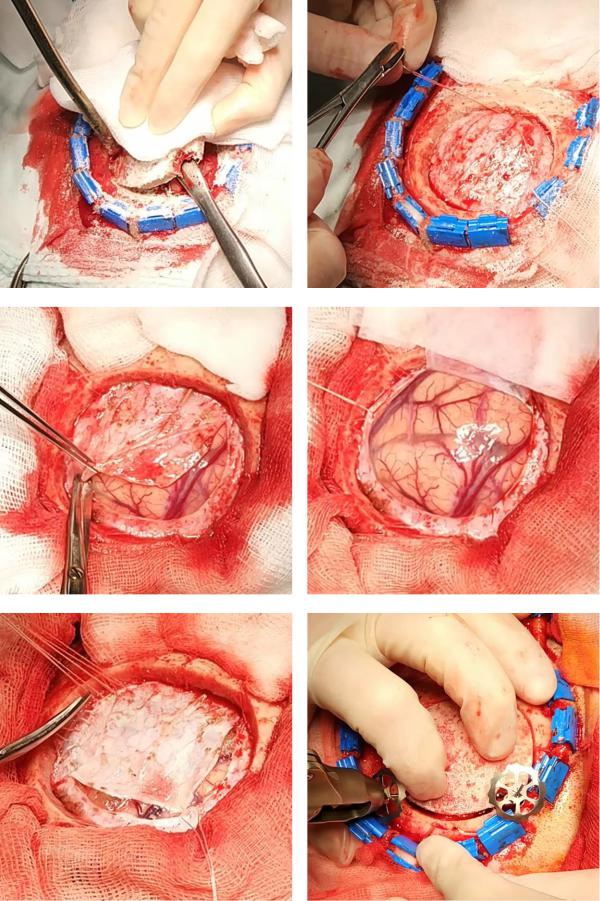
Рис. 30. Элевация кости |
Рис. 31. Подшивание ТМО по периметру |
Рис. 32. Разрез ТМО |
Рис. 33. Поднятие ТМО |
Рис. 34. Ушивание ТМО |
Рис. 35. Фиксация костного лоскута |
46
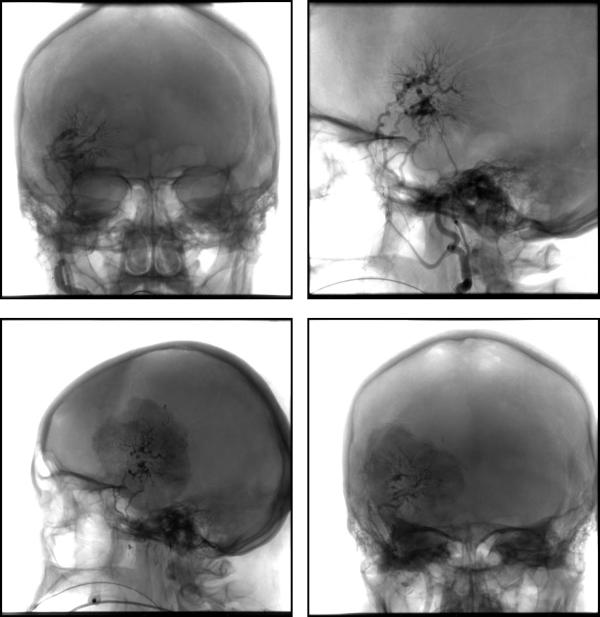
а) |
б) |
в) г)
Рис. 36. Эндоваскулярная эмболизация сосудов менингиомы. Интраоперационные изображения.
Рисунки а) и б) (фронтальный и боковая проекции) демонстрируют на полученных ангиограммах в проекции основной кости справа, правой лобно-височной области, патологическую опухолевую сосудистую сеть, получающую кровоснабжение из ветвей правой средней менингеальной артерии и незначительно из правой передней хороидальной артерии.
Рисунки в) и г) демонстрируют субтотальную окклюзию сосудистой сети опухоли.
гемостаз в нейрохирургической ране – риск образования послеоперационной гематомы и прогрессирование неврологического дефицита, включая угнетение сознания и риск гибели пациента. В отношении качественного послойного ушивания послеоперационной раны следует сказать, что послеоперационная подлоскутная и наружная ликвореи могут стать грозным осложнением, стирающим в ряде ситуаций достижения основного микрохирургического этапа операции. Все, что снижает интра- и периоперационный риск, снижает травматичность нейрохирургического
47
вмешательства, а также повышает его эффективность, с нашей точки зрения должно быть использовано в ходе нейрохирургической операции. Разумеется, везде есть грань разумного: использование каждого дополнительного аппарата неизбежно увеличивает время выполнения вмешательства (хотя порой и сокращает его). Мы любя называем дополнительные технические достижения, помогающие нейрохирургу на этапах операции «нейрохирургическими костылями» и стараемся разумно и по делу применять их в своей работе.
Следует отметить, что на сегодняшний день одной из активно развивающейся отрасли нейрохирургии является эндоваскулярное лечение, которым занимаются хирурги-интервенционисты. Эндоваскулярный этап лечения опухолей головного мозга подразумевает выполнение диагностической процедуры (церебральной ангиографии), о возможностях которой говорилось ранее, а также эмболизации сосудистой сети опухоли. Эмболизация сосудов опухоли не является самостоятельным видом лечения опухолей головного мозга, однако в ряде случаев представляет собой незаменимый этап хирургического лечения. Так, предварительная эмболизация в значительной степени помогает сократить объемы интраоперационной кровопотери, что особенно важно для высоковаскуляризированных опухолей. Наряду с этим следует иметь в виду, что эмболизация сосудистой сети опухоли может вызвать ее отек, что повлечет за собой прогрессирование неврологического дефицита. В этой связи целесообразно сокращать время между эндоваскулярным и открытым хирургическим этапами лечения опухоли. Для опухолей, не имеющих богато выраженной сосудистой сети, а также для опухолей с выраженным инфильтративным характером роста эндоваскулярное лечение не имеет актуальности.
Безусловно, нейрохирургическое вмешательство при опухолях головного мозга должно выполняться нейрохирургом, имеющим достаточный опыт микрохирургической работы на тканях головного мозга, в том числе в области нейроонкологии. Кроме того, вмешательство должно выполняться в условиях достаточного современного нейрохирургического инструментария.
Нейрохирургическая операция при опухолях центральной нервной системы может быть разделена на три основных этапа, включающих доступ к тканям мозга (наложение трепанационного окна), микрохирургический этап и ушивание послеоперационной раны. Первый и последний из них больше похожи на общехирургическую операцию с элементами травматологической. Выполняется разрез мягких тканей, отслаивается надкостница для пластики твердой мозговой оболочки, в большинстве случаев с использованием силового оборудования (бор, краниотом и проч.) накладывается трепанационное окно, твердая мозговая оболочка подшивается по периметру. Этапы выполнения стандартной костно-пластической трепанации при выполнении конвекситальных доступов представлена на рисунках 20-31. Аббревиатурой ТМО обозначена твердая мозговая оболочка. Особенностями доступа является работа в зоне высоко васкуляризированных тканей, в связи с чем нейрохирург должен обладать навыками и умениями, позволяющими профилактировать и предотвращать интраоперационную кровопотерю. При ушивании операционной раны выполняется герметичная пластика твердой мозговой оболочки в ряде случаев с использованием ранее приготовленного надкостничного лоскута, а также современных материалов для ее аллопластики. «Доступ» и «уход» выполняются послойно и анатомично. Микрохирургический этап удаления является основным и предполагает изобилие микрохирургического инструментария и высокотехнологичных средств помощи нейрохирургу. Во всех случаях удаления любой патологической ткани из организма пациента осуществляется отправка ее для выполнения гистологического исследования и его вариантов.
48
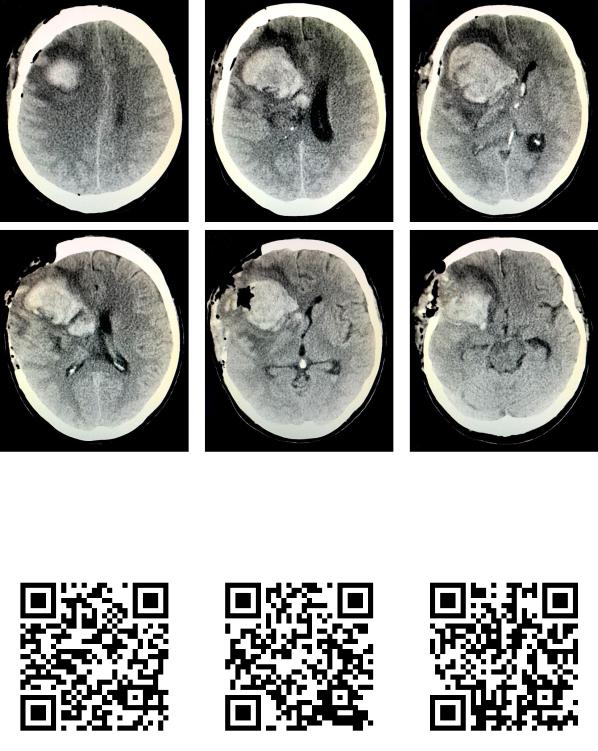
Рис. 37. Выполнение резекционной трепанации черепа как попытка жизнеспасающего оперативного вмешательства нейрохирургом, не имеющим достаточного опыта работы с опухолями головного мозга, у пациента с глиальной опухолью и послеоперационным кровоизлиянием. Первый ряд – послеоперационный контроль после КПТЧ и попытки удаления глиомы с кровоизлиянием, второй ряд – резекционная трепанация черепа в неотложном порядке.
Рис. 38.
QR-коды для перехода к просмотру образовательных видео на канале YouTube, демонстрирующих наложение трепанационного окна и его закрытие (интраоперационные видео).
49
