
- •1. Стабильность Si-C-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •26. Присоединение диалкилфосфитов к кратным связям (С=С, С=О, С=N), реакция Абрамова и Пудовика.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •42. Антихолинэстеразная активность фосфорорганических соединений. Обратимое и необратимое ингибирование холинэстеразы. Примеры обратимого и необратимого ингибирования в ряду фосфорорганических инсектицидов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •45. 2-Хлорэтильные производные в ряду кремний- и фосфорорганических соединений. Синтез хлорэтилфосфоновой кислоты, механизм дефолиантного действия.
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение О-метил-О-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило ЖМКО в реакции их солей с органическими галогенидами
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.

10. Способы получения, токсические характеристики и практическое использование органических производных свинца
Связи Pb–С более чувствительны к термическому воздействию и к действию света в сравнении с металлуглеродными связями кремния и олова. Они также легче разлагаются в присутствии кислот и окислителей.
В лабораторных условиях органические производные свинца получают действием соответствующих реактивов Гриньяра или литийорганических соединений на дихлорид свинца, например:
2 PbCl |
+ |
4 C H |
MgBr |
Pb(C H ) |
+ |
Pb |
+ |
2 MgBr |
+ |
2 MgCl |
||
2 |
|
6 |
5 |
|
6 |
5 4 |
|
|
|
2 |
|
2 |
Вместо хлорида свинца в этой реакции можно использовать соли других неорганических и органических кислот, а также оксид и сульфид свинца. В этой реакции образуется тонкодисперсный металлический свинец, который может реагировать с алкилиодидами по обычной схеме образования металлорганических соединений:
Pb |
+ |
2 CH |
I |
(CH ) |
PbI |
|
|
|
3 |
|
3 |
2 |
2 |
Образующийся диметилдииодплюмбан также можно перевести в тетраметилсвинец действием соответствующего реактива Гриньяра или литийорганического соединения. В соответствии с этим для получения тетраметилсвинца, например, к кипящей смеси дихлорида свинца и метилиодида в абсолютном эфире прибавляют раствор метилмагнийиодида. Реакция протекает в соответствии со схемой:
PbCl |
+ |
3 CH MgI |
+ |
CH |
I |
Pb(CH ) |
+ |
2 MgI |
+ |
MgCl |
2 |
|
3 |
|
3 |
|
3 4 |
|
2 |
|
2 |
При пиролизе солей свинца с органическими кислотами образуется возгорающийся при контакте с воздухом (пирофорный) свинец, который может реагировать с активными органическими галогенидами по реакции, аналогичной реакции Вюрца. Так, например,
хлорангидриды кислот в реакции с пирофорным свинцом превращаются в 1,2-дикетоны:
|
O |
O |
|
Pb (пирофорный) |
|
|
|
|
2 R C |
|
R |
|
Cl |
R |
|
|
|
|
|
O |
40

Тетраалкил- и тетраарилплюмбаны образуются при взаимодействии соответствующих органических галогенидов со сплавом свинца и натрия. Иногда для ускорения реакции в реакционную массу добавляют такие основания, как пиридин. В
промышленном масштабе проводили синтез тетраэтилсвинца из этилхлорида и сплава свинца с натрием.
Ещё один способ образования Pb–С-связи представлен присоединением соединений с Pb–Н-связью к С=С-связям в составе эфиров акриловой кислоты,
акрилонитрила, стирола и аналогичных непредельных соединений:
(C4H9)3PbH + CH2 CHCN  (C4H9)3PbCH2CH2CN
(C4H9)3PbCH2CH2CN
Эта реакция протекает без катализатора уже при температуре около 0 С. Особенно легко идёт присоединение гидроплюмбанов к алкинам с концевой тройной связью.
Тетраалкилплюмбаны можно использовать в качестве реагентов в синтезе других элементоорганических соединений. Так, например, тетраэтилсвинец реагирует при охлаждении с трихлоридом фосфора по реакции:
Pb(C H ) |
+ |
2 PCl |
(C H ) |
PbCl |
+ |
2 C H PCl |
||||
2 |
5 4 |
|
3 |
2 |
5 2 |
2 |
|
2 |
5 |
2 |
Образующийся при этом диэтилдихлорплюмбан реагирует с ещё одной молекулой трихлорида фосфора только при нагревании:
(C |
H ) |
PbCl |
+ |
PCl |
PbCl |
+ |
C H PCl |
+ |
CH Cl |
||
2 |
5 2 |
2 |
|
3 |
2 |
|
2 |
5 |
2 |
|
3 |
Органические производные свинца находят применение в составе катализаторов реакций полимеризации, в качестве катализаторов реакций этерификации и переэтерификации, в присадках к смазочным маслам. Тетраэтилсвинец использовался в качестве добавки к моторным топливам для повышения октанового числа. При этом надо принимать во внимание, что все соединения свинца токсичны. Органические производные свинца раздражают слизистые оболочки и кожу. Важно также, что отравление можно получить при многократном поступлении в организм небольших доз содержащих свинец соединений, поскольку все они обладают кумулятивным эффектом.
Органические производные металлов четвёртой группы – кремния, германия, олова и свинца – представляют собой соединения с наименее реакционноспособными связями
41
атомов металлов с атомом углерода. Известно использование тетраэтилсвинца для повышения октанового числа моторного топлива.
42

11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
Гидролиз и ацидолиз эфиров кислот фосфора.
*точно также гидролиз эфира дибутилфосфинистой кислоты приводит к образованию соединения с тетракоординированным атомом фосфора, которое может называться как дибутилфосфинистой кислотой, так и дибутилфосфиноксидом:
C H |
|
|
|
C H |
O |
|
||
4 |
9 |
|
|
|
4 |
9 |
|
|
|
P |
OC |
H |
+ H O |
|
P |
+ C H OH |
|
|
|
2 |
5 |
2 |
|
|
2 |
5 |
C H |
|
|
|
C H |
H |
|
||
4 |
9 |
|
|
|
4 |
9 |
|
|
*Диэфиры фосфорной кислоты могут быть также получены в результате гидролиза триэфиров в присутствии щелочей, поскольку эта реакция, как отмечалось выше,
приводит к образованию стабильных в щелочных средах солей диэфиров:
(C H O) PO |
+ |
NaOH |
(C H O) POONa |
+ |
C H OH |
|||||
4 |
9 |
3 |
|
|
4 |
9 |
2 |
|
4 |
9 |
*Трибутиловый эфир фосфорной кислоты, используемый в качестве экстрагента для выделения и очистки солей тяжёлых металлов, в частности, урана, получают только из бутанола и фосфорилхлорида. Эта реакция не требует присутствия акцепторов хлористого водорода, хотя она может сопровождаться образованием бутилхлорида и дибутилфосфата в результате ацидолиза эфирных связей хлористым водородом:
POCl |
|
+ |
3 C H OH |
(C H O) PO |
+ 3 HCl |
|||||||
|
3 |
|
4 |
9 |
|
4 |
9 |
3 |
|
|
|
|
(C H O) PO |
+ HCl |
(C H O) POOH |
+ |
C H Cl |
||||||||
4 |
9 |
3 |
|
|
|
4 |
9 |
|
2 |
|
4 |
9 |
Электронная структура атома фосфора 1s22s22p63s23p3 предполагает возможность образования соединений трикоординированного фосфора с тремя σ-связями,
образованными р-электронами 3p3. В соответствии с этим при хлорировании элементного фосфора получают его трихлорид, однако при гидролизе трихлорида фосфора образуется фосфористая кислота, которая имеет только две гидроксильные группы и в соответствии с этим представляет собой двухосновную кислоту. Очевидно,
43

что такое превращение потенциально трёхосновной кислоты в двухосновную связано с таутомерией, равновесие которой практически полностью сдвинуто вправо:
PCl |
+ 3 H O |
H PO |
+ 3 HCl |
|||
3 |
|
2 |
3 |
3 |
|
|
HO |
|
|
|
|
HO |
O |
|
P |
OH |
|
|
|
P |
HO |
|
|
|
|
HO |
H |
Строение фосфористой кислоты впервые стало предметом научного исследования в защищенной в шестидесятые годы ХIХ века магистерской диссертации русского ученого Н.А.Меншуткина на тему «О водороде фосфористой кислоты, не способном к металлическому замещению при обыкновенных условиях для кислот» (одним из оппонентов на защите был Д.И.Менделеев). Эта изомерия имеет некоторое сходство с кетоенольной таутомерией, однако в этом случае электроны атома фосфора образуют более выгодную в энергетическом отношении гибридизованную систему связей (в
соответствии с приведенной выше классификацией σ4λ5), аналогичную sp3-гибридизации у атома углерода. Это означает, что во всех случаях, когда фосфорильная группа может образовываться – она образуется.
Взаимодействие трихлорида фосфора со спиртами должно приводить к триэфирам фосфористой кислоты, однако при проведении этой реакции без использования акцепторов хлористого водорода она протекает с образованием диалкилфосфитов,
структура которых соответствует эфирам представленной выше фосфористой кислоты с тетракоординированным атомом фосфора. Это связано с тем, что полученные в результате замещения атомов хлора в трихлориде фосфора триэфиры реагируют с хлористым водородом с образованием соответствующих алкилхлоридов и диалкилфосфитов по схеме:
PCl |
+ 3 ROH |
(RO) P + 3 HCl |
(RO) |
P(O)H + 2 HCl + RCl |
2 |
|
|||
3 |
|
3 |
|
|
Превращение триалкилфосфита при действии хлористого водорода начинается с протонирования нуклеофильного атома фосфора с образованием квазифосфониевого промежуточного соединения, мезомерная форма которого с положительным зарядом
44
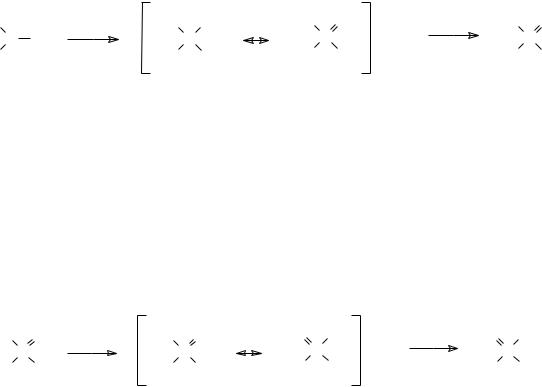
на атоме кислорода легко элиминирует алкильный карбокатион, соединяющийся с хлоридным анионом:
|
|
|
|
|
RO |
|
+ |
|
|
|
|
|
RO |
|
+ HCl |
RO |
+ OR |
|
OR |
_ |
|
|
RO |
O |
|
|
|
P |
|
|
|
|||||||
P |
OR |
|
|
P |
RO |
H |
Cl |
_ |
RCl |
|
P |
|
RO |
|
|
RO |
H |
|
|
RO |
H |
||||
|
|
|
|
|
Для повышения выхода диалкилфосфитов в реакции трихлорида фосфора с низшими спиртами взаимодействие проводят при интенсивном охлаждении, так как хлористый водород может реагировать с эфирами кислот фосфора в электронном состоянии σ4λ5 по схеме ацидолиза. Для диалкилфосфитов этому превращению соответствует механизм, основанный на протонировании атома кислорода в фосфорильной группе:
|
|
|
|
|
+ |
+ |
|
|
|
|
|
RO |
|
O |
|
RO |
RO |
OH |
|
|
O |
OH |
|
|
+ HCl |
OH |
_ |
|
|||||||
|
P |
|
|
P |
P |
Cl |
|
|
P |
||
|
|
|
|
_ |
RCl |
|
|||||
RO |
|
H |
|
RO |
H |
RO |
H |
RO |
H |
||
|
|
|
Если реакцию трихлорида фосфора со спиртом проводят при повышенной температуре, например, при добавлении трихлорида фосфора к кипящему спирту, то основным продуктом реакции становится соответствующий алкилхлорид и фосфористая кислота. Интересно также, что гидролиз эфиров кислот фосфора с фосфорильной группой при нагревании в 10 %-ной соляной кислоте приводит к образованию алкилхлоридов, а
не спиртов. То есть речь и в этом случае идет о реакции ацидолиза. При этом высшие первичные спирты, в частности, бутиловый спирт, могут реагировать с трихлоридом фосфора с образованием диалкилфосфитов при температуре до 50°С, т.е. высшие диалкилфосфиты более устойчивы к действию хлористого водорода.
**Соединения фосфора склонны к таутомерии между трикоординированной и тетракоординированной формами. В реакциях, в которых образуется незамещённая гидроксильная группа, обязательно происходит перегруппировка в тетракоординированное состояние, где водород напрямую связан с атомом фосфора.
Гидролиз эфиров кислот не стал исключением, поэтому в этих реакциях, например при
45

водном гидролизе триалкилфосфитов, образуются диалкилфосфиты с фосфором в тетракоординированном состоянии.
Триалкилфосфиты можно было бы получать взаимодейстием трихлорида фосфора и спиртов, однако, в данной реакции образуются не триалкил-, а диалкилфосфиты с тетракоординированным фосфором. Причиной тому ацидолиз, происходящий вследствие взаимодействия между образующимся триалкилфосфитом и хлороводородом.
|
|
|
|
|
RO |
|
+ |
|
|
|
|
|
RO |
|
+ HCl |
RO |
+ OR |
|
OR |
_ |
|
|
RO |
O |
|
|
|
P |
|
|
|
|||||||
P |
OR |
|
|
P |
RO |
H |
Cl |
_ |
RCl |
|
P |
|
RO |
|
|
RO |
H |
|
|
RO |
H |
||||
|
|
|
|
|
Ацидолиз может протекать и далее, до образования моноалкилфосфита, и для увеличения выхода по диалкилфосфитам реакция проводится при охлаждении.
|
|
|
|
|
+ |
+ |
|
|
|
|
|
RO |
|
O |
|
RO |
RO |
OH |
|
|
O |
OH |
|
|
+ HCl |
OH |
_ |
|
|||||||
|
P |
|
|
P |
P |
Cl |
|
|
P |
||
|
|
|
|
_ |
RCl |
|
|||||
RO |
|
H |
|
RO |
H |
RO |
H |
RO |
H |
||
|
|
|
Реакция МакКенны, получение триметилсилильных эфиров кислот фосфора.
Алкиловые эфиры кислот фосфора достаточно трудно поддаются гидролизу,
поэтому для синтеза кислых фосфатов и фосфонатов сложного строения,
представляющих собой биомолекулы, метаболиты в биохимических превращениях или промежуточные продукты для их получения, а также для получения их фосфонатных аналогов, используют бензиловые или силиловые эфиры производных кислот фосфора,
которыми и проводят фосфорилирование соответствующих соединений. В полученных несимметричных эфирах бензильные группы снимают гидрированием по методикам,
используемым в пептидных синтезах, а силильные группы легко снимаются даже протонными растворителями, например, водой. Самым распространенным способом получения силиловых эфиров кислот фосфора является взаимодействие соответствующих кислот с активными силилирующими реагентами. В качестве таких реагентов чаще всего используют галогеносиланы в присутствии третичных аминов,
аминосиланы, силазаны, силиламиды, алкокси- и ацилоксиланы, силоксаны, силанолы и
46

силаноляты, а также гидросиланы в катализируемых переходными металлами реакциях.
Так, например, силилирующим реагентом может быть триметисилан в присутствии коллоидного никеля:
|
(CH |
) |
SiH, Ni (coll) |
(CH ) |
SiO |
O |
|
3 3 |
|
||||
H PO |
|
|
3 3 |
|
|
|
|
|
|
|
P |
||
3 |
4 |
|
|
|
|
|
|
|
|
|
(CH ) |
SiO |
OSi(CH ) |
|
|
|
|
3 3 |
|
3 3 |
Более удобный способ получения трис(триметилсилил)фосфата представлен реакцией гексаметилдисилоксана с фосфорным ангидридом:
|
|
(CH |
) |
SiOSi(CH ) |
(H C) SiO |
O |
|
|
|
|
3 |
3 |
|
|
|||
P O |
3 3 |
3 3 |
|
|
P |
|
||
|
|
|
|
|
|
|||
4 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
(H C) SiO |
OSi(CH |
) |
|
|
|
|
|
|
3 |
3 |
3 3 |
|
К сожалению, триметилсилильные защитные группы при атоме кислорода не позволяют проводить реакции соответствующих производных кислот фосфора в протонных средах или в присутствии соединений с подвижными атомами водорода. В
соответствии с этим для перевода алкиловых эфиров кислот тетракоординированного фосфора в соответствующие силиловые эфиры используют реакцию с триметилсилилбромидом (TMSBr, Charls A. McKenna, 1977 год). Эта реакция протекает в мягких условиях, при этом многие другие функциональные группы в составе молекулы фосфорорганического соединения не затрагиваются. Этот способ совместим с такими группами, как бензильные, бензоильные, алкоксиалкильные, алкенильные,
трихлорметильные, диазометильные группы, а также карбоксилатные группы эфиров карбоновых кислот в составе фосфорорганического соединения. Реакция при этом протекает по схеме:
R |
O |
TMSBr |
R |
+ |
O |
Si(CH ) |
|
||
P |
|
|
|
|
|
3 3 |
|
||
|
|
|
P |
|
|
Br |
- |
|
|
CH O |
OCH |
|
CH O |
|
OCH |
|
- CH Br |
||
3 |
3 |
|
|
|
|
||||
|
|
|
3 |
|
|
3 |
|
|
3 |
R O
P 
CH3O OSi(CH3)3
47

Опыты, поставленные с метиловыми, этиловыми и изопропиловыми эфирами фосфоновых кислот показывают, что реакционная способность алкильных групп в этом ряду соответствует соотношению 1:0,25:0,04. В соответствии с этим для получения моноизопропиловых эфиров фосфоновых кислот можно использовать деалкилировние соответствующих метил-изопропилфосфонатов. Эта реакция, которую иногда называют реакцией МакКенны, подвергалась многочисленным модификациям, в частности,
исследовалось влияние температуры реакции и соотношения реагентов. Вместо триметилсилилбромида можно использовать триметилсилилиодид, образующийся in situ из триметилсилилхлорида и иодида натрия или лития. Сам триметилсилилхлорид реагирует с эфирами фосфоновых кислот при кипячении в течение нескольких дней или даже недель. Триметилсилилиодид характеризуется более высокой реакционной способностью и для исключения побочных реакций деалкилирование этим реагентом надо проводить при пониженных температурах (до -20 С).
В качестве примера можно привести способ получения ацилфосфоновых кислот. В
эфирах фосфоновых кислот, атом фосфора которых непосредственно связан с ацильной группой, РС-связь гидролизуется даже скорее, чем эфирные связи. В соответствии с этим для получения ацилфосфоновой кислоты её диметиловый эфир переводят в бис(триметилсилил)ацилфосфонат действием иодида калия и триметилсилилхлорида в ацетонитриле и снимают триметилсилильные группы действием метанола:
CH O |
O |
|
TMSCl, KI |
(CH ) |
SiO |
O |
|
|
|
HO |
O |
|
|
3 |
|
|
|
CH OH |
|
|
|
||||||
|
|
|
3 3 |
|
|
|
|
|
|
||||
|
P |
|
|
|
|
P |
|
|
3 |
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH O |
CO |
R |
- CH |
I |
(CH ) |
SiO |
CO |
R |
- (CH ) |
SiOCH |
HO |
CO |
R |
3 |
|
|
3 |
|
|
|
|
||||||
|
|
|
|
3 3 |
3 |
|
|
|
|||||
|
|
|
|
|
3 3 |
|
|
|
|
|
|
|
|
48
