
- •1. Стабильность Si-C-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •26. Присоединение диалкилфосфитов к кратным связям (С=С, С=О, С=N), реакция Абрамова и Пудовика.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •42. Антихолинэстеразная активность фосфорорганических соединений. Обратимое и необратимое ингибирование холинэстеразы. Примеры обратимого и необратимого ингибирования в ряду фосфорорганических инсектицидов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •45. 2-Хлорэтильные производные в ряду кремний- и фосфорорганических соединений. Синтез хлорэтилфосфоновой кислоты, механизм дефолиантного действия.
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение О-метил-О-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило ЖМКО в реакции их солей с органическими галогенидами
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.

4. Способы получения и химические свойства литийорганических соединений.
1)Реакция металлического лития с соответствующим галогенидом – основной способ получения литийорганических соединений
Нельзя использовать для получения литийорганических соединений алкилиодиды, поскольку они реагируют с литием по реакции Вюрца.
В соответствии с этим для увеличения выхода и для получения свободных от галогенидов лития растворов литийорганических соединений лучше всего использовать в качестве исходных соединений хлорпроизводные в алифатическом ряду и бромпроизводные в ароматическом.
При этом следует отметить, что по схеме реакции Вюрца с металлическим литием реагируют и реакционноспособные органические хлориды, например, аллилили бензилхлориды.
2)Некоторые простые эфиры реагируют с металлическим литием так же, как и
алкилили арилгалогениды. Так, например, бензиллитий может быть получен с хорошим
выходом из бензилалкиловых эфиров в тетрагидрофуране, например, по реакции:
CH OCH |
3 |
|
|
|
CH Li |
2 |
|
|
|
2 |
|
|
+ |
2 Li |
|
|
+ CH OLi |
|
|
|
|
|
3 |
|
|
|
|
|
|
3)В метилале СН2(ОСН3)2 действием лития на хлорметиловый эфир можно
получить метоксиметиллитий:
CH OCH Cl |
+ |
2 Li |
CH OCH Li |
+ |
LiCl |
||
3 |
2 |
|
|
3 |
2 |
|
|
4)Определённое значение имеет способ получения литийорганических
соединений в соответствии с общей схемой:
RHal + R1Li |
|
RLi + R1Hal |
|
Равновесие в этой реакции сдвинуто в сторону образования литийорганического соединения, органическая составляющая которого лучше воспринимает состояние с частичным анионным статусом.
15
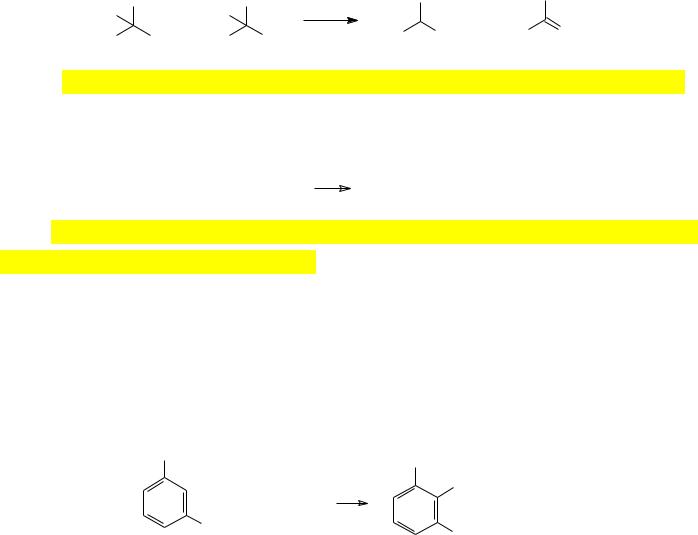
Хорошие результаты получаются, когда в этой обменной реакции галоген представлен атомом брома, но при использовании в качестве литиирующего реагента бутиллития побочным продуктом реакции становится достаточно реакционноспособный бутилбромид. При повышении температуры он может реагировать с образовавшимся литийорганическим соединением или вступать в реакцию с продуктом его дальнейшего превращения. Если присутствие бутилбромида в реакционной массе нежелательно, то для реакции литиирования берут два эквивалента третбутиллития. В этом случае образовавшийся третбутилбромид реагирует с избытком третбутиллития с образованием изобутена, изобутана и бромида лития:
|
|
|
|
|
|
|
|
CH |
|
|
CH |
|
CH |
|
|
CH |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
3 |
|
|
|
||
H C |
3 |
|
H C |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
||
3 |
|
+ |
3 |
|
_ |
|
|
|
|
|
|
|
|
|
|
|
H C |
CH |
|
H C |
CH |
||
|
|
|
|
|
LiBr |
|
|||||
H C |
Li |
|
H C |
Br |
|
3 |
|
3 |
|
|
|
3 |
|
|
3 |
|
|
|
|
|
|
|
|
5)Литийорганические соединения можно также получать из реактивов Гриньяра. В
качестве примера можно привести реакцию бензилмагнийхлорида с металлическим литием:
C H CH MgCl |
+ |
2 Li |
C H CH Li |
+ |
LiCl |
+ |
Mg |
||||
6 |
5 |
2 |
|
|
6 |
5 |
2 |
|
|
|
|
6)Ещё один способ получения литийорганических соединений представлен замещением литием атома водорода. Особенно легко эти реакции протекают на активированных СН-связях, например, при взаимодействии бутиллития с ацетиленом и с монозамещенными ацетиленами, а также с трифенилметанами. Ароматические соединения с электронодонорными заместителями также могут вступать в реакции обмена атома водорода на литий. В качестве примера можно привести реакцию фениллития с диметиловым эфиром резорцина:
OCH |
|
OCH |
|
|
3 |
|
|
|
|
|
|
3 |
|
|
|
|
Li |
|
|
+ |
C H Li |
+ |
C H |
|
|
6 5 |
|||
|
|
|
6 |
6 |
OCH |
|
OCH |
|
|
3 |
|
|
|
|
|
|
3 |
|
|
16
Высокая нуклеофильность литийорганических соединений не позволяет проводить по этой схеме реакции обмена атома водорода на атом лития на соединениях с электрофильными функциональными группами. В этом случае в качестве литиирующего реагента используют диизопропиламид лития ([(CH3)2CH]2NLi, LDA) или 2,2,6,6-
тетраметил-пиперидид лития, анионы которых проявляют исключительно основные свойства. В отдельных случаях можно использовать в реакция литиирования и менее основный гексаметилдисилазид лития [(CH3)3Si]2NLi.
Синтезы с участием литийорганических соединений во многом аналогичны превращениям, в которых участвуют представленные ниже реактивы реактивы Гриньяра*, но более высокая реакционная способность органических производных лития позволяет проводить с их участием и специфические превращения.
1)К ним относятся, например, реакции присоединения к двойным азот-углеродным связям в составе гетероциклических соединений. В качестве примера приводится реакция получения 2-фенилпиридина:
|
C6H5Li |
H O, O |
|
|
H |
2 |
2 |
N |
|
N |
|
NLi |
|
||
|
|
||
Взаимодействие пиридина с фениллитием протекает при температуре 110°С. В
соответствии с этим в инертной атмосфере к раствору фениллития в эфире прибавляют раствор сухого пиридина в толуоле, отгоняют эфир и нагревают реакционную массу с обратным холодильником в течение 8 часов. После разложения образовавшегося продукта присоединения водой окисление образующегося 2-фенилдигидропиридина идёт кислородом воздуха.
2)Определённое препаративное значение имеют также реакции литийорганических соединений, протекающие с образованием азот-углеродных связей.
В их основе лежит замещение уходящей группы связанным с атомом лития остатком или присоединение литийорганического соединения по кратной связи между атомами
азота, например:
17
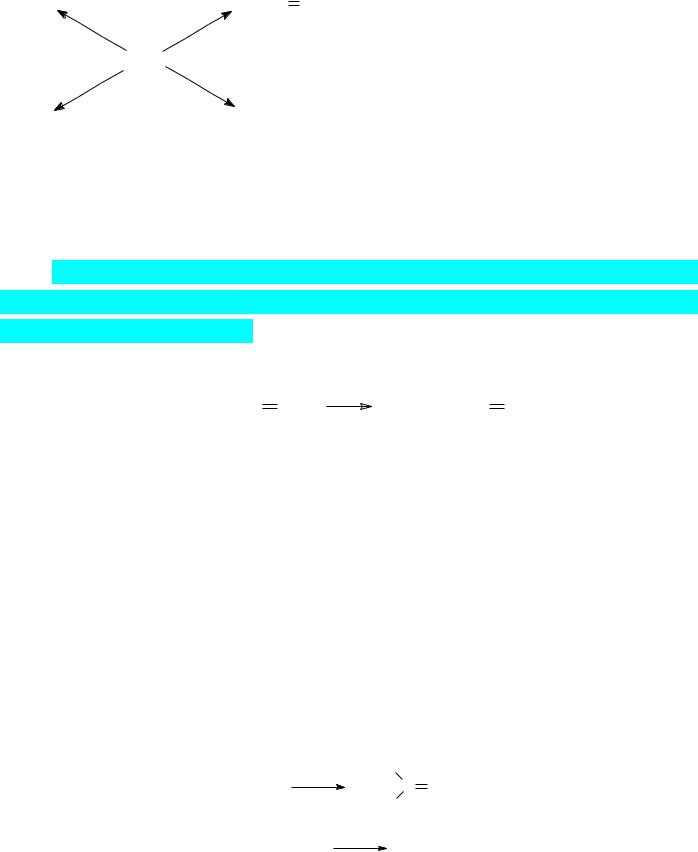
RNH2 |
1 |
1 |
RNHN NR1 |
|
|
R ONH2 |
R N3 |
|
|
|
RLi |
|
|
|
R1ONO2 |
|
R1SO N |
3 |
|
|
|
|
2 |
|
RNO2 |
|
|
RN3 |
|
*Реакции, аналогичные превращениям с реактивами Гриньяра
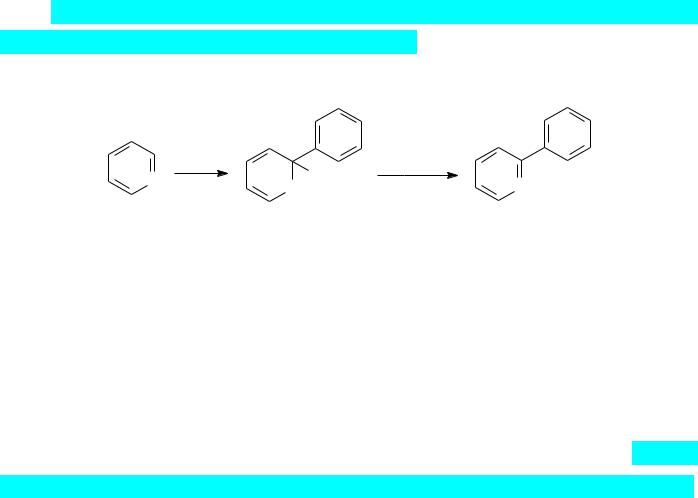
3)Магнийорганические соединения могут вступать в реакции с реакционноспособными органическими галогенидами с образованием С-С-связей по типу реакции Вюрца–Фиттига. Так, например, фенилмагнийбромид реагирует с аллилхлоридом с образованием аллилбензола:
C H MgBr + ClCH CH |
CH |
C H CH CH |
CH |
+ |
MgBrCl |
||||
6 |
5 |
2 |
2 |
6 |
5 |
2 |
2 |
|
|
По схеме гетеросочетания реактивы Гриньяра реагируют и с другими |
|||||||||
органическими |
галогенидами с |
активными |
атомами |
галогена |
(например, с |
||||
α-хлорзамещёнными простыми эфирами). |
|
|
|
|
|
|
|||
Заметное различие в реакционной способности магний- и литийорганических соединений демонстрируется в реакциях гетеросочетания с такими третичными галогенидами, как третбутилбромид. Литийорганическое соединение, представляющее собой сильное основание, реагирует с третбутилбромидом с отщеплением бромистого водорода, тогда как реактив Гриньяра реагирует с этим галогенидом, замещая атом
брома по механизму SN1:
|
|
H C |
|
|
|
3 |
|
(CH ) |
CBr + RLi |
C CH |
+ RH + LiBr |
3 3 |
|
2 |
|
|
|
H C |
|
|
|
3 |
|
(CH)CBr+RMgX |
(CH)CR+MgBrX |
||
|
33 |
33 |
|
Много внимания уделяется реакциям гетеросочетания реактивов Гриньяра с алкинильными, алкенильными и арильными галогенидами. Выходы в этих реакциях могут быть значительно повышены добавлением таких катализаторов, как соли меди,
18
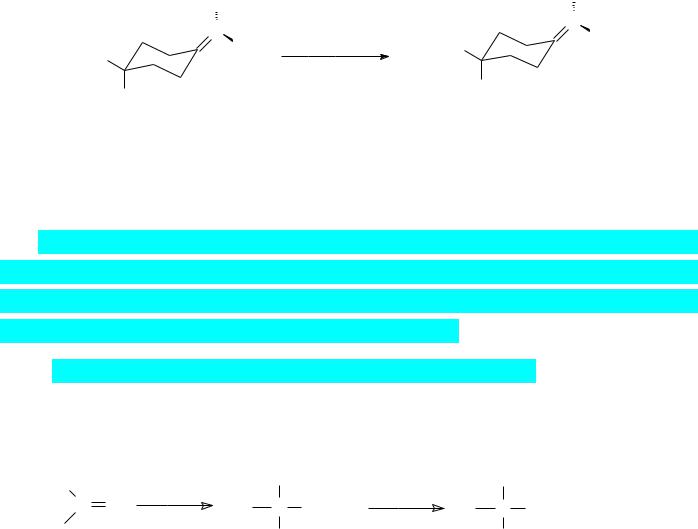
серебра, железа или никеля в стехиометрическом или в каталитическом количестве. В
качестве примера можно привести реакцию (S)-(4-метилциклогексилиден)-бромметана с метилмагнийбромидом:
|
H |
|
|
H |
|
|
|
|
|
|
C |
|
|
C |
|
CHMgBr |
|
CH |
|
|
Br |
HC |
3 |
|
|
3 |
|
||
HC |
|
|
3 |
|
|
|
|
|
|
3 |
|
|
|
|
H |
|
|
H |
|
|
|
|
|
В присутствии никелевых и кобальтовых катализаторов эта реакция протекает с сохранением хиральности, тогда как катализаторы с ионами серебра приводят к полной рацемизации продукта реакции.
основная область применения магнийорганических соединений представлена реакциями с образованием С–С-связей в результате их присоединения к карбонильным группам в составе альдегидов, кетонов или сложных эфиров, а также в результате присоединения к иминам, нитрилам и диоксиду углерода.
4)Взаимодействие реактива Гриньяра с карбонильной группой представляет собой восстановительный процесс, поскольку образование новой С–С-связи приводит к превращению карбонильной группы в спиртовую:
R |
2 |
|
R |
|
H O |
|
R |
|
|
R MgBr |
|
|
|
|
|
|
|
C |
O |
1 |
C |
OMgBr |
2 |
1 |
C |
OH |
|
||||||||
1 |
|
R |
|
R |
||||
R |
|
|
2 |
|
|
|
2 |
|
|
|
|
R |
|
|
|
R |
|
Если в этой реакции R1 означает атом водорода, то продуктом реакции становится вторичный спирт, а взаимодействие с реактивом Гриньяра кетона (R1 означает органический остаток) приводит к третичному спирту.
Литийорганические соединения реагируют с кетонами так же, как и магнийорганические соединения. Однако они более реакционноспособны, что позволяет использовать их в тех случаях, когда реактивы Гриньяра с кетонами не реагируют. В соответствии с этим реакции по карбонильным группам стерически затруднённых кетонов лучше проводить с литийорганическими соединениями. Так,
19

например, для получения триизопропилкарбинола проводят взаимодействие
диизопропилкетона с изопропиллитием:
|
|
|
|
|
|
|
|
|
CH(CH ) |
|
|
|
|
|
|
|
|
|
|
|
3 2 |
(CH ) |
CH |
C |
CH(CH ) |
+ |
(CH ) |
CHLi |
(CH ) |
CH |
C |
CH(CH ) |
3 2 |
|
|
3 2 |
|
3 2 |
|
3 2 |
|
|
3 2 |
|
|
O |
|
|
|
|
|
|
OLi |
|
5)Действие реактивов Гриньяра на сложные эфиры (в приведенном выше общем уравнении R означает алкоксильную группу) также приводит к образованию третичных спиртов, поскольку образующиеся в результате первичного присоединения магнийорганического соединения аддукты разлагаются на алкоголят и кетон:
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
O |
|
|
|
|
OR |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
R |
C |
+ |
R MgBr |
R |
C |
OMgBr |
R |
C |
+ |
1 |
||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
2 |
|
|
|
2 |
|
|
|
OR |
|
|
|
|
|
|
R |
|
|
||
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
O |
|
|
|
|
R |
|
H O |
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
R |
C |
+ |
R MgBr |
|
R |
C |
OMgBr |
2 |
R |
C |
OH |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
2 |
|
|
|
|
R |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
R |
|
|
|
R |
|
На первой стадии реакцию можно остановить только с эфирами муравьиной кислоты.
В соответствии с этим 6)гидролиз продуктов присоединения реактивов Гриньяра к формиатам приводит к альдегидам:
|
|
|
|
|
OC H |
|
|
|
||
|
|
|
|
|
|
2 |
5 |
H O |
|
|
|
|
|
|
|
|
|
|
|
|
|
RMgBr |
+ |
HCOOC H |
R |
C |
OMgBr |
2 |
R |
CHO |
||
|
||||||||||
|
|
2 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
7)Гладко реагируют с реактивами Гриньяра ортоэфиры карбоновых кислот:
OC2H5
RMgBr + H3CC(OC2H5)3 |
H3C |
|
C |
|
R + C2H5OMgBr |
|
|
OC2H5
Образующиеся при этом кетали можно перевести в кетоны действием водных растворов сильных кислот.
20
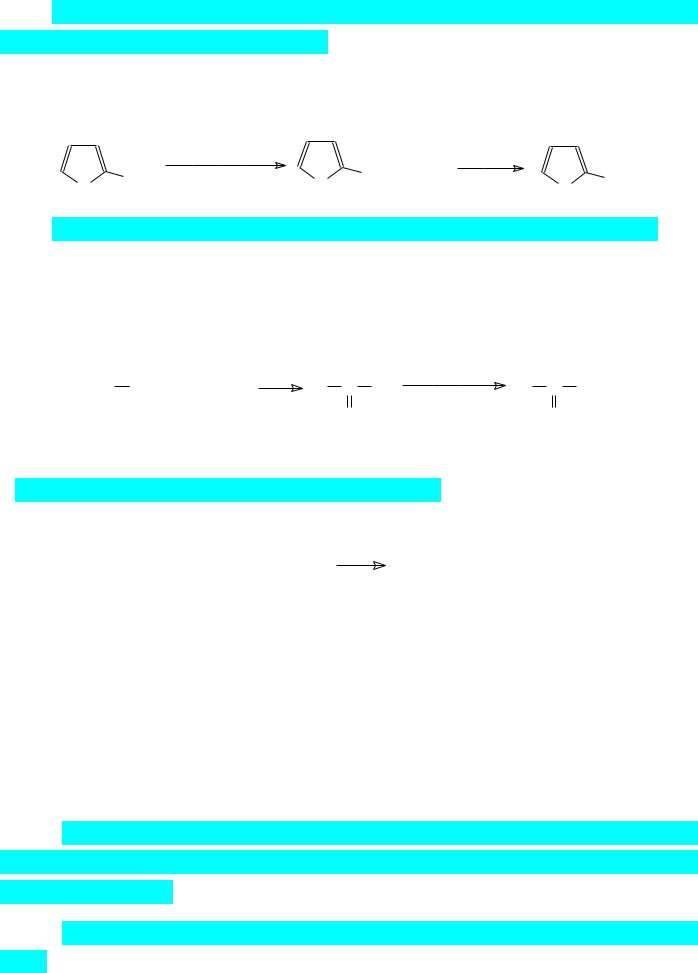
8)Взаимодействие реактивов Гриньяра с триэтилортоформиатом можно использовать для получения альдегидов. Так, например, из полученного на основе 2-
бромтиофена магнийорганического соединения и триэтилортоформиата получают
2-формилтиофен:
|
HC(OC H ) |
|
|
|
H O |
|
|
|
2 |
5 3 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
MgBr |
|
|
CH(OC H ) |
|
CHO |
|
S |
|
S |
2 |
5 2 |
S |
||
|
|
|
|
|
|||
|
|
|
|
|
|
||
9)С низкой скоростью идёт взаимодействие реактивов Гриньяра с нитрилами. При длительном кипячении в эфире или при нагревании в растворителях с более высокой температурой кипения в этой реакции образуются соли кетиминов, гидролиз которых приводит к кетонам:
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
H , H O |
|
|
|
R |
CN |
+ |
1 |
R |
C |
1 |
2 |
R |
C |
1 |
|
||||||||||
R MgX |
R |
|
R |
|||||||
|
|
|
|
|
NMgX |
|
|
O |
|
|
При пониженных температурах и при интенсивном перемешивании проводят
9)реакцию реактивов Гриньяра с диоксидом углерода, протекающую с образованием солей соответствующих карбоновых кислот:
RMgBr |
+ |
CO |
RCOOMgBr |
|
|
2 |
|
Поддерживая температуру от 10 до –10 °С, при перемешивании пропускают диоксид углерода над эфирным раствором реактива Гриньяра. Такой способ введения в
реакцию диоксида углерода нужен для того, чтобы осадок образующей соли карбоновой кислоты не забивал трубку для подачи СО2. Можно также приливать раствор магнийорганического соединения к измельченной твёрдой углекислоте. Для протекания реакции с некоторыми магнийорганическими соединениями, полученными из третичных галогенидов, требуется повышенное давление СО2.
10)Реактивы Гриньяра присоединяются также к кратным связям с участием других гетероатомов, например, к С=S-связям в тиоэфирах или к кратным СN-связям в иминах или в карбодиимидах.
11)Реактивы Гриньяра реагируют с алкиленоксидами с раскрытием оксиранового цикла, например, по схеме:
21
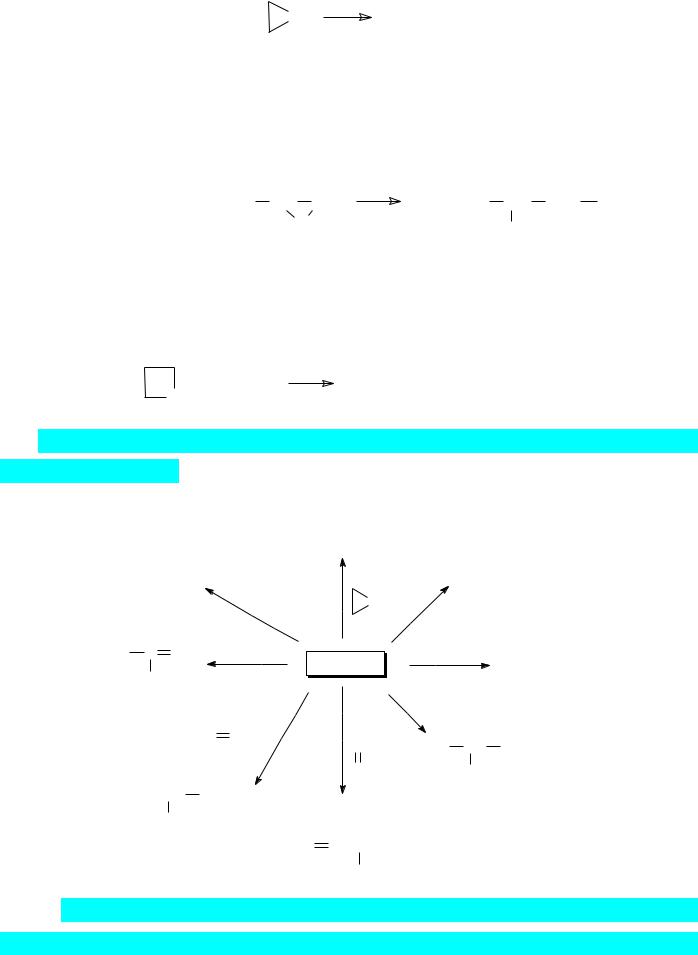
RMgBr |
+ |
O |
RCH CH OMgBr |
|
|
|
|
2 |
2 |
В результате реакции с этиленоксидом образуется первичный спирт, с увеличенной на две метиленовых группы углеводородной цепью. При взаимодействии с замещёнными оксиранами органический остаток в составе реактива Гриньяра присоединяется к наименее стерически затрудненному атому углерода:
C H MgBr |
+ |
(CH ) |
CH |
CH CH |
(CH ) |
CH |
CH CH |
C H |
|||
2 |
5 |
|
3 |
2 |
|
2 |
3 2 |
|
2 |
2 |
5 |
|
|
|
|
|
|
O |
|
|
OMgBr |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
По аналогичной схеме реагируют с магнийорганическими соединениями оксетаны.
При этом продуктами реакции становятся спирты с углеводородной цепью, удлиненной на три атома углерода:
+ |
RMgBr |
RCH CH CH |
OMgBr |
||
O |
|
2 |
2 |
2 |
|
|
|
|
|
|
|
Общая картина превращений, протекающих с использованием реактивов Гриньяра,
представлена схемой, в которой в качестве исходного соединения используется метилмагнийбромид:
|
|
|
CH CH CH OH |
|
|
||
|
|
|
3 |
2 |
2 |
|
|
|
|
RCOCH |
|
|
|
CH OH |
|
|
|
3 |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
RCOCl |
|
O O |
|
|
|
|
|
|
|
2 |
|
|
R |
C |
NH |
RCN |
|
|
CO |
2 |
|
|
|
|
|
|
|
CH COOH |
|
CH |
|
|
|
|
3 |
|
|
|
|
|
|
|
||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
RCHO |
|
|
|
RCH |
NCH |
|
CH |
R |
CH OH |
|
|
|
|
|
|||
|
|
|
|
|
2 |
||
|
|
|
|
|
CHCHO |
|
CH |
|
|
|
|
|
|
|
3 |
|
RCH NHCH |
|
|
|
|
||
|
|
|
3 |
|
|
|
|
|
|
CH |
CH CH CH CHO + |
|
|
||
|
|
3 |
2 |
2 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
CH |
CHCHCH |
|
|
|
|
|
|
2 |
|
3 |
|
|
|
|
|
|
|
OH |
|
|
12)В отдельных случаях стерически затрудненные карбонильные соединения или стерически затрудненные реактивы Гриньяра реагируют с образованием енольных
22
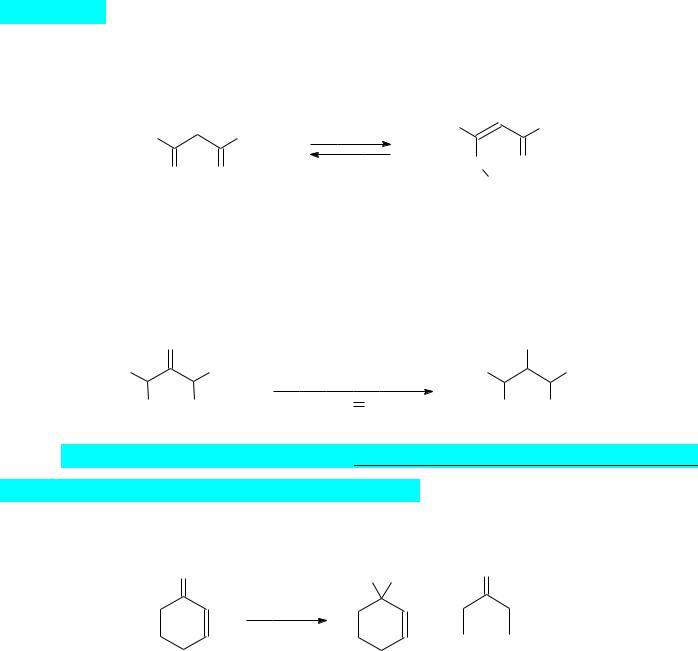
производных. Чаще всего енолизация при действии стерически затрудненных магнийорганических соединений протекает с СН-кислотами, представленными β-
дикарбонильными соединениями:
|
|
|
RMgX |
H C |
|
CH |
H C |
|
CH |
3 |
|
3 |
|
3 |
|
3 |
|
|
|
|
|
|
|
+ |
|
O |
O |
O |
O |
|
H |
|
|
MgX |
|
|
|
|
|||
|
|
|
|
|
|
В некоторых случаях реактивы Гриньяра с атомами водорода в β-положении восстанавливают карбонильные соединения вместо того, чтобы присоединяться по двойной связи:
O |
|
|
|
|
OMgBr |
|
H C |
CH |
+ RCH CH MgBr |
H C |
CH |
||
3 |
3 |
3 |
3 |
|||
|
|
|
2 |
2 |
|
|
CH |
CH |
_ |
RCH |
CH |
CH |
CH |
|
||||||
|
|
2 |
||||
3 |
3 |
|
|
|
3 |
3 |
13)Взаимодействие алкильных магнийорганических соединений с
α,β-ненасыщенными карбонильными соединениями протекает обычно с образованием смеси продуктов 1,2- и 1,4-присоединения, например:
O |
R |
OH |
O |
|
|
||
|
RMgX |
|
|
|
|
|
+ |
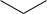
 R
R
Вреакции циклогексен-3-она с этилмагнийбромидом 3-гидрокси-3-
этилциклогексен (продукт 1,2-присоединения) образуется с выходом 52 %, выход продукта 1,4-присоединения (3-этилциклогексанона) составляет 24 %, а
третбутилмагнийхлорид реагирует с циклогексен-3-оном только по схеме
1,4-присоединения с образованием 3-третбутилциклогексанона с выходом до 70 %. В
отличие от этого аллильные и ароматические магнийорганические соединения всегда реагируют с ненасыщенными кетонами по схеме 1,2-присоединения.
23
14)Магнийорганические соединения, полученные из третичных алкилгалогенидов или арилгалогенидов, реагируют с бромидом серебра, хлоридом или бромидом меди(II)
по схеме реакции Вюрца, например, по реакции:
2 (CH ) |
CMgCl |
+ |
2 AgBr |
(CH ) |
C |
C(CH ) |
+ 2 MgBrCl |
+ |
2 Ag |
3 3 |
|
|
|
3 3 |
|
3 3 |
|
|
|
2. ЭОС Литий, натрий.docx
24
