
- •Семинары по физической химии 1 часть
- •Физическая химия
- •Теория
- •Задачи
- •Второй закон термодинамики
- •Объединенное выражение I и II начал термодинамики. Зависимость энтропии от параметров состояния
- •Типы задач
- •Рассчитайте изменение энтропии при изобарном нагревании 1 моль хлора от температуры 300 до 500 К. Воспользуйтесь справочными данными о зависимости теплоемкости хлора от температуры.
- •Рассчитайте изменение энтропии в реакции синтеза аммиака при температуре 598 К и давлении 1 атм.
- •Энергия Гиббса. Энергия Гельмгольца.
- •Типы задач
- •Рассчитайте изменение энергии Гиббса, если в результате расширения 20 кг гелия при 298 К объем газа увеличился в 1 000 раз. Газ считать идеальным.
- •Рассчитайте изменение энергии Гельмгольца, если в результате сжатия 500 моль кислорода при 400 К давление газа увеличилось в 100 раз. Газ считать идеальным.
- •Расчет изменения энергии Гиббса при смешении идеальных газов
- •54 г воды испаряются при 373 К и давлении 1 атм, а затем изотермически расширяются до давления 0,1 атм. Рассчитайте общее изменение энергии Гиббса и энергии Гельмгольца.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Уравнение Гиббса-Гельмгольца
- •Химическое равновесие
- •Влияние общего давления и добавления инертного газа на смещение равновесия
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изобары Вант-Гоффа
- •Методы расчета константы равновесия
- •Фазовое равновесие в однокомпонентных системах
- •Фазовое равновесие в однокомпонентных системах
- •Уравнение Клапейрона
- •Уравнение Клапейрона-Клаузиуса
- •Парциальные мольные величины
- •Методы определения парциальных молярных величин
- •Коллигативные свойства
- •Фазовая диаграмма для растворителя и раствора
- •Основные формулы
- •Основные формулы
- •В 1000 г воды растворили 0,0684 кг сахарозы (M = 342 г/моль). Удельная теплота испарения воды 2256,7 кДж/кг. Рассчитать давление пара над раствором при 500С и температуру кипения раствора. Воспользоваться справочными данными.
Уравнение Гиббса-Гельмгольца
• ΔGT = HT – T ST - для реакции
•HT= H298 + Cp(T-298) ST= S298 + Cp*ln(T/298)
Химическое равновесие
•Составление материальногобаланса. Степень превращения.
•Связь , , ,
•Влияние общегодавления и добавления инертногогаза на смещение равновесия
•Зависимостьконстантыравновесия оттемпературы(уравнение изобарыВант-Гоффа). Определение среднего и истинноготеплового эффекта.
•Уравнения стандартного( G°) и полногохимическогосродства (ΔG) – уравнение изотермыВант-Гоффа. Изменение направления протеканияпроцесса за счет изменения начальных давлений веществ.
•Методы расчета константы равновесия

Для реакции ½A+B→3C записать уравнение связи |
|
с равновесным |
|
количеством веществ и общим давлением Р. |
Записать уравнения связи |
||
|
|
|
|
с другимиконстантами ( , , ). |
|
|
|
исх
равн
=
1 |
|
|
+ |
|
|
|
1 |
|
|
|
|
→ |
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
½A |
|
|
|
|
|
|
B |
|
|
|
|
|
|
|
|
3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
21 − νν |
|
|
|
|
|
|
−31 |
|
|
|
|
|
|
|
|
образовавшеесяк моментуравновесия |
|||||||||||||||||||||
2 |
|
|
|
|
|
( |
|
общ) ( |
общ) |
|
|
|
|
|
|
общ |
∆ |
||||||||||||||||||||
|
= |
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
общ |
|
|
|
|
|
|
общ |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
( |
|
|
|
) |
|
( |
|
|
|
|
) |
|
|
|
|
|
|
|
|
|
|||||||||
общ |
∆ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
= |
|
= |
|
|
|
1 |
|
|
= общ |
общ1 |
1 |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
1 |
|
|
1 |
|
|
1/23 |
1 |
|
|
1 |
1 |
1 |
|
|
|
|
+ |
3/2 |
|
|
||||||||||||||||
|
|
|
|
|
(2 |
|
− 6 |
) |
( |
− |
3 |
) |
|
2 |
− 6 |
+ |
− |
3 |
|
|
|
|
|||||||||||||||

Для реакции ½A+B→3C записать уравнение связи |
|
с равновесным |
|
с другимиконстантами ( , , ). |
Записать |
|
|
количеством веществ и общим давлением Р. |
|
|
уравнения связи |
piV = niRT |
|
|
|
|
|
ci=ni/V |
|
pi = ciRT |
|||||||||
|
|
|
|
( ) |
( ) |
|
|
∆ |
|||||||||
|
= |
|
= ( ) ( ) |
= |
|
|
|||||||||||
|
|
= |
|
∆ |
− 1 |
|
3 |
− |
1 |
|
1 |
( ) |
|
|
|||
|
|
|
|
= 1 |
1/2 |
|
|
|
|
||||||||
|
|
|
|
|
2 |
6 |
( ) |
1 |
|
3 |
|
|
3/2 |
|
|
||
|
|
|
|
|
( |
|
|
) |
( |
|
|
|
|
) |
|
|
|
|
|
|
|
|
|
|
[ , (Па)3/2] |
|
|
|
|
|
|||||

Для реакции ½A+B→3C записать уравнение связи |
|
с равновесным |
||||||||||||||||||||||||
с другимиконстантами ( , |
, ). |
|
Записать уравнения связи |
|||||||||||||||||||||||
количеством веществ и общим давлением Р. |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
( общ) ( общ) |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
= общ |
|
|
|
|
|
|
|
||||||
|
= |
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
( общ) |
|
||||||||
|
|
|
|
|
|
|
|
|
( общ) |
|
|
|||||||||||||||
|
|
= |
|
|
|
|
|
|
|
|
|
1общ ∆ |
= |
общ ∆ |
||||||||||||
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
1 1 |
|
|
)−3 |
1 |
|
|
3 |
+ |
|
|
|
||||||||
|
|
|
= |
2 |
− 6(3+ |
3 + = 2 |
2 |
|
|
|||||||||||||||||
|
|
|
|
= |
|
|
1 − 1 |
1/2 |
1 |
− 1 |
1 |
( |
) |
3/2 |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
+ |
|
|
|
|
общ |
|
|
|||||||
|
|
|
|
|
|
2 |
6 |
|
2 |
|
|
3 |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
( |
|
) |
|
( |
|
|
|
) |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
3 |
|
|
|
3 |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
2 |
+ 2 |
|
|
|
|
2 |
+ 2 |
|
|
|
|
|
|
|
||||

Составитьматериальныйбаланс для газофазной реакции, зная количества веществ A, B,C, D до начала реакции.
|
A |
+ |
4B |
→ |
3C |
+ |
2D |
|
|
|
|
|
|
|
|
исх, моль |
1 |
|
2 |
|
3 |
|
0 |
|
|
|
|
|
|
|
|
равн (1), моль |
1 – 1/3x |
|
2 – 4/3x |
|
3 + x |
|
2/3x |
|
|
|
|
|
|
|
|
равн (2), моль |
1 – 1/2y |
|
2 – 2y |
|
3 + 3/2y |
|
0 + y |
равн (3), моль |
1 – z |
|
2 – 4z |
|
3 + 3z |
|
0 + 2z |
|
|
|
|
|
|
|
|
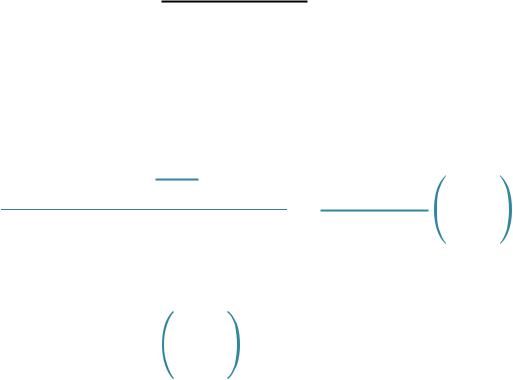
Определитьстепень диссоциацииPCl5 в реакцииPCl5(г) |
→ PCl3(г) + Cl2(г), |
|
||||||||||||||||||||||||||||||
если при150°С константа равновесия |
|
|
равна 0,333.Общее давление в |
|||||||||||||||||||||||||||||
системек моментуравновесия |
составляет 0,8атм.В начальный момент |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
времени продуктыреакции отсутствовали. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 1 |
31 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
= |
|
|
|
= |
|
|
|
|
51 |
|
= 0,333 |
|
|
|
|||||||||||
= общ |
= |
|
общ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
общ) ( |
общ) |
|
|
|
|
|
|
|
|
общ ∆ |
|
|||||||||||||||||
|
|
|
|
( |
|
|
|
|
|
|
|
|
||||||||||||||||||||
ЗаконДальтона |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
= |
|
|
|
= |
|
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
= |
||||||||||
|
|
|
|
( |
общ) |
( |
общ) |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
= |
общ ∆ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
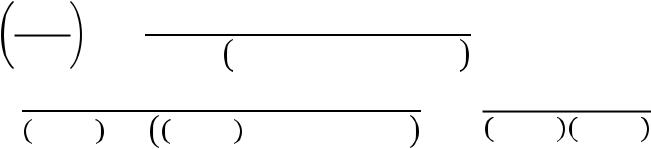
Определитьстепень диссоциацииPCl5 |
в реакцииPCl5(г) → PCl3(г) + Cl2(г), |
если при150°С константа равновесия |
равна 0,333.Давление, которое |
установилосьв системек моментуравновесия (в условии была ошибка,
было указано,что давлениеначальное),составляет 0,8атм.В начальный моментвремени продуктыреакции отсутствовали.
|
|
PCl5(г) → PCl3(г) + Cl2(г) |
|
|
|
|
|
α = nпродукта/n0 |
|
|||||||
исх |
n0 |
|
|
0 |
0 |
|
|
|
|
|
|
|
|
|||
равн |
n |
-n α |
n α |
n α |
|
|
3 2 |
|
|
|
|
|||||
|
|
0 |
0 |
|
0 |
|
0 |
|
|
|
|
|
|
|||
|
= |
|
∑ |
= 5 |
∙ |
5 |
+ 3 |
+ 2 |
|
|
||||||
|
|
|
|
= |
|
|
|
n0 |
α∙ n0α |
|
|
= |
α2 |
|
||
|
|
|
|
|
|
0 |
|
|
|
0 |
0 |
0 |
1 − α 1 + α |
|||
|
|
|
|
|
|
1 − α n ∙ 1 − α n + n α+ n α |
|
|
||||||||
|
|
|
|
|
|
α2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Прирасчете |
|
и констант равновесия учитываютсятолько |
|
||||||||||
|
=2-1=1. |
|
= |
1 − α2 |
|
|
|
|
|
|
|
|
|
|
||
газообразные вещества. |
|
|
|
|
|
|
|
|
|
|||||||
∆ |
|
|
|
|
|
|
∆ |
|
|
|
|
|
|
|
|
|
D=b2-4ac;x= (-b±√D)/2a= 0,54
Ответ: α=0,54.
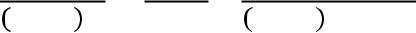
Определитьстепень диссоциацииPCl5 |
в реакцииPCl5(г) → PCl3(г) + Cl2(г), |
|||
если при150°С константа равновесия |
равна 0,333.Давление, которое |
|||
установилосьв системек моментуравновесия, составляет 0,8атм. В |
||||
начальный моментвремени продуктыреакции отсутствовали. |
||||
|
PCl5(г) → PCl3(г) + Cl2(г) |
α = nпродукта/n0 |
||
исх |
P0 |
0 |
0 |
|
равн |
P0-P0α |
P0α |
P0α |
|
Pобщ(равн)= P0-P0α + P0α + P0α = P0 + P0α = P0(1+α) |
|
|
|
||||||||||
P0 |
– начальноедавление |
|
|
|
|
|
|
|
|
|
|||
|
= |
3 2 |
= |
P0 |
α∙ P0α |
= |
|
α2P0 |
= |
α2 общ |
= |
α2 общ |
|
|
5 |
|
0 |
|
1 − α |
1 − α (1 + α) |
1 − |
2 |
|||||
|
|
|
1 − α P |
|
|
|
|
|
|||||
|
|
|
|
|
|
0 |
|
общ |
|
|
|
|
|
|
|
|
|
|
|
= 1 + α |
|
|
|
|
|||
Ответ: α=0,54.
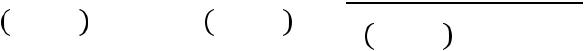
Известна α при некоторых P и T. Найти Кp.
Если в условии не сказано, какое именно давление дано, подразумевается, что дано общее давлениев системе к моменту равновесия.
|
|
2А |
|
|
= |
|
2B + C |
|
|
|
|
|
|
|
|
|
||||||
исх |
|
P0 |
|
|
|
|
|
0 |
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
равн P0-P0α |
(P α) |
P0α |
1/2P0α |
|
|
|
общ |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
∙ |
|
P α |
|
α |
P |
|
|
α |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Баланс по давлению составляется от исходного вещества. |
|
|
||||||||||||||||||||
|
|
|
2 |
|
|
|
0 |
2 |
|
1 |
0 |
|
|
3 |
0 |
|
|
3 |
|
|
|
|
|
= |
|
|
|
|
= |
|
|
|
2 |
|
|
= |
|
|
|
= |
|
|
|
1 |
|
|
2 |
|
|
|
|
0 |
2 |
|
|
2 |
|
2 |
|
|
||||||||
|
|
|
|
|
|
|
2 1 − α |
2 1 − α |
|
) |
||||||||||||
|
|
|
|
|
|
( 1 − α P ) |
|
|
|
|
|
(1 + 2 |
||||||||||
Pобщ = P0-Pα+P0α+1/2P0α = P0 + 1/2P0α= P0(1+1/2α)
P0= Pобщ / (1+1/2α)
|
2А |
= |
B |
исх |
P0 |
|
0 |
равн P0-P0α |
1/2P0α |
||
|
А |
= |
2B |
исх |
P0 |
|
0 |
равн P0-P0α |
2P0α |
||
|
2А |
= |
B |
исх |
P0 |
|
0 |
равн P0-Px |
|
1/2Px |
|
|
А |
= |
2B |
исх |
P0 |
|
0 |
равн P0-Px |
|
2Px |
|

Рассчитатьсреднийтепловойэффектреакции разложения |
|
|||||||||||||||||||
NH4Cl(тв)= NH3(г) |
+ HCl(г), если притемпературе813К давление |
|
||||||||||||||||||
диссоциациисоставляет 0,983атм,а при843К – 1,763атм. |
|
|||||||||||||||||||
Среднийтепловойэффект– тепловойэффект взаданном интервале |
|
|||||||||||||||||||
температур |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
31 1 |
|
|
= |
|
|
1 |
− |
|
|
|
2 |
||||||||
= |
= |
31 |
|
1 |
= |
|
дисс |
∙ |
1 |
дисс |
= 0,2 5( дисс) |
|||||||||
|
4 |
|
1 |
|
|
|
|
2 |
2 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
NH4Cl(тв) |
= |
NH3(г) |
+ |
HCl(г) |
|
|
|
|
|
|
1/2Рдисс |
|
1/2Рдисс |
|
|
||
|
|
0,25∙ |
|
, |
|
|
||
|
|
0,2 5∙ |
|
, |
= , |
|
||
|
|
|
, |
|
|
|
|
|
|
|
∙ |
, |
= |
, |
− |
||
|
|
|
= кДж/моль |
|||||
−

Константа равновесия |
реакции Fe O + CO → 3FeO + CO |
при |
||
600°С равна 1,15. Определите |
конечный3 4 |
состав системы, |
2если |
|
изначально в системе присутствовали 1 моль Fe3O4, 2 моль CO, 0,5 |
|||||||||||||||||||||||||||||||||||||
молей FeO |
и |
|
|
|
0,3 моля CO2 |
|
при |
общем |
|
давлении 5 |
атм. |
||||||||||||||||||||||||||
|
|
= |
|
|
|
= |
2 1 3 |
= |
2 1 |
|
|
|
|
|
|
= 1,15 |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
1 |
3 4 |
|
|
|
2 |
1 |
|
|
|||||||||||||||||||||
|
= общ |
= |
|
|
|
|
|
|
|
|
|
|
|
|
( общ− |
|
) |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
общ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
( |
|
общ) ( |
|
|
общ) |
|
|
|
|
|
|
|
|
|
|
∆ |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
общ |
||||||||||||||||||||||||||
|
= |
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
( |
общ) |
( |
общ) |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
∆ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
∆ |
|
|
|
= |
общ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
∆ |
|
и констант равновесия учитываютсятолько |
|||||||||||||||||||||||
|
=1-1=0.Прирасчете |
|
|
|
|||||||||||||||||||||||||||||||||
газообразные вещества.
Константа равновесия реакции Fe3O4 + CO → 3FeO + CO2 при 600°С равна 1,15. Определите конечный состав системы, если изначально в системе присутствовали 1 моль Fe3O4, 2 моль CO, 0,5 молей FeO и 0,3 моля CO2 при общем давлении 5 атм.
|
Fe3O4 + CO → |
|
исх |
1 |
2 |
равн |
1-x |
2-x |
равн’ |
1-1/3y |
2-1/3y |
0,3+x= 2,3-1,15x 2,15x=2
x=0,93моль
3FeO + |
CO2 |
|
0,5 |
0,3 |
|
0,5+3x |
0,3+x |
|
|
0,3 + |
= 1,15 |
= = 2 − |
||
0,5+y |
0,3+1/3y |
|
Ответ: 0,07мольFe3O4; 1,07моль CO;3,29мольFeO; 1,23моль CO2.
