- •Семинары по физической химии 1 часть
- •Физическая химия
- •Теория
- •Задачи
- •Второй закон термодинамики
- •Объединенное выражение I и II начал термодинамики. Зависимость энтропии от параметров состояния
- •Типы задач
- •Рассчитайте изменение энтропии при изобарном нагревании 1 моль хлора от температуры 300 до 500 К. Воспользуйтесь справочными данными о зависимости теплоемкости хлора от температуры.
- •Рассчитайте изменение энтропии в реакции синтеза аммиака при температуре 598 К и давлении 1 атм.
- •Энергия Гиббса. Энергия Гельмгольца.
- •Типы задач
- •Рассчитайте изменение энергии Гиббса, если в результате расширения 20 кг гелия при 298 К объем газа увеличился в 1 000 раз. Газ считать идеальным.
- •Рассчитайте изменение энергии Гельмгольца, если в результате сжатия 500 моль кислорода при 400 К давление газа увеличилось в 100 раз. Газ считать идеальным.
- •Расчет изменения энергии Гиббса при смешении идеальных газов
- •54 г воды испаряются при 373 К и давлении 1 атм, а затем изотермически расширяются до давления 0,1 атм. Рассчитайте общее изменение энергии Гиббса и энергии Гельмгольца.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Уравнение Гиббса-Гельмгольца
- •Химическое равновесие
- •Влияние общего давления и добавления инертного газа на смещение равновесия
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изобары Вант-Гоффа
- •Методы расчета константы равновесия
- •Фазовое равновесие в однокомпонентных системах
- •Фазовое равновесие в однокомпонентных системах
- •Уравнение Клапейрона
- •Уравнение Клапейрона-Клаузиуса
- •Парциальные мольные величины
- •Методы определения парциальных молярных величин
- •Коллигативные свойства
- •Фазовая диаграмма для растворителя и раствора
- •Основные формулы
- •Основные формулы
- •В 1000 г воды растворили 0,0684 кг сахарозы (M = 342 г/моль). Удельная теплота испарения воды 2256,7 кДж/кг. Рассчитать давление пара над раствором при 500С и температуру кипения раствора. Воспользоваться справочными данными.
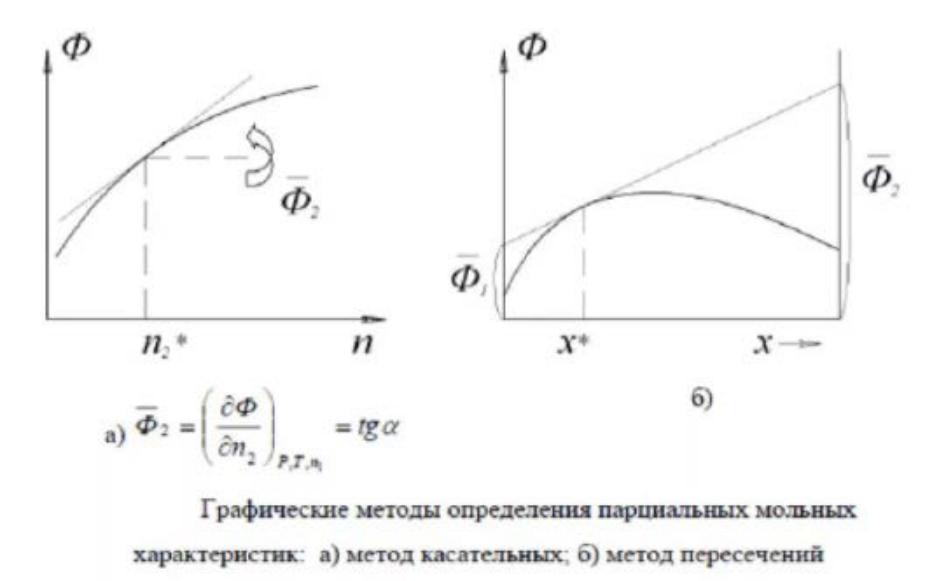
Методы определения парциальных молярных величин

Для водного раствораMgSO4 |
зависимостьобъемаотконцентрации |
||||||||||||
выражается уравнением: V = 1001,21+ 34,69(m- 0,07)2 |
(V,см3) |
||||||||||||
Рассчитатьпарциальный мольный объемводы и MgSO4 |
в растворе, |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
приготовленномрастворением9 г солии1,5кг воды. |
|
||||||||||||
|
|
= |
|
|
, ,≠ |
|
|
|
|||||
|
2 |
= |
|
|
, , ≠ |
|
|
|
|||||
|
|
|
|
− 0,07 |
|||||||||
2 = 2 ∙34,69∙ |
− 0,07 |
= 69,38∙ |
|||||||||||
|
|
2 |
|
|
|
|
22 |
|
2 ∙1000 |
||||
Моляльность m показывает мольное содержание растворенного |
|||||||||||||
вещества в 1 кг растворителя. |
|
= |
|
|
= |
|
|
|
|
||||
= |
|
|
|
|
|
|
|
1 |
2 |
|
|||
|
|
|
2 |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
1000 г |
|
1000 |
|
|
|
∙ |
|
|||||
|
|
= |
9 ∙ 1000 |
|
|
|
|
|
|||||
|
1500 ∙12 0 = 0,05 |
|
|
||||||||||

Для водного раствораMgSO4зависимостьобъемаотконцентрации |
|||||||||||
выражается уравнением: V = 1001,21+ 34,69(m- 0,07)2 |
(V,см3) |
||||||||||
Рассчитатьпарциальный мольный объемводы и MgSO4 в растворе, |
|||||||||||
2 |
= 69,38∙ |
|
|
0,05 − 0,07 = −1,39 |
см3 |
||||||
приготовленномрастворением9 г солии1,5кг воды. |
моль |
||||||||||
|
|
|
|
= 1 1 |
+ 2 2 |
||||||
|
|
|
|
= 1 1 |
+ 2 2 |
|
|||||
V = 1001,21 + 34,69(m= |
|
− 2 2 |
= |
− 2 |
|
|
|||||
|
|
1 |
|
1 |
|
||||||
1001,22 см3 |
|
1 |
|
|
|
|
|
|
|||
|
|
- 0,07)2 = 1001,21 + 34,69(0,05 - 0,07)2 = |
|||||||||
1 |
= |
1001,22+ 0,05 ∙ 1,39 |
= 18,05 |
см3 |
|||||||
|
|
1000 |
|
|
моль |
||||||
|
|
|
|
|
18 |
|
|
|
|
||
Задачи из раздаточногоматериала
•Задача на функцию смешенияидеального раствора
•Задача на закон Дальтона
•Задача на расчет активности и коэффициентовактивности неидеальных растворов