- •Семинары по физической химии 1 часть
- •Физическая химия
- •Теория
- •Задачи
- •Второй закон термодинамики
- •Объединенное выражение I и II начал термодинамики. Зависимость энтропии от параметров состояния
- •Типы задач
- •Рассчитайте изменение энтропии при изобарном нагревании 1 моль хлора от температуры 300 до 500 К. Воспользуйтесь справочными данными о зависимости теплоемкости хлора от температуры.
- •Рассчитайте изменение энтропии в реакции синтеза аммиака при температуре 598 К и давлении 1 атм.
- •Энергия Гиббса. Энергия Гельмгольца.
- •Типы задач
- •Рассчитайте изменение энергии Гиббса, если в результате расширения 20 кг гелия при 298 К объем газа увеличился в 1 000 раз. Газ считать идеальным.
- •Рассчитайте изменение энергии Гельмгольца, если в результате сжатия 500 моль кислорода при 400 К давление газа увеличилось в 100 раз. Газ считать идеальным.
- •Расчет изменения энергии Гиббса при смешении идеальных газов
- •54 г воды испаряются при 373 К и давлении 1 атм, а затем изотермически расширяются до давления 0,1 атм. Рассчитайте общее изменение энергии Гиббса и энергии Гельмгольца.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Уравнение Гиббса-Гельмгольца
- •Химическое равновесие
- •Влияние общего давления и добавления инертного газа на смещение равновесия
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изобары Вант-Гоффа
- •Методы расчета константы равновесия
- •Фазовое равновесие в однокомпонентных системах
- •Фазовое равновесие в однокомпонентных системах
- •Уравнение Клапейрона
- •Уравнение Клапейрона-Клаузиуса
- •Парциальные мольные величины
- •Методы определения парциальных молярных величин
- •Коллигативные свойства
- •Фазовая диаграмма для растворителя и раствора
- •Основные формулы
- •Основные формулы
- •В 1000 г воды растворили 0,0684 кг сахарозы (M = 342 г/моль). Удельная теплота испарения воды 2256,7 кДж/кг. Рассчитать давление пара над раствором при 500С и температуру кипения раствора. Воспользоваться справочными данными.

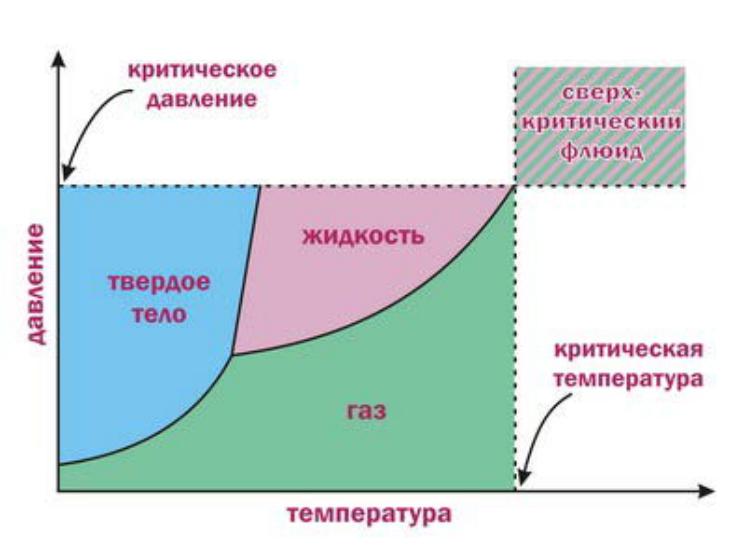
Фазовое равновесие в однокомпонентных системах
Диаграмма фазовогоравновесия однокомпонентной системы (диаграммасостояния):
Неверно изображать сильный наклонлинии плавления

Фазовое равновесие в однокомпонентных системах
Тпл увеличивается с увеличением |
Тпл уменьшается с увеличением |
|
давления(H2O, Ga, Bi); ΔVпл < 0;Vж < Vтв; |
||
давления(CO2); ΔVпл > 0;Vж > Vтв; ρж < ρтв |
||
ρж > ρтв |
||
Правилофаз Гиббса: f = k – ф + 2 |
||

Уравнение Клапейрона∆
= ∆ фп
фп
- уравнение Клапейрона– длявсех фазовых переходов. = ∆∆пл
пл
– для плавления. |
|
= |
∆ пл |
||
ΔVпл = Vж – Vтв |
|||||
|
|
∆ пл |
|||
|
|
|
|
|
|
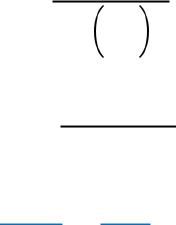
Уравнение Клапейрона-Клаузиуса
= ∆фп∆ фп
Допущения: |
|
|
|
|
|
|
|
|
|
|
|
|
|
• при температурах далеких от критических Т<< Т |
V >> V |
|
, поэтому |
||||||||||
можно считать, что ΔV = (V |
пар |
- V |
конд. фазы |
) ≈ V |
пар |
кр |
пар |
конд. фазы |
|
||||
• при Т<< Ткр поведение пара не отличается от свойств идеального газа. Тогда |
|||||||||||||
для1 моль газа |
пар = |
|
|
|
∆исп/субл |
|
|
|
|
||||
|
. Подставляемобъем пара в уравнение Клапейрона. |
||||||||||||
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
∆исп/субл |
|
|
|
|
|||
|
|
|
= |
|
|
2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
и сублимации. |
|
|
|
|
|
|
|
|
|
|
|
|
|
- уравнение Клапейрона-Клаузиуса |
используется дляпроцессов парообразования |
||||||||||||
|
|
= |
|
|
|
|
|
||||||

Зависимостьтемпературыплавления калия отдавления выражается уравнением: T = 335,65+ 1,56·10-2P– 6,8·10-7P2 (P, атм).Определить
теплотуплавления придавлении 100атм, если температураплавления |
||||||||||||
|
|
|
|
|
|
∆ пл |
|
|
|
|
|
|
равна 337,2К иизменение объемаприплавлениисоставляет 0,0265см3/г. |
||||||||||||
ΔVпл = Vж – Vтв |
|
|
|
= |
|
∆ пл |
|
|
|
|
|
|
|
|
|
|
= |
|
∆ пл |
|
|
|
|
|
|
|
dT |
|
|
∆ пл |
|
−7 |
|
|
|
|||
|
= 1 ,56·1 0 |
−2 |
|
|
P |
|
|
|||||
При р = 100атм |
dp |
|
|
– 1 3,6·10 |
|
град |
||||||
dT = 1 ,56·1 0−2 – 1 3,6·10−7·100=0,015 |
град |
= 0,015·10−5 |
||||||||||
dp |
|
|
∆пл= |
∆пл |
|
атм |
|
|
Па |
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
Дж |
|
|
∆Hпл= |
337,2 · 0,02 65 · 10−6 |
= 59,6 |
|
||||||||
|
|
0,015·10−5 |
|
г |
|
|||||||

Теплота плавления бензола притемпературе5,6°С и давлении 1атм
составляет 128Дж/г.Изменение объемаприплавлении составляет 1,3·10-2 |
||||||||||||||||
|
|
|
|
|
|
∆пл |
|
|
|
|
|
|
|
|||
см3/г.Определитьтемпературуплавления придавлении 100атм. |
|
|
|
|||||||||||||
|
|
|
|
= ∆ пл |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
∆ пл |
|
|
|
|
|
|
|
||
|
|
|
|
= |
|
∆ пл |
|
|
|
|
|
|
|
|||
|
|
|
2 − 1 |
|
∆ пл |
|
|
|
|
|
|
|
||||
dp |
∆Hпл |
|
= |
∆ пл |
( 2 − 1) |
7 |
Па |
|
|
атм |
||||||
|
12 8 |
|
|
7 |
Па |
= 350 |
|
|||||||||
dT = |
T∆Vпл = 2 78,6∙ |
1,3·10−2·10−6 |
= 3,5 · 10 |
К = 3,5 · 10 |
°С |
|
или К |
|||||||||
|
|
|
|
|
|
|
|
|
°С |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
2 = 2 78,6 + |
2 = 1 + ( 2 − 1) |
= 2 78,87 К |
|
|
|
|||||||||
|
|
1 |
7 |
100 − 1 |
· 105 |
|
|
|
||||||||
|
|
|
|
3,5 · 10 |
|
|
|
|
|
|
|
|
|
|
|
|

Зависимость давленияпара длятвердого и жидкого вещества от температуры выражается следующим образом:
|
тв = 10,648 − |
2 559,5 |
|
( , мм рт. ст. ) |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1511,3 |
|
|
|
|
|
|
|
|
|
|
|||||
|
координаты тройной точки и теплоту плавления в тройной точке. |
||||||||||||||||||
Определить |
ж |
= 7,540 − |
|
|
|
|
|
|
|
( , мм рт. ст. ) |
|
|
|||||||
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
В тройнойточке линии |
возгонки( |
|
|
|
|
) и испарения( |
|
|
) пересекаются. |
||||||||||
= − |
|
|
+ |
|
ж |
|
|
||||||||||||
|
|
|
|
|
тв |
|
|
|
|
|
|
|
|
|
|||||
|
10,648 − |
2 559,5 |
= 7,540 − |
1511,3 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= 337,3 ; |
= 1148 мм рт. ст. |
|
|
|
|
|||||||||||||
|
|
= − |
|
|
|
|
+ |
|
|
|
|
|
|||||||
|
|
2,3 |
|
|
∆возг> ∆исп> ∆пл |
||||||||||||||
|
|
∆возг= ∆пл + ∆исп |
|
|
|||||||||||||||
|
|
∆пл= ∆возг − ∆исп |
|
|
|
|
кДж |
||||||||||||
∆пл= 2,3 · 8,31 · 2 559,5 − 2,3 · 8,31 · 1511,3 = 2 0,04 |
моль |
||||||||||||||||||
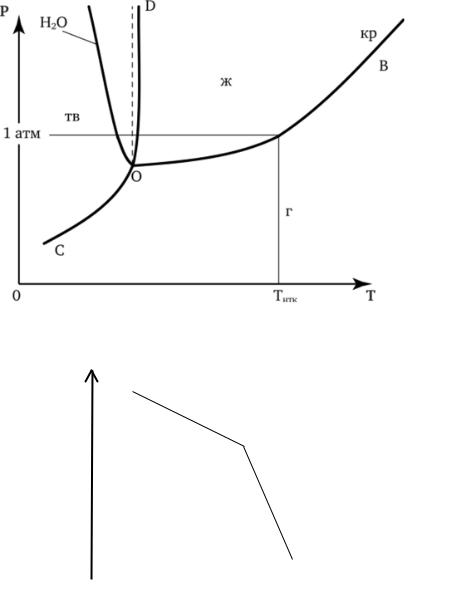
Определение координат тройнойточки
lnp |
H>0 |
Hисп = - Rtgα |
|
Hсубл = - Rtgβ
 1/Т
1/Т
Н |
|
температуру кипения ацетона при давлении 0,6 атм, если температура |
|||||||||||||||||||
нормального кипения (Т |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
айти |
|
|
|
|
нтк) равна 56,2 °С, используя справочные данные (табл. 24). |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
= |
|
исп |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
= |
|
|
|
|
− |
|
|
|||||
|
Температура |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
нормальногокипения- температура,прикоторой |
|||||||||||||||||
|
давление насыщенного пара жидкостистановится равным 1 атм. |
||||||||||||||||||||
|
1 атм= 760ммрт. ст. |
исп |
|
|
1 |
|
|
|
|
|
|
1 |
|||||||||
|
|
|
|
760 |
= |
|
|
|
|
|
|
|
|
||||||||
|
0,6атм= ? |
400 |
8,31 |
|
(39,5 + 2 73) − |
(56,2 + 2 73) |
|||||||||||||||
|
|
|
|
|
|
|
|
исп = 32,87 |
кДж |
|
|||||||||||
|
|
|
|
|
|
760 |
моль |
|
|||||||||||||
|
|
|
|
|
= |
32 870 |
1 |
|
− |
|
|
|
1 |
|
|||||||
|
|
|
|
456 |
|
8,31 |
|
3 |
|
|
°С |
|
|||||||||
|
|
|
|
|
|
3 |
|
|
(56,2 + 2 73) |
||||||||||||
|
|
|
|
|
|
|
|
= 31 5,8 К = 42,8 |
|
|
|||||||||||
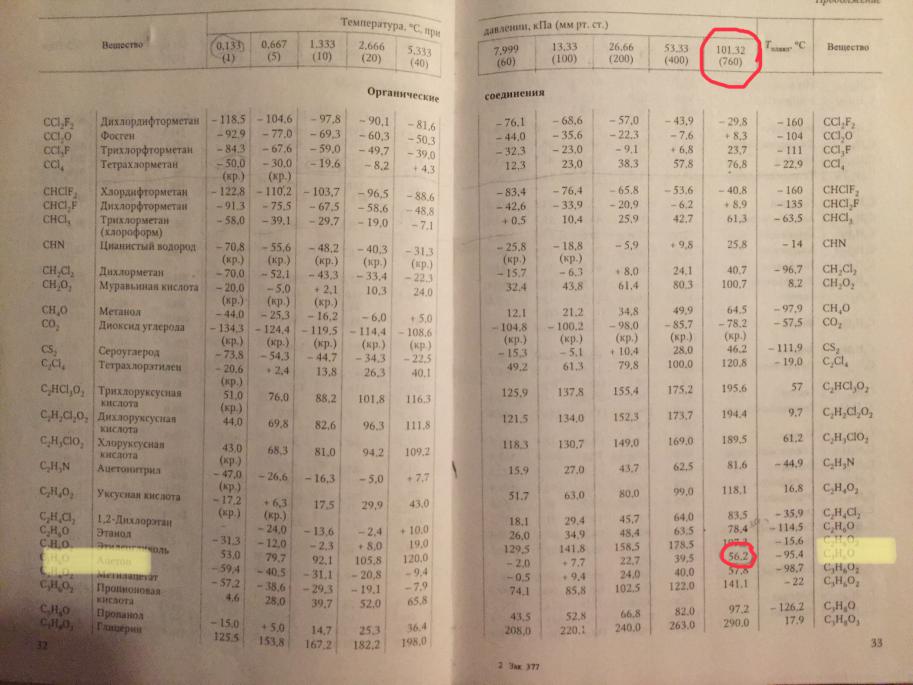
Температурывозгонкиили кипения придавлении ≤1атм

Аналитический расчет истинного теплового
Истинныйтепловойэффектэ фекта– тепловойэффектпри однойконкретнойтемпературе. Аналитически определяетсяпо справочнойзависимости =
( ). = исп,возг °
1)Перевести“lg” в “ln” путемдомножения каждогослагаемогона коэффициент 2,3(ln10 =2,3;lg10=1).Если слагаемое содержит“lg”, то коэффициент перед “lg” не меняется; меняется только логарифмс
“lg”на “ln”. = ( )′
2)Взятьпроизводнуюlnpпотемпературе( )
3)Умножитьполученную зависимостьна RT2
4) Подставитьзаданнуютемпературу

Зависимость давлениянасыщенного пара от температуры дляжидкого фриона |
||||||||||||||||
Рассчитать |
|
= 34,5 − |
2 406,1 |
− 9,2 6 + 0,0037T (p, Па) |
|
|||||||||||
имеет вид: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
истинный тепловой эффектиспарения, энтропию испарения и |
|
||||||||||||||
изменение внутренней энергии испарения при температуре 298 К. |
|
|||||||||||||||
|
|
|
= 2,3∙34,5 − |
2,3∙ |
2 406,1 |
− , + 2,3∙ 0,0037T |
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
= 79,35 − |
5534,03 |
− 9,2 6 + 0,00851 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||
′ |
|
5534,03 |
|
исп ° = ∙ |
= ∙ ( )′ |
|
||||||||||
|
|
9,2 6 |
|
|
|
|
|
|
|
|
||||||
( ) |
= |
2 |
|
− |
|
+ 0,00851 |
|
|
|
|
||||||
исп ° = |
2 |
∙ |
5534,03 |
− |
9,2 6 |
+ 0,00851 = 5534,03 − 9,2 6 + 0,00851 |
2 |
|||||||||
|
|
2 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
исп °2 98 = 2 9,35 кДж/моль |
|
|||||||

Зависимость давлениянасыщенного пара от температуры дляжидкого фриона |
||||||||
Рассчитать |
= 34,5 − |
2 406,1 |
− 9,2 6 + 0,0037T (p, Па) |
|||||
имеет вид: |
|
|
|
|
|
|
|
|
|
истинный тепловой эффект испарения и энтропиюиспаренияи |
|||||||
изменениевнутреннейэнергиииспарения при температуре 298 К. |
||||||||
|
|
|
∆исп= |
∆ исп |
|
|||
|
|
|
|
Дж |
||||
|
∆исп= |
2 9 350 |
= 98,5 |
|||||
|
|
2 98 |
моль · К |
|||||
|
∆исп= ∆исп − |
|
на 1 моль вещества , Δνисп = 1 |
|||||
|
∆исп= 2 9 350 − 8,31 · 2 98 = 2 6,9 кДж/моль |
|||||||
|
|
∆конд= −∆исп |
||||||
|
|
∆конд= −∆исп |
||||||
|
|
∆конд= −∆исп |
||||||

|
Аналитический расчет истинного теплового |
|||||||||
|
эффекта |
|
|
|
|
|
||||
Аналитическиопределяетсяпосправочнойзависимости = ( ). |
||||||||||
|
|
= |
исп,возг |
° |
|
|
|
|||
|
|
|
|
|
|
|
|
|||
|
|
исп,возг |
° · |
|
|
|
||||
|
= |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
1) |
Взятьпроизводнуюpпо |
|
|
|
′ |
|
|
|||
|
исптемпературе,возг ° = |
( |
· |
|
|
|
|
) |
||
2) |
|
|
|
|
||||||
Рассчитатьзначение давления, подставив= ( ) |
|
|||||||||
|
зависимостьp=f(T) |
|
|
|
|
|
заданную температурув |
|||
|
|
|
|
|
|
|
|
|
|
|
3) |
Умножитьполученную зависимостьна RT2 и разделить на p |
|||||||||
4) |
Подставитьзаданнуютемпературу |
|
|
|
|
|
|
|
||
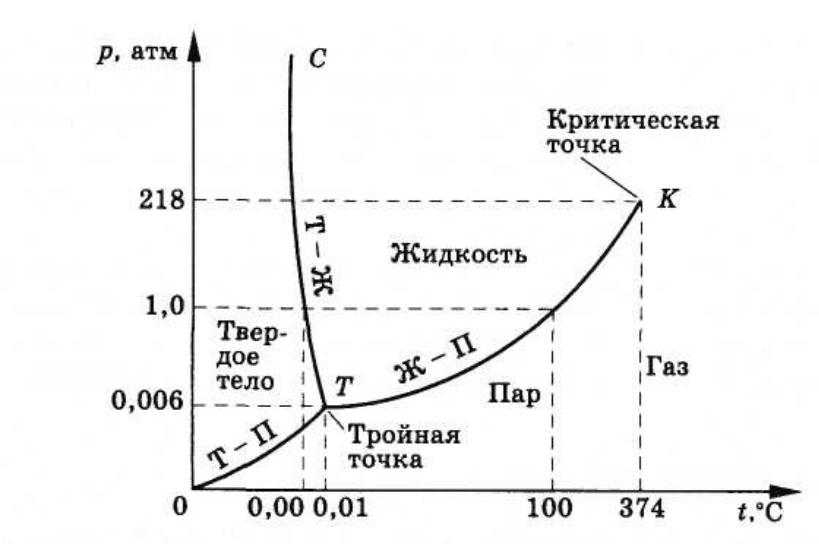
Фазоваядиаграммаводы
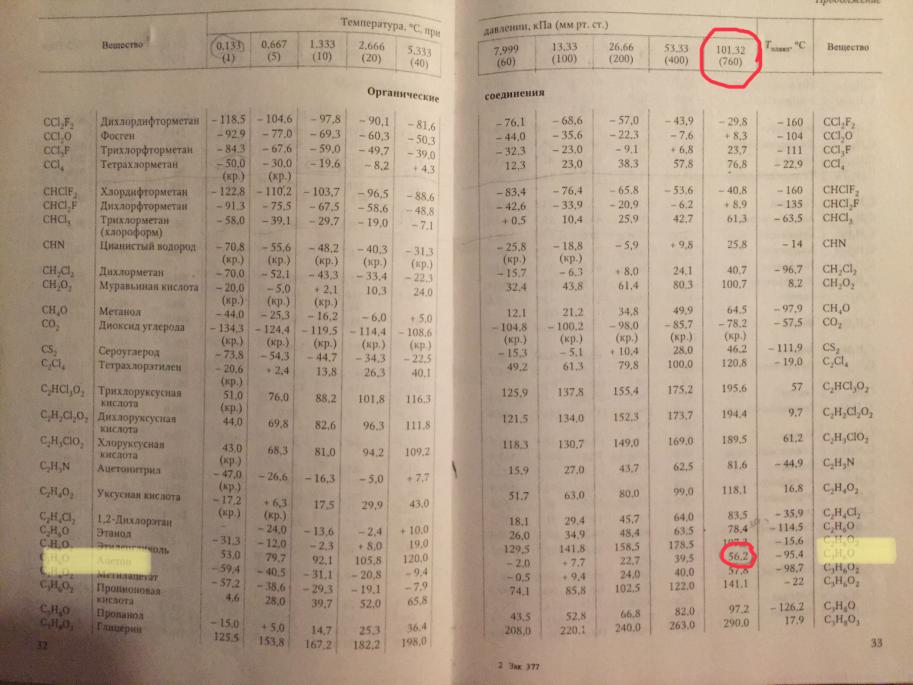
Температурывозгонкиили кипения придавлении ≤1атм