- •Семинары по физической химии 1 часть
- •Физическая химия
- •Теория
- •Задачи
- •Второй закон термодинамики
- •Объединенное выражение I и II начал термодинамики. Зависимость энтропии от параметров состояния
- •Типы задач
- •Рассчитайте изменение энтропии при изобарном нагревании 1 моль хлора от температуры 300 до 500 К. Воспользуйтесь справочными данными о зависимости теплоемкости хлора от температуры.
- •Рассчитайте изменение энтропии в реакции синтеза аммиака при температуре 598 К и давлении 1 атм.
- •Энергия Гиббса. Энергия Гельмгольца.
- •Типы задач
- •Рассчитайте изменение энергии Гиббса, если в результате расширения 20 кг гелия при 298 К объем газа увеличился в 1 000 раз. Газ считать идеальным.
- •Рассчитайте изменение энергии Гельмгольца, если в результате сжатия 500 моль кислорода при 400 К давление газа увеличилось в 100 раз. Газ считать идеальным.
- •Расчет изменения энергии Гиббса при смешении идеальных газов
- •54 г воды испаряются при 373 К и давлении 1 атм, а затем изотермически расширяются до давления 0,1 атм. Рассчитайте общее изменение энергии Гиббса и энергии Гельмгольца.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Рассчитайте изменение энергии Гиббса и энергии Гельмгольца при стандартных условиях и температуре 400 К для реакции H2 + 1/2O2 = H2O(ж), считая температурный коэффициент энергии Гиббса величиной постоянной. Воспользуйтесь справочными данными.
- •Уравнение Гиббса-Гельмгольца
- •Химическое равновесие
- •Влияние общего давления и добавления инертного газа на смещение равновесия
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изотермы Вант-Гоффа
- •Уравнение изобары Вант-Гоффа
- •Методы расчета константы равновесия
- •Фазовое равновесие в однокомпонентных системах
- •Фазовое равновесие в однокомпонентных системах
- •Уравнение Клапейрона
- •Уравнение Клапейрона-Клаузиуса
- •Парциальные мольные величины
- •Методы определения парциальных молярных величин
- •Коллигативные свойства
- •Фазовая диаграмма для растворителя и раствора
- •Основные формулы
- •Основные формулы
- •В 1000 г воды растворили 0,0684 кг сахарозы (M = 342 г/моль). Удельная теплота испарения воды 2256,7 кДж/кг. Рассчитать давление пара над раствором при 500С и температуру кипения раствора. Воспользоваться справочными данными.
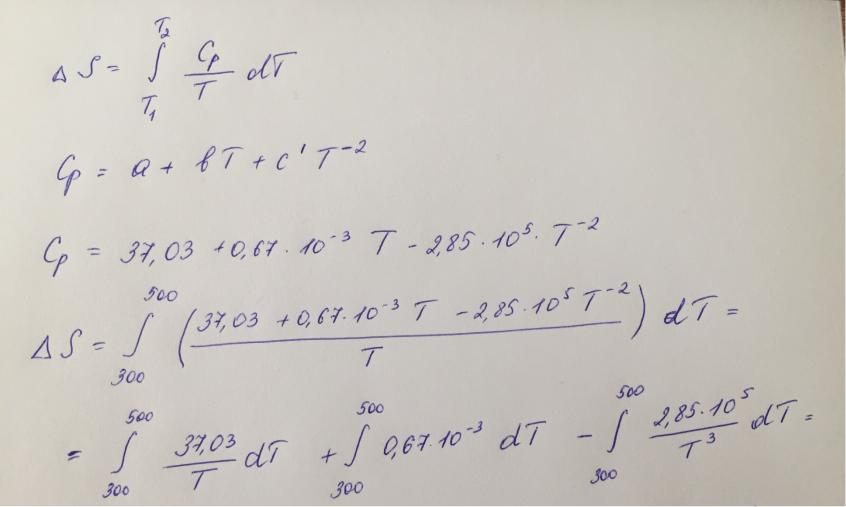
Рассчитайте изменение энтропии при изобарном нагревании 1 моль хлора от температуры 300 до 500 К. Воспользуйтесь справочными данными о зависимости теплоемкости хлора от температуры.
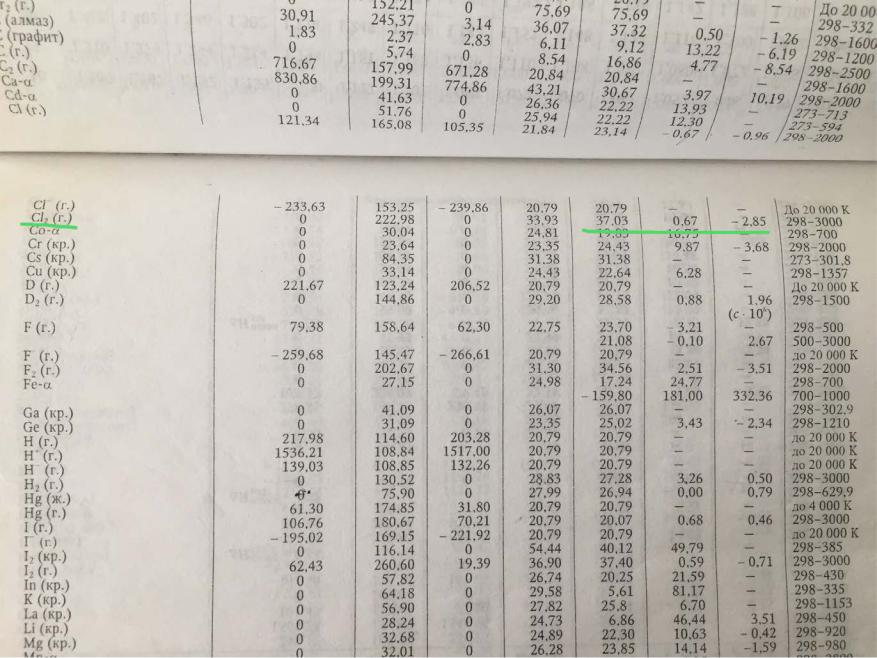


Рассчитайте изменение энтропии при смешении 100 см3 аргона и 400 см3 окиси углерода при температуре 293К и давлении 1 атм. Газы считать идеальными.
Процесс смешения газов необратим. Поэтому общее изменение энтропии при смешении газов можно заменить суммой изменения энтропий за счет расширения каждого из газов.
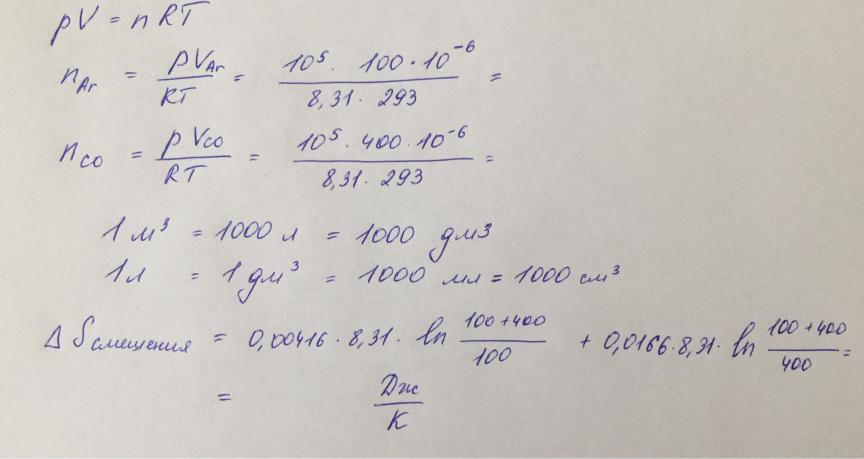

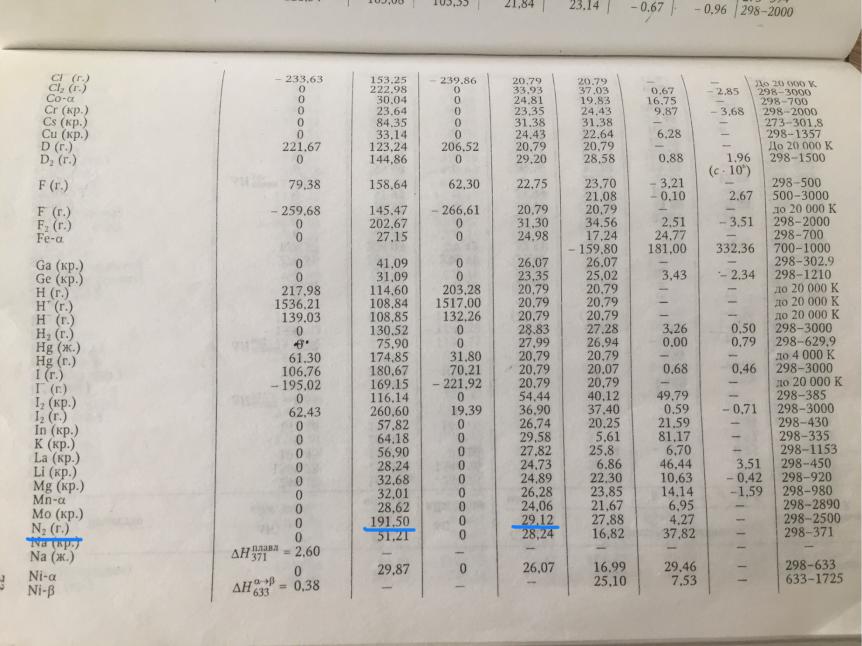
Рассчитайте абсолютную энтропию 1,5 моль азота при
температуре 600 К и давлении 10-6 атм. Газ считать идеальным. |
|||||||
Считать теплоемкость газообразного азота независящей от |
|||||||
|
= |
|
|
|
|
|
|
температуры. |
|
− |
|||||
° |
° |
|
|
|
° |
|
|
= 298 |
+ 298 |
|
|
− 1 |
|||

Рассчитайте абсолютную энтропию 180 г водяного пара при
температуре 500 К и давлении 1 атм. Газ считать идеальным. |
||||||||||||||||||||
Считать теплоемкость газообразной воды независящей от |
|
|||||||||||||||||||
температуры, а теплоемкость жидкой воды зависящей от |
|
|||||||||||||||||||
температуры. |
|
|
|
пл |
|
|
кип ж |
|
|
|
исп |
|
|
|
г |
|
||||
|
пл тв |
|
|
|
|
|
|
|
|
|
|
|
||||||||
= |
|
|
+ |
∆ |
+ |
|
|
|
+ |
∆ |
+ |
|
|
|
||||||
0 |
|
|
пл |
|
пл |
|
|
кип |
|
кип |
|
|||||||||
|
|
|
|
|
|
|
ф.п. = |
∆ ф.п. |
|
|
|
|
|
|
|
|
||||
|
|
|
° |
|
|
кип |
ф.п. |
исп |
|
|
г |
|
|
|
|
|||||
|
|
|
|
|
ж |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
= 298 |
+ |
|
|
+ |
∆ |
+ |
|
|
|
|
|
|||||||
|
|
|
|
|
2 98 |
|
|
|
кип |
|
кип |
|
|
|
|
|||||