
- •Часть II рабочая тетрадь
- •Введение
- •1.1. Строение атома и периодическая система
- •1. 2. Химическая связь
- •2.1. Основы химической термодинамики
- •2.2. Химическая кинетика
- •Зависимость скорости реакции от температуры
- •2.3. Химическое равновесие
- •И стехиометрические расчёты
- •Характерные реакции оснóвных оксидов
- •4.1. Общие свойства растворов
- •4.2. Равновесия в растворах электролитов
- •Ионно-молекулярные реакции в растворах электролитов
- •Методы определения рН растворов
- •Гидролиз солей
- •5.1. Окислительно-восстановительные процессы
- •5.3. Электролиз
- •5.4. Коррозия металлов
- •Защитные покрытия
- •Электрохимические методы
- •6.1. Качественный химический анализ
- •6.2. Количественный химический анализ
- •6.3. Физико-химические и физические методы анализа
- •7.1. Общие сведения и методы получения полимеров
- •7.3. Природные полимеры
- •Библиографический список
- •Заключение
Зависимость скорости реакции от температуры
Температура опыта, оС |
Время помутнения, с |
Относительная скорость реакции, υ=1:τ, с-1 |
Температурный коэффициент скорости реакции, γ |
|
теоретический |
экспериментальный |
|||
Т1 = |
τ 1 = |
υТ1 = |
1,80 |
|
Т2 = |
τ 2 = |
υТ2= |
||
Рассчитаете относительную скорость реакции при температуре Т1 (υТ1) и Т2 (υТ2), температурный коэффициент «γ» (формула 2.5) и заполните таблицу 2.2.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Что характеризует «γ»? Сравнив экспериментальное значение температурного коэффициента с теоретическим значением, оцените точность эксперимента.
________________________________________________________________________________________________________________________________________________________________
Пример 2.6. Температурный коэффициент реакции равен 3. При охлаждении сис-
темы от 500 С до300 скорость химической реакции … 1) уменьшится в 9 раз 2) увеличится в 9 раз 3) уменьшится в 6 раз 4) не изменится
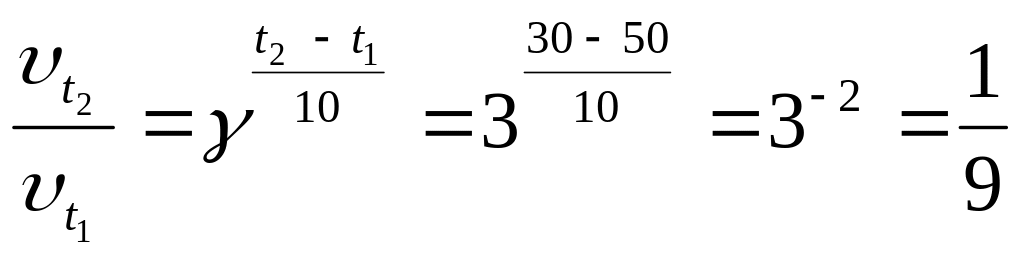 .
Правильный ответ: уменьшится в 9 раз.
.
Правильный ответ: уменьшится в 9 раз.
Пример 2.7. Образец СаСО3 растворяется в соляной кислоте при 20 0С в течение 6 минут, при 40 0С – за 40 секунд. Температурный коэффициент реакции равен …
1) 2 2) 2,5 3) 3 4) 4
6 минут составляет 360 секунд. Температура увеличилась на 20 0С, скорость увеличилась в (360 : 40) = 9 раз. При изменении температуры на 10 0С скорость увеличится в три раза, т.е. температурный коэффициент равен трём.
Упражнение 2.10. Если температурный коэффициент реакции карбоната магния с кислотой равен 3 и при температуре 25 оС она заканчивается за 36 минут, то при температуре 45 оС время завершения будет равно _______ минут(ы).
1) 3 2) 4 3) 6 4) 8
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ТИПОВЫЕ КОНТРОЛЬНЫЕ УПРАЖНЕНИЯ
1. Основные факторы, от которых зависит скорость химических реакций:
1) природа реагирующих веществ и температура
2) в растворах: природа и концентрация реагирующих веществ, температура, присутствие катализатора
3) в газообразной системе: парциальные давления участников реакции, температура, присутствие катализатора 4) концентрация реагирующих веществ и температура.
Укажите ответ, наиболее полно отвечающий на поставленный вопрос.
2. Если увеличить давление в 10 раз, то скорость прямой реакции
H2 (газ) + Br2 (газ)↔2 HBr (г),
при условии ее элементарности, увеличится в ____ раз. 1) 50 2) 100 3) 20 4) 5
3. Если скорость реакции увеличилась в 8 раз при повышении температуры на 30 0С, то температурный коэффициент скорости равен ….. 1) 9 2) 3 3) 2 4) 8
