
- •Лекция 1
- •Лекция 2
- •Лекция 3 Временная организация клетки. Клеточный цикл, его периодизация. Митотический цикл. Репликация днк. Митоз. Механизм регуляции митотической активности.
- •Лекция 4
- •Лекция 5 Законы наследственности г. Менделя
- •Лекция 6
- •Лекция 7
- •Лекция 8
- •Лекция 9
- •Лекция 10
- •Лекция 11
- •Лекция 12
- •Лекция 13
- •Лекция 14
- •Лекция 15
- •Лекция 16
- •Лекция 17
- •Лекция 18
Лекция 17
Постэмбриональный онтогенез, его периодизация. Рост и конституция человека. Биологические аспекты старения.
После выхода организма из яйцевых оболочек или из утробы матери начинается постэмбриональный период развития (постэмбриональный онтогенез). Это период с момента появления на свет до естественной гибели организма. В постэмбриональном развитии в зависимости от способности к размножению выделяют три периода:
Дорепродуктивный период (особи не способны к размножению).
Репродуктивный период (особь осуществляет функцию размножения).
Пострепродуктивный период (характеризуется ослаблением или полным прекращением участия в размножении).
Интересным и важным с точки зрения биологии и медицины является дорепродуктивный период развития. Этому периоду характерен еще не закончившийся до конца при эмбриональном развитии морфогенез. Начинают функционировать после рождения пищеварительная система, система дыхания, органы чувств. В этот период происходят выраженные структурные и функциональные преобразования. Важнейшей особенностью дорепродуктивного периода является рост организма. Рост определяет размеры, пропорции тела, размеры внутренних органов. Рост происходит на клеточном, тканевом, органном и организменном уровнях. Для человека, как и многих животных, характерен аллометрический рост. Такой рост связан с определенным этапом онтогенеза и получил называние также ограниченный рост. Но существуют организмы (рыбы, например), которые растут на протяжении всего онтогенеза, вплоть до смерти. Этот тип роста получил название неограниченный рост.
В основе роста организма лежат три механизма: 1) увеличение числа клеток (пролиферация); 2) увеличение клеток в размерах; 3) увеличение объема и массы внеклеточного вещества. С пролиферацией клеток связан как рост отдельных органов, так и организма в целом. На определенных этапах имеет значение увеличение клеток в размерах за счет увеличения объема цитоплазмы, количества органелл. Примером увеличения межклеточного вещества является рост кости, где основная масса ткани приходится на межклеточную часть.
У человека наиболее явным является рост за счет увеличения продольных размеров тела. Это происходит в основном за счет линейного роста длинных трубчатых костей. На этапе эмбрионального развития первоначально длинная трубчатая кость представляет собой скопление хрящевой ткани с ядром окостенения по средине (диафиз) и распространением хрящевых клеток на концах (эпифизах). Образование новых клеток в области эпифизарных хрящей, их превращение в костные клетки и определяет линейный рост костей, а значит и рост человека. Окончательное окостенение у каждой кости происходит в определенные сроки и заканчивается обычно к 18-20 годам у мужчин и 16-18 годам у женщин. У человека эпифизарные хрящи длинных трубчатых костей окостеневают полностью и поэтому рост конечностей невозможен. Рост же позвоночного столба продолжается и в возрасте 20-30 лет за счет отложения новых слоев костного вещества на верхних и нижних поверхностях позвонков. Поэтому длина тела за эти годы увеличивается в среднем на 3-5 см. Между 30 и 40-50 годами длина тела остается постоянной, а затем начинает уменьшаться. Таким образом, рост организма на протяжении жизни происходит не равномерно. Рост человека, как и других организмов с определенным типом роста, описывается S-образной кривой (рис. 1). В эмбриональный период скорость роста высокая. После рождения скорость роста ребенка постепенно снижается. Это снижение прерывается в возрасте 12-14 лет, который соответствует периоду полового созревания (пубертатному периоду). В этот период резко возрастает скорость роста, происходит своеобразный скачок роста. В дальнейшем происходит опять снижение скорости роста и в конечном итоге рост человека прекращается. Кривые роста большинства скелетных и мышечных органов примерно повторяют ход общей кривой роста тела. Тоже самое можно сказать о размере отдельных органов – печени, селезенки, почек. Однако существует целый ряд тканей и органов, кривые роста которых существенно отличаются. К ним относятся мозг, череп, органы размножения, лимфатическая ткань и подкожная жировая клетчатка. Мозг, например, развивается раньше любой другой части тела. У новорожденных мозг составляет 25% своего дефинитивного (окончательного) веса, у 5-летнего ребенка – 90%, у 10-летнего -95%. Относительная масса вилочковой железы (тимуса) достигает максимума в возрасте 10-12 лет (относительно массы тела), а абсолютный рост железы достигает своего максимума к 30 годам. После этого начинается возрастная инволюция тимуса, которая выражается в его постепенной атрофии (уменьшение массы).
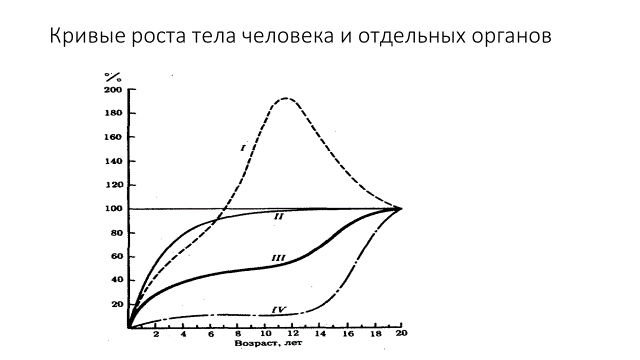
Рис. 1. Кривые роста (ІІІ – кривая роста тела в целом; ІІ – кривая роста мозга; І – кривая роста тимуса; IV – кривая роста органов размножения)
Процессы роста, как и всего индивидуального развития, подвергаются генетическому контролю. Рост относится к генетическим признакам, которые передаются по наследству. Рост – это полигенный признак, он связан с большим числом генов. Генетический контроль роста действует на протяжении всего периода роста. Гены контролируют процессы роста, главным образом, через факторы роста и гормоны. Выделено несколько специфических факторов, стимулирующих рост (фактор роста нервов, фактор роста фибробластов и др.). Один из основных стимуляторов роста тканей является гормон роста (соматотропин), выделяемый передней долей гипофиза. Гормон роста способствует образованию новых хрящевых клеток, стимулирует синтез белков в клетках. Большую роль в регуляции роста человека играют гормоны щитовидной железы, половые гормоны. Имеются данные, свидетельствующие о наличии тканеспецифических ингибиторов роста. Они получили название кейлонов. Кейлоны – это белки, действие которых заключается в подавлении или замедлении скорости деления клеток в тех тканях, которые их вырабатывают.
Хотя роль наследственности для роста велика, но все же она не является единственным фактором, определяющим рост. Правильно рассматривать роль наследственности как некую ориентировочную программу, согласно которой рост человека может оказаться, например, в пределах от 160 до 180 сантиметров. Каким он будет на самом деле во многом зависит от условий жизни, которые могут тормозить наследственную программу или способствовать ее реализации. Большое значение для процесса роста имеют питание, физическая нагрузка, психологические воздействия. Таким образом, в процессе роста имеет место взаимосвязь биологического и социального в период детства и молодости, когда организм растет.
С ростом и развитием связано формирование определенных конституционных типов. Под этим понятием понимают особенности строения тела, т.е. особенности внешних форм тела, особенности функций и психологической деятельности человека. В зависимости от строения тела, внешних форм тела выделяют различные типы телосложения. Вне зависимости от половой принадлежности в российской медицинской школе принято рассматривать типы телосложения, описанные в свое время академиком М. В. Черноруцким. Согласно этой классификации выделяют три типа телосложения: 1) Астенический тип; 2) Нормостенический; 3) Гиперстенический. За рубежом и в современном спортивном сообществе более популярна классификация по Шелдону. Но принцип обеих классификаций одинаков (табл. 1).
Табл. 1. Классификация типов телосложения
Классификация по академику М.В. Черноруцкому |
Классификация по Шелдону |
Астенический |
Эктоморфный |
Гиперстенический |
Эндоморфный |
Нормостенический |
Мезоморфный |
Каждый тип телосложения имеет свои особенности строения и функций (табл. 2 ).
Табл. 2. Морфологические типы конституции (типы телосложения)
Типы телосложения |
Особенности |
|
строения |
функции |
|
1. Астенический |
Длинные и тонкие конечности, короткое туловище, узкая и плоская грудная клетка с острым эпигастральным углом, низкая диафрагма, длинная шея, узкие плечи, продолговатое лицо, слабо развитая мускулатура, тонкая и бледная кожа. |
Повышена возбудимость нервной системы, склонность к неврозу, гипотензии, опущению внутренних органов, язвенной болезни, туберкулезу. |
2. Нормостенический |
Относительно пропорциональные размеры тела, хорошо развита костная и мышечная ткань, широкий плечевой пояс, выпуклая грудная клетка. |
Люди энергичны, уверены в себе, склонны к заболеваниям верхних дыхательных путей, двигательного аппарата, к развитию атеросклероза, инфаркта миокарда. |
3. Гиперстенический |
Относительно длинное туловище и короткие ноги, шея короткая, голова круглая, широкая грудная клетка, высокая диафрагма, выступающий живот. |
Люди общительны, подвижны, практичны, склонны к гипертензии, ожирению, диабету, атеросклерозу, желчнокаменной болезни, преобладают процессы ассимиляции, повышена функция половых желез и надпочечников. |
Репродуктивный период (период зрелости) – это период стабильного функционирования органов и систем. Характеризуется относительной устойчивостью к различным воздействиям.
Пострепродуктивный период. Пострепродуктивный период связан со старением организма. Выяснить механизмы старения и смерти высших организмов, в том числе человека, является одной из важнейшей и самой сложной задачей современной биологии и медицины. Почему некоторые люди живут более ста лет, но ни одна из мышей, которые являются также млекопитающими, не живут более 4 лет. У человека в 80-летнем возрасте обычно более морщинистая кожа, менее сильные мускулы, более слабое зрение, чем он имел в 30 лет. Какова причина тех изменений к худшему, которые произошли за полвека. Обратимы ли эти изменения? Можно ли было предотвратить их? Можно ли продлить человеческую жизнь? Вот найти ответы на эти вопросы и многие другие, связанные со старением, должна наука, которая получила название геронтология. Конечная цель геронтологии состоит в том, чтобы установить природу и причины старения человека. Это является задачей в целом биологии и медицины.
Старение – это неизбежно возникающий, закономерно развивающийся разрушительный процесс, ограничивающий приспособительные возможности организма, сокращающий продолжительность жизни и увеличивающий вероятность смерти. А применительно к людям необходимо добавить, что это процесс, способствующий возрастной патологии. Из определения следует, что изменения, которые возникают в процессе старения носят неблагоприятный характер, они повышают вероятность гибели организма. Старение ведет к уменьшению способности организма приспосабливаться к окружающей среде. Это свойственно представителям всех видов и неизбежно происходит при увеличении возраста. В этой связи старение следует рассматривать как фундаментальное свойство живых организмов. Со старением связан широкий круг патологических процессов: сердечно-сосудистые заболевания, возрастная недостаточность иммунной системы, дисфункция мозга. В старости наблюдается снижение функций всех органов чувств. Существенные изменения происходят в репродуктивной системе, страдает функция мочевыделительной системы.
Относительно причин и механизмов старения существует около 500 различных гипотез. Все эти гипотезы в отдельности не отражают сущности сложных процессов, которые происходят при старении. Большинство современных гипотез можно свести к двум главным направлениям, которым в настоящее время уделяется особое внимание при рассмотрении старения: 1) старение – это генетически запрограммированный процесс; 2) старение связано с накоплением повреждений, случайно (стохастически) возникающих, в процессе жизни организма.
Согласно первого направления старение находится под прямым генетическим контролем, оно генетически запрограммировано. Ранее мы отмечали, что развитие организма в целом – это реализация генетической программы, полученной от родителей. Поскольку старение тоже генетически запрограммировано, можно считать, что старение по существу продолжение развития. Старение можно рассматривать как закономерную стадию индивидуального развития. Экспериментально на животных показано, что если замедлить развитие и рост организма путем ограничения питания, то это приводит к замедлению старения. Это указывает, что развитие и старение - это стороны одного и того же процесса. Генетическое предопределение старения является сущностью «программных гипотез» старения. Признавая генетический контроль старения и продолжительности жизни, пока трудно сказать насколько сильно этот контроль влияет на старение и через какие конкретные генетические механизмы он осуществляется. Специальных генов, прямо определяющих процессы старения в организме, пока не выявлено.
Согласно второго направления в основе наблюдаемых изменений при старении лежит накопление повреждений, случайно (стохастически) возникающих в организме. Такой механизм отражает сущность «стохастических гипотез» старения. Эти изменения происходят в первую очередь на молекулярном уровне с повреждением ДНК, РНК, различных белков, в том числе белков хроматина, ферментов, липидов мембран клеток. Сдвиги в этих молекулах, а также в мембранах клеток, формируют возрастные изменения клеток, тканей, органов и целого организма. Все это снижает жизнеспособность всего организма, повышает вероятность смерти. События, ведущие к старению можно представить в виде следующей схемы:
Внешние и внутренние факторы
↓ ↓ ↓ ↓ ↓
Молекулярные повреждения (стохастический процесс)
↓
Ухудшение структуры и функции органелл
↓
Ухудшение функции клеток
↓
Ухудшение функций тканей и органов
↓
Снижение жизнеспособности организма
↓
Повышение вероятности смерти
Какие молекулы подвергаются повреждениям и изменениям в первую очередь? Этими молекулами являются молекулы ДНК. Повреждение ДНК нужно отнести к числу самых существенных причин старения. Среди повреждений ДНК – это одно- и двунитевые разрывы молекулы, повреждение азотистых оснований, межцепочечные сшивки, сшивки ДНК-белок, депуринизация и др. Такие повреждения ДНК в конечном итоге приводят к соматическим мутациям. Повреждение ДНК происходит спонтанно и с высокой скоростью. Примерно каждую секунду в геноме каждой клетки человека спонтанно возникает одно повреждение ДНК. Это очень большое число повреждений ДНК, если принять во внимание биологическую роль ДНК. Какие факторы повреждают ДНК? Во-первых, – это действие внутренних факторов, продуктов обмена веществ. Особую роль в повреждении ДНК (да и других молекул) играют активные формы кислорода: О2─ - супероксидный радикал, ОН. - гидроксильный радикал, перекись водорода, которые являются генотоксическими продуктами метаболизма в клетках. Подсчитано, что за 70 лет жизни человека организм производит около одной тоны радикалов кислорода. Поэтому в настоящее время наиболее разрабатываемой является свободнорадикальная теория старения. Правда, необходимо отметить, что подавляющее большинство активных форм кислорода нейтрализуется еще до того, как они успеют повредить те или иные компоненты клетки. В их нейтрализации принимают участие основные эндогенные факторы антиоксидантной защиты организма, к которым относятся некоторые ферменты (супероксиддисмутаза, каталаза) и витамины (β-каротин, α-токоферол). Кроме активных форм кислорода, повреждающим действием обладают перекиси липидов и другие активные молекулы, образующиеся в процессе нормального обмена веществ. Во-вторых, повреждающим действием обладают внешние факторы (ионизирующее излучение, температурный фактор, химические вещества). Однако надо иметь ввиду, что при действии как внутренних, так и внешних факторов основной мишенью действия повреждающих агентов является ДНК.
Старение, по крайней мере у млекопитающих и человека, проявляется в зрелом возрасте, но процессы, которые к нему приводят, возникают значительно раньше и составляют причину старения. Уже в ДНК молодых здоровых людей обнаруживаются повреждения ДНК. По-видимому, такие молекулярные изменения составляют стадию инициации старения, но лишь спустя много лет после возникновения таких повреждений в организме обнаруживаются существенные физиологические или даже патофизиологические изменения.
Однако не надо считать, что изменение ДНК это единственный фактор снижения жизнеспособности организма при старении. Во-первых, повреждение ДНК запускает изменения, которые происходят при старении в других молекулах, в первую очередь белках и РНК. Во-вторых, другие молекулы непосредственно повреждаются теми же факторами, что и ДНК. В результате молекулярных дефектов менее эффективно будет осуществляться функция органелл клеток. Например, повреждение липидов мембран может отрицательно сказываться на функции митохондрий, что нарушает систему энергообеспечения организма. Дефекты в белках, РНК будут снижать функциональную активность рибосом. Ухудшение функции органелл будет понижать эффективность работы клеток. В результате уменьшения эффективности работы клеток будет ухудшаться работа тканей, органов и их систем. Например, изменения в нервных клетках будут влиять на функции мозга, изменения в лимфоцитах понизят эффективность иммунной системы и т. д. Ухудшение работы тканей и органов приводит к уменьшению жизненности организма в целом и повышению вероятности смерти.
Как было отмечено ранее, скорость спонтанного повреждения ДНК очень высокая. Если бы не было сдерживающих факторов, то при такой скорости повреждения ДНК организм старился очень быстро. Но подавляющее большинство спонтанных повреждений ДНК ликвидируется с участием репарирующих ферментов. Большинство из индуцированных ионизированным облучением повреждений ДНК также репарируется. Механизм репарации ДНК играет важную роль в сдерживании скорости старения и продолжительности жизни. В ряду различных видов млекопитающих существует прямая корреляция между способностью клеток определенного организма к репарации ДНК и видовой продолжительностью жизни. Предполагают, что гены, которые обеспечивают репарацию ДНК, определяют и жизнеспособность организмов и продолжительность жизни. Способность к репарации повреждений ДНК, эффективность работы ферментов, обеспечивающих эту способность, - одна из биологических основ долголетия. Ученые провели полногеномный анализ столетних людей, доживших до 105 и 110 лет. В ходе исследования геномов было выявлено, что у людей старше 105 лет особо активны гены, препятствующие повреждению ДНК и «отвечающие» за ее репарацию. Однако несмотря на процессы репарации ДНК часть повреждений ДНК проходит через барьер репарации и приводит к соответствующим изменениям в организме.
Какие же изменения на разных уровнях организации организма наблюдаются при старении? На генетическом уровне: 1. Повреждение ДНК; 2. Увеличение прочности связывании ДНК с белками гистонами; 3. Снижение транскрипционной активности генов. На молекулярном уровне: 1. Нарушение структуры и функции белков, липидов; 2. Нарушение функции ферментов; 3. Повреждение белка коллагена. На клеточном уровне: 1. Повреждение мембран клеток; 2. Снижение способности клеток к делению ( это один из основных функциональных признаков старения клеток); 3. Уменьшение числа функционирующих клеток в ряде органов (тимус, головной мозг); 4. Увеличение объема клеток; 5. Изменение состояния ядерных оболочек; 6. Нарушение структуры митохондрий (набухание, разрушение крист и внутренней мембраны), появление гигантских митохондрий; 7. Повреждение мембран лизосом и выход гидролитических ферментов; 8. Уменьшение активности рибосом. На тканевом и органном уровне: 1. Избыточное развитие и качественные изменения соединительной ткани; 2. Атрофические и дистрофические изменения в отдельных клетках тканей и органов; 3. Уменьшение количества клеток паренхиматозных органов; 4. Ухудшение функций тканей и органов. Системный уровень: Снижение эффективности различных систем организма в обеспечении нормальной жизнедеятельности.
Все указанные изменения, возникающие при старении, ограничивают продолжительность жизни (ПЖ). У человека выделяют хронологическую и биологическую ПЖ. Хронологическая – это средняя статистическая ПЖ людей. В настоящее время средняя ПЖ в странах с высокими социально-экономическими условиями жизни составляет около 80 лет (Япония, Австрия, Италия, Швеция). Однако во многих развивающихся странах она не достигает 40 лет. В нашей стране средняя ПЖ составляет около 73 лет. Причем женщины живут на 3-5 лет дольше. Что касается биологической ПЖ, то разные авторы дают разные цифры – от 100 до 200 лет. Существование биологической ПЖ указывает, что средняя ПЖ, которая в настоящее время имеет место – это не предел. В настоящее время ведутся поиски путей замедления скорости старения и увеличения продолжительности жизни.
С медицинской точки зрения старость – патологическое состояние. Вопросы изменения состояния органов и систем при старении является предметом изучения патологов и клиницистов. В настоящее время сформировалась медицинская наука гериатрия – наука о болезнях в пожилом и старческом возрасте и нормализации физиологических процессов в старости.
Направлениями продления жизни могут быть: 1) улучшение социальных условий жизни людей; 2) соответствующий образ жизни (двигательная активность, ограничение калорийности пищи); 3) использование геропротекторов, в частности антиоксидантов, способных подавлять активность свободных радикалов. Не исключено, что уже в ближайшем будущем биологи и медики найдут средства, снижающие скорость спонтанного повреждения клеток или увеличения их способности залечивать такие повреждения.
